Pacienții care urmează o dietă renală tradițională găsesc adesea că consumă o „dietă nesănătoasă”, ceea ce înseamnă că dieta este săracă în fructe și legume proaspete, cereale integrale și produse lactate.
În cele din urmă, acest lucru se traduce printr-o dietă săracă în fibre și micronutrienți și bogată în grăsimi. În timp ce dieta convențională, dacă este urmată conform prescripției, poate menține potasiul și fosforul seric în limite normale, poate contribui, de asemenea, la modificarea funcției gastrointestinale (GI) și, potențial, la insuficiențele micronutrienților.
Tractul GI este un organ activ din punct de vedere metabolic, care contribuie la funcția imunitară și la disponibilitatea aminoacizilor, glucozei, lipidelor și micronutrienților pentru o conversie metabolică ulterioară de către ficat. În plus, tractul gastrointestinal adăpostește o populație uriașă de bacterii, care la rândul lor contribuie la starea metabolică a corpului. Se crede că tractul intestinal uman conține peste 10 14 bacterii cu peste 500 de tipuri diferite (J Renal Nutr 2005; 15: 77-80).
S-a sugerat că tulburările tractului gastrointestinal apar atunci când se dezvoltă boala renală cronică (CKD). De exemplu, bacteriile din intestin devin versuri mai aerobe anaerobe. Escherichia coli și Bifidobacterium sunt exemple de bacterii aerobe și, respectiv, anaerobe.
Echilibrul dintre aceste două tipuri de bacterii se poate modifica și poate duce la o creștere a toxinelor și la o scădere a nutrienților disponibili. Terapiile potențiale pentru îmbunătățirea mortalității și a sănătății generale ar putea viza tractul gastrointestinal prin corectarea echilibrului dintre microbii aerobi și anaerobi prin suplimentarea bacteriilor (de exemplu, probiotice), eliminarea toxinelor prin deșeurile fecale (absorbanți intestinali) sau furnizarea de substrat, cum ar fi fibrele, susține un anumit tip de bacterii (de exemplu, prebiotice).
Indoxilsulfat și p-crezolsulfatul sunt două toxine uremice care au fost studiate în legătură cu CKD. Ambele toxine sunt asociate cu rezultate negative în populația de CKD.
Indoxilsulfatul provoacă inflamații, disfuncții endoteliale și tulburări ale metabolismului osos și este asociat cu o pierdere a funcției renale (Purificatorul de sânge 2010; 29: 130-136); p-crezolsulfatul este o moleculă pro-inflamatorie care afectează monocitele și limfocitele. În plus, în studiile observaționale, p-crezol, care este convertit în p-crezolsulfat, este asociat cu mortalitate, boli cardiovasculare, complicații infecțioase și simptome uremice.
Producția de indoxilsufat și p-crezolsulfatul începe în tractul GI. Bacteriile aerobe au o enzimă numită triptofanază, care transformă triptofanul în intestin în indol. Indolul este absorbit în sânge din tractul gastro-intestinal și se deplasează către ficat, unde este transformat în sulfat de indoxil. În mod similar, tryozina din intestin este convertită în p-crezol.
Pentru a reduce cantitatea de toxine produse, pacienții ar trebui să consume mai puțin triptofan sau tirozină, ambele fiind găsite în alimentele bogate în proteine sau să absoarbă și să elimine precursorii înainte de a părăsi intestinul. Dietele cu conținut scăzut de proteine sunt recomandate pacienților de pre-dializă; totuși, acest tip de dietă nu ar fi recomandat pacienților cu dializă. Prin urmare, s-au sugerat adsorbanți orali și pre- și probiotice. Un adsorbant oral „absoarbe” ureea și alte toxine și le elimină prin fecale.
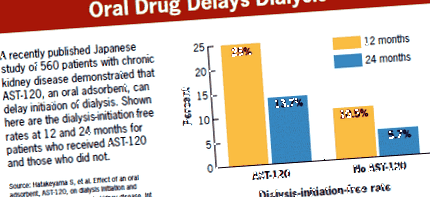
AST-120 este un adsorbant oral care a fost studiat la șobolani și oameni. Într-un studiu japonez cu pacienți cu CKD, AST-120 a fost comparat cu îngrijirea standard. Rata fără inițiere a dializei a fost semnificativ mai mare în grupul AST-120 comparativ cu grupul non-AST-120 la 12 și 24 de luni (25% și, respectiv, 13,7% față de 10,5% și respectiv 5,7%). Cu toate acestea, această rată îmbunătățită nu s-a tradus prin rate de supraviețuire îmbunătățite în grupul AST-120 (Int J Nefrol 2012; publicat online înainte de tipărire. Curr Med Res Opin. 2009; 25: 1913-1918).
În cele din urmă, pre- și probiotice împreună într-un simbiotic au fost testate la pacienții cu hemodializă (HD) pentru a vedea dacă cantitatea de p-crezolul poate fi redus (Transplant de Dial Nephrol 2011; 26: 1094-1098). Simbioticul a fost testat la nouă pacienți cu HD timp de două săptămâni. Pacienții au fost chestionați cu privire la obiceiurile intestinale și p-crezolul a fost măsurat înainte și după tratament. La sfârșitul tratamentului, p-crezolul a scăzut semnificativ și volumul și consistența scaunului s-au îmbunătățit.
Aceste tipuri de intervenții pot fi mai puțin costisitoare și pot avea efecte pozitive de anvergură asupra stării generale de sănătate a pacienților, dar trebuie făcute mult mai multe cercetări în acest domeniu înainte ca aceste terapii să devină practică standard.
- Dieta pe bază de plante care nu este asociată cu hiperkaliemie gravă în CKD - Știri renale și urologice
- Purina® Pro Plan® Dietele veterinare NF Funcția renală Hrana uscată pentru câini
- Persoanele cu colesterol ridicat ar trebui să elimine carbohidrații, nu grăsimile saturate
- Activitatea urokinazei renale pielonefrite la șobolani în dietele esențiale cu acizi grași SpringerLink
- Toxine alimentare naturale