1 Departamentul de Medicină Clinică și Experimentală, Școala de Nefrologie, Universitatea din Pisa, Via Paradisa 2, 56100 Pisa, Italia
Abstract
Prezentarea cazului. Bărbat în vârstă de 53 de ani cu hipertensiune esențială și proteinurie nefrotică (1,3 gr/24 ore) și cu funcție renală normală (eGFR-MDRD 123 ml/min/1,73 m2) a fost internat la secția de nefrologie; biopsia renală a prezentat FSGS; doi ani mai târziu, pacientul a prezentat ulcerații și gangrenă ischemică a vârfurilor degetelor mâinii drepte IV și V; analiza genetică a demonstrat polimorfismul genelor metilenetetrahidrofolat reductazei C677T (heterozigot C677T/1298AC cu valoarea normală a homocisteinei) și a mutațiilor genei protrombinei G20210A și a inhibitorului activatorului plasminogen-1 4G/5G 675 cu o ușoară creștere a valorii sale. După cinci ani de la biopsie, proteinuria de 24 de ore era încă în jur de 1-1,3 g/moare; funcția renală era încă normală (eGFR 107 ml/min/1,73 m 2). Aceste date sunt împotriva diagnosticului anterior de FSGS primar. Ipotezăm că trombofilia genetică poate explica toate semnele clinice ale pacientului nostru. Concluzii. Modificările genelor trombofiliei trebuie excluse la pacienții cu diagnostic bioptic de FSGS „primar”, în special dacă sunt atipici clinic.
1. Fundal
Glomeruloscleroza focală segmentară este un model histopatologic al leziunilor, în care „focal” se referă la implicarea unei minorități de glomeruli, iar „segmentar” se referă la implicarea unei porțiuni din smocul capilar glomerular, cauzat de leziunea podocitelor. Clinic manifestă proteinurie, care poate evolua spre sindrom nefrotic și, în cele din urmă, pentru a pune capăt insuficienței renale. Unele date clinice și analitice pot fi extrem de utile pentru a diferenția formele primare sau genetice ale FSGS de tipurile de hiperfiltrare.
O creștere lentă a proteinuriei și absența hipoalbuminemiei și edemului chiar și în prezența proteinuriei masive sunt foarte caracteristice hiperfiltrării FSGS. Acest lucru este în contrast cu apariția rapidă a sindromului nefrotic și o scădere rapidă a funcției renale la tipurile primare.
Distincția între diferitele tipuri de FSGS este crucială, deoarece tratamentul lor este radical diferit.
Microangiopatia trombotică este o cauză rară a FSGS adaptiv datorită trombofiliei moștenite. Scopul acestei lucrări este de a sugera că trombofilia moștenită ar trebui considerată ca o posibilă cauză a FSGS secundar.
2. Prezentarea cazului
În această lucrare raportăm cazul unui bărbat italian în vârstă de 53 de ani (greutate corporală 85 Kg, înălțime 1,85 m și IMC 24,8 kg/m 2) cu familiaritate pentru bolile cardiovasculare și renale (tatăl, afectat de hipertensiune arterială și boală renală, a murit la 55 de ani din cauza infarctului miocardic acut). Pacientul fusese diagnosticat cu hipertensiune arterială esențială moderată la vârsta de 42 de ani și tratat cu terapie combinată de blocante ale canalelor de calciu (amlodipină 5 mg) și ACEI (ramipril 5 mg). La vârsta de 47 de ani, analizele de laborator au demonstrat hipercolesterolemie (colesterol total 270 mg/dL) și proteinurie nefrotică (1,3 gr/24 h) cu funcție renală normală (creatinină serică 0,8 mg/dL, eGFR-MDRD 123 mL/min/1,73 m 2 ).
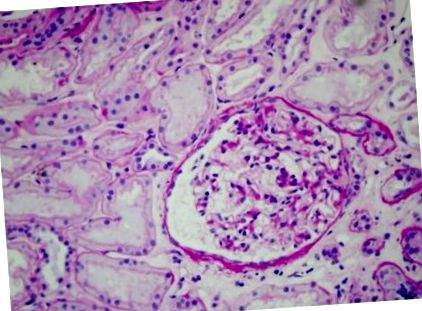
Pacientul a fost internat într-o secție de nefrologie unde a fost efectuată biopsia renală. Materialul de biopsie conținea 19 glomeruli: scleroza glomerulară globală și infiltrarea limfocitelor au fost demonstrate în patru glomeruli (Figura 1), zone mici de scleroză segmentară au fost găsite în alți doi glomeruli, iar restul de 13 glomeruli au prezentat doar anomalii minore (Figura 2). Au fost observate, de asemenea, semne rare de atrofie tubulară, fibroză interstițială și scleroză interlobulară. Examinarea imunofluorescenței nu a arătat depunerea de fragmente IgA, IgG, IgM, C1q, C3, k și lambda. Diagnosticul final a fost glomeruloscleroza focală și segmentară primară (FSGS). Conform acestui diagnostic, pacientul a fost tratat cu restricție dietetică de sodiu, medicamente antihipertensive (ramipril 5 mg și losartan 100 mg) și terapie cu doze mari de glucocorticoizi (metilprednisolonă 1000 mg ev o dată pe lună timp de trei luni) urmată de prednison 1 mg/kg/mor (75 mg), cu reducerea progresivă a dozei, timp de 6 luni. La sfârșitul tratamentului, proteinuria a fost Figura 1
Pe baza analizelor genetice, pacientul a fost tratat cu acid folic 400 mcg/matriță și pentoxifilină 800 mg timp de 6 luni și a avut tratament pe termen lung cu acid acetilsalicilic 100 mg/matriță. Pacientul în vârstă de 53 de ani a fost evaluat în clinica noastră de nefrologie anul acesta. De fapt, tensiunea arterială este de 140/90 mmHg în tratamentul cu ramipril 5 mg și losartan 100 mg; analiza urinei arată pH 5,5, gravitația urinară 1020, proteine 30 mg/dL; Excreția de proteine urinare 24 de ore este în intervalul 1-1,3 g/matriță; funcția renală este încă normală (sCr 0,76 mg/dL și eGFR 107 mL/min/1,73 m 2). Aceste date sunt împotriva diagnosticului anterior de FSGS primar. Scopul acestei lucrări este de a sugera trombofilia moștenită ca posibilă cauză a FSGS secundar la acest pacient.
3. Discuție
Protrombina (PT) (G20210A) [2], metilenetetrahidrofolat reductaza (MTHFR) (C677T) [1] și Factorul V Leiden (G1691A) [3] sunt factori genetici de risc recunoscuți pentru tromboza venoasă, în timp ce rolul lor la pacienții cu rămâne de clarificat tromboza arterială. Factorul V Leiden, PT G20210A și polimorfismele MTHFR C677T cresc riscul de infarct miocardic, accident vascular cerebral ischemic și boli vasculare periferice, în special la pacienții mai tineri și la femei [4]. De asemenea, s-a demonstrat că alela G20210A PT reprezintă un factor de risc moștenit pentru sindromul coronarian acut [5]. Mai mult, pacienții cu hipertensiune esențială, C677TT homozigot sau genotipuri C677CT/1298AC dublu heterozigoți sunt predispuși să dezvolte nefroscleroză hipertensivă și insuficiență renală cronică [6]. Nefroscleroza, care este frecventă în glomerulonefrita cronică, poate fi determinată de coagularea sângelui intraglomerulară, ca în microangiopatia trombotică [7].
Glomeruloscleroza focală segmentară, considerată odată o singură boală, este acum privită ca un grup de sindroame clinico-patologice care împart o leziune glomerulară comună, mediată de diverse insulte direcționate către podocite. În mod obișnuit, FSGS este clasificat ca o formă primară, idiopatică, mediată de factori de permeabilitate circulanți sau ca o formă secundară. Glomeruloscleroza focală segmentară are ca rezultat, de obicei, mai multe setări mediate de hiperfiltrare hipertrofie glomerulară (de exemplu, oligonefronie, agenezie renală unilaterală sau cicatrici din cauza nefropatiei de reflux sau a bolilor sistemice, precum obezitate severă, hipertensiune arterială, diabet zaharat, vasculită, lupus și trombită glomerulară microangiopatie în sindromul antifosfolipidic [8]). Alte cauze cunoscute includ infecția cu HIV, nefropatia cu heroină, interferonul și medicamentele pamidronato.
FSGS primar se caracterizează prin proteinurie severă și progresia insuficienței funcționale renale, în timp ce formele secundare, în special forma adaptativă, prezintă doar proteinurie modestă, ușoară progresie a insuficienței renale și un prognostic mai bun [9].
Este important să distingem FSGS primar de cel secundar, deoarece tratamentul este radical diferit. Terapia FSGS secundară constă în inhibarea angiotensinei decât terapia imunosupresivă sub formă idiopatică.
Într-adevăr, datele clinice ale pacientului nostru sunt de acord cu raportul recent al unei asocieri între glomerulonefrita cronică și trombofilia moștenită. Trombofilia moștenită a apărut la opt dintre cei 17 pacienți (47%) cu boală vasculară renală idiopatică: s-au constatat mutații PT G20210A, mutație factor V Leiden și homozigozitate pentru polimorfismul MTHFR C677T. Rețineți că la 7/11 pacienți diagnosticul bioptic a fost FSGS. Niciun pacient nu a avut sindrom nefrotic și funcția renală a fost redusă moderat (am calculat un eGFR mediu de 45 ml/min/1,73 m 2, variind între 15 și 79 ml/min/1,73 m 2) [10, 11].
4. Concluzii
În ansamblu, rapoartele din literatura de specialitate și datele pacientului nostru sugerează că factorii trombofilici moșteniți menționați pot duce la FSGS printr-o microangiopatie trombotică și cicatrici glomerulare datorate nefrosclerozei hipertensive; în plus, acest raport de caz confirmă că mutația raportată poate duce la scleroză vasculară renală.
Lista de abrevieri
| MDRD: | Dieta modificată în bolile renale |
| PT: | Protrombină |
| MTHFR: | Metilenetetrahidrofolat reductază |
| FSGS: | Glomeruloscleroza focală segmentară. |
Consimţământ
Consimțământul informat scris a fost obținut de la pacient pentru publicarea acestui raport de caz și a oricăror imagini însoțitoare. O copie a consimțământului scris este disponibilă spre examinare de către editorul acestui jurnal
Conflict de interese
Autorii declară că nu au niciun conflict de interese.
Referințe
- A. S. Hussein, „Prevalență ridicată a trei polimorfisme protrombotice în rândul palestinienilor: factorul V G1691A, factorul II G20210A și metilenetetrahidrofolat reductaza C677T” Journal of Thrombosis and Thrombolysis, vol. 34, pp. 383–387, 2012. Vizualizați la: Site-ul editorului | Google Scholar
- F. Bhaijee, B. Jordan, D. J. Pepper, R. Leacock și W. A. Rock Jr., „Tromboza venoasă atât cu mutații ale factorului heterozigot V Leiden, (R507Q), cât și ale factorului II, (G20210A)” Științe clinice de laborator, vol. 25, pp. 199–205, 2012. Vezi la: Google Scholar
- Y. Saemundsson, S. V. Sveinsdottir, H. Svantesson și P. J. Svensson, „Factorul homozigot V Leiden și heterozigoza dublă pentru factorul V Leiden și mutația protrombinei” Journal of Thrombosis and Thrombolysis, vol. 36, pp. 324–331, 2013. Vizualizare la: Google Scholar
- F. Burzotta, K. Paciaroni, V. De Stefano și colab., „Prevalența crescută a variantei genei de protrombină G20210A în sindroame coronariene acute fără factori de risc metabolici sau dobândiți sau cu grad limitat de boală”. European Heart Journal, vol. 23, nr. 1, pp. 26-30, 2002. Vizualizare la: Site-ul editorului | Google Scholar
- R. J. Kim și R. C. Becker, „Asocierea între factorul V Leiden, protrombina G20210A și mutațiile metilenetetrahidrofolat reductazei C677T și evenimentele sistemului circulator arterial: o meta-analiză a studiilor publicate” American Heart Journal, vol. 146, nr. 6, pp. 948–957, 2003. Vizualizare la: Site-ul editorului | Google Scholar
- P. Koupepidou, C. Deltas, T. C. Christofides, Y. Athanasiou, I. Zouvani și A. Pierides, „Genotipurile MTHFR 677TT și 677CT/1298AC la pacienții ciprioti pot predispune la nefroscleroză hipertensivă și insuficiență renală cronică”. Angiologie internațională, vol. 24, nr. 3, pp. 287–294, 2005. Vizualizare la: Google Scholar
- N. L. Kozlovskaia, L. A. Bobrova, V. V. Shkarupo, V. A. Varshavskiǐ și N. G. Miroshnichenko, „Caracteristicile clinicomorfologice ale tulburărilor renale la pacienții cu trombofilie genetică” Terapevticheskiǐ Arkhiv, vol. 81, nr. 8, pp. 30–36, 2009. Vizualizare la: Google Scholar
- M. C. Amigo, „Disezaza rinichilor în sindromul antifosfolipidic” Clinici de boli reumatice din America de Nord, vol. 32, pp. 509–522, 2006. Vizualizare la: Google Scholar
- J. A. Velosa, K. Holley, V. E. Torres și K. P. Offord, „Semnificația proteinuriei asupra rezultatului funcției renale la pacienții cu glomeruloscleroză focală segmentară”. Procedurile clinicii Mayo, vol. 58, nr. 9, pp. 568–577, 1983. Vezi la: Google Scholar
- R. L. Goforth, H. Rennke și S. Sethi, „Scleroza vasculară renală este asociată cu trombofilii moștenite”. Kidney International, vol. 70, nr. 4, pp. 743–750, 2006. Vizualizare la: Site-ul editorului | Google Scholar
- M. Bochud, M. Burnier și I. Guessous, „Top trei aplicații de farmacogenomică și medicină personalizată la legătura dintre fiziopatologia renală și medicina cardiovasculară” Farmacogenomică actuală și medicină personalizată, vol. 9, nr. 4, pp. 299–322, 2011. Vezi la: Google Scholar
- Glomeruloscleroză focală segmentară MedlinePlus Enciclopedia Medicală
- Articolul complet Glomeruloscleroza focală segmentară la un pacient cu asimptomatic bilateral mare
- Mastocitoza cutanată Centrul de informații despre bolile genetice și rare (GARD) - un program NCATS
- Variația genetică și epigenetică, dar nu dieta, modelează metilomul spermei - ScienceDirect
- Origini genetice și de mediu ale obezității relevante pentru reproducere - ScienceDirect