Glicogenul este o pulbere amorfă albă, slab solubilă în apă și ușor hidrolizată de acizi minerali pentru a produce reziduuri de glucoză.
Termeni asociați:
- Gluconeogeneză
- Glucoză
- Acizi grași
- Hipoglicemie
- Enzime
- Adenozin trifosfat
- Insulină
- Glucidele
- Lipide
- Proteină
Descărcați în format PDF
Despre această pagină
GLICOGEN
Introducere
Glicogenul este o polizaharidă a glucozei care apare în majoritatea celulelor de mamifere și nemamifere, în microorganisme și chiar în unele plante. Este o sursă importantă și rapid mobilizată de glucoză stocată. La vertebrate este depozitat în principal în ficat ca rezervă de glucoză pentru alte țesuturi. În celulele hepatocitare se acumulează și se mobilizează în funcție de disponibilitatea glicemiei și a celulelor extrahepatice. Glicogenul este, de asemenea, stocat în mușchi și celulele adipoase. În mușchi pare să fie utilizat în principal în scopuri energetice ca combustibil metabolic pentru glucoliză producând glucoză 6-fosfat. Astfel, glicogenul joacă un rol crucial ca sursă de energie sistemică și celulară și, de asemenea, ca depozit de energie. Un număr mare de enzime și hormoni controlează sinteza și degradarea glicogenului. În consecință, depozitele de glicogen din corpul uman pot varia dramatic din cauza dietei, a exercițiilor fizice și a stresului.
Glicogen
Glicogeneza
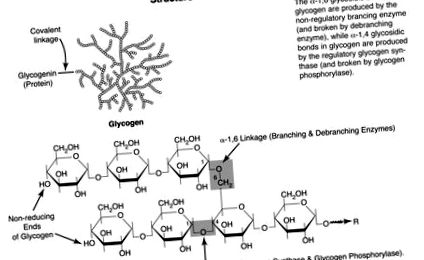
Structura glicogenului este reprezentată în FIG. 23-1 . Ramificarea moleculei de glicogen are loc la o frecvență medie din fiecare zece reziduuri de glucoză. Ramificarea mărește solubilitatea, precum și viteza cu care glucoza poate fi stocată și recuperată. Fiecare moleculă de glicogen are o proteină, glicogenină, legată covalent de polizaharidă. Lanțurile liniare de glicogen constau din molecule de glucoză legate între ele prin legături glicozidice α-1,4. La fiecare dintre punctele ramificate, două molecule de glucoză sunt legate între ele prin legături glicozidice α-1,6. Capetele nereducătoare ale moleculei de glicogen sunt locurile în care apar atât sinteza, cât și degradarea.
Calea prin care glucoza-6-fosfat (Glc-6-P) este convertită în glicogen este prezentată în FIG. 23-2 . După fosforilarea glucozei de către hexokinază (HK) sau glucokinază, Glc-6-P poate fi transformat în glucoză-1-fosfat (Glc-1-P) de către enzima reversibilă, fosfoglucomutaza (PGM). Această reacție, ca și cea pentru fosforilarea glucozei, necesită Mg ++ ca cofactor. Glc-1-P este apoi transformat în nucleotidă activă, uridină difosfat-glucoză (UDP-Glc, FIG. 23-3 ), prin acțiunea UDPGlc pirofosforilazei. UDP-glucoza devine acum un punct ramificat pentru intrarea în calea acidului uronic hepatic (prin UDP-glucuronat, vezi Capitolul 29), sinteza lactozei în glanda mamară (prin UDP-galactoză) sau sinteza glicogenului în mai multe țesuturi (prin activitate sporită de glicogen sintazat).
Glicogen sintază catalizează pas de limitare a ratei în glicogeneză. Fiind o enzimă cheie, activitatea sa poate fi inhibată de fosforilare, sau activat prin defosforilare (vezi Capitolul 58). Condițiile postprandiale (adică după masă) activează activitatea glicogen sintazei în diferite moduri. Sistemul nervos parasimpatic (SNP) are un efect indirect prin stimularea autonomă a insulină eliberarea din pancreas. Nivelurile ridicate de glucoză stimulează, de asemenea insulină eliberare. Insulina, hormonul anabolic care favorizează stocarea recompenselor alimentare, stimulează activitatea proteina fosfataza 1, care la rândul său stimulează glicogen sintază activitatea cauzând-o defosforilare.
Când lanțul α-1,4 de glicogen se extinde la 11-15 reziduuri de glucoză din cel mai apropiat punct de ramificare, apare ramificarea. Un bloc de 6-7 reziduuri de glucoză este mutat de la capătul unui lanț la alt lanț sau la o poziție internă a aceluiași lanț. Prin catalizarea acestor transferuri de glucan α-1,4 → α-1,6, nereglementarea enzima ramificatoare ajută la crearea de noi site-uri pentru alungire prin glicogen sintază.
Căi metabolice în corpul uman
Tsugikazu Komoda, Toshiyuki Matsunaga, în Biochimie pentru profesioniștii din domeniul medical, 2015
Sinteza glicogenului
Glicogenul este polizaharida de rezervă din organism și este alcătuit în principal din glicogen hepatic. Glicogenul este sintetizat în ficat și mușchi. α-D-Glucoza se combină pentru a forma glicogen continuu. Există un zahăr redus care indică caracteristici de reducere și multe reziduuri nereducătoare care nu indică o reducere a moleculei de glicogen. Când glucoza se leagă de glicogen sau când este scindată, este implicat un reziduu nereducător. Producția de glicogen din glucoză este prezentată în Figura 4.4. O enzimă importantă în sinteza glicogenului este glicogen sintaza. Prin acțiunea acestei enzime, o glucoză se poate combina cu glicogen. Cu toate acestea, atunci când glucoza se leagă de glicogen, aceasta se leagă cu un reziduu nereducător.
Figura 4.4. Derivarea glicogenului și activarea fosforilazei de către adenozin monofosfat ciclic (AMPc).
Sursă: Modificat din Fig. II-15A în Kagawa și Nozawa, Chimie medicală ilustrată (2001, p. 132).
Carbohidrați, nucleozide și acizi nucleici
6.15.2.1 Glicogen bacterian
Carbohidrați și derivații lor, inclusiv taninuri, celuloză și legături conexe
3.14.2.1 Glicogen în bacterii
Glial Glicogen Metabolism ☆
Concluzii finale
Glicogenul reprezintă marea rezervă de energie a creierului. În deceniile de cercetare, glicogenul a fost perceput ca o rezervă de urgență utilizată în cazul deficitului de aprovizionare cu energie, dar date mai recente, obținute odată cu dezvoltarea de noi tehnici, indică acum un rol fiziologic pentru glicogen în raport cu activarea neuronală. Cu toate acestea, unele întrebări cu privire la procesele fiziologice ale glicogenului necesită în continuare explorări suplimentare. În acest context, apariția metodelor spectroscopice RMN neinvazive poate permite dezvoltarea unor abordări experimentale foarte utile pentru a investiga funcția glicogenului la oameni. Localizarea destul de exclusivă a glicogenului în glia și mobilizarea acestuia la activarea neuronală subliniază cooperarea metabolică strânsă care are loc între neuroni și astrocite.
Biomarkeri patologici în toxicologie
Meliton N. Novilla,. Stewart B. Jacobson, în Biomarkers in Toxicology, 2014
Hepatopatie glicogenă
Glicogenul se acumulează în hepatocite secundare xenobioticelor care cresc sinteza glicogenului sau scad glicogenoliza. Analogii glucocorticoizi, cum ar fi dexametazona, sunt stimulatori puternici ai sintezei glicogenului, în special la câine, provocând hipertrofie hepatocelulară centrilobulară secundară acumulării glicogenului (Figura 54.4). Acumularea de glicogen se extinde în regiunile midzonale atunci când efectul are o magnitudine mai mare. Mărimea și greutatea ficatului sunt crescute datorită acumulării crescute de glicogen hepatocelular. Ultrastructural, hepatocitele au acumulări mari de glicogen liber în citosol care deplasează componentele citoplasmatice către periferia celulară. Intercalate în glicogen sunt picături de lipide. Apariția lor este adesea neapreciată datorită faptului că a fost spălată din hepatocite în timpul procesării și eșecul de a părăsi vacuolul lor citoplasmatic clar indică prezența lor.
Figura 54.4. Hepatopatie glicogenă cauzată de administrarea de corticosteroizi la un câine.
(Amabilitatea dr. V. Meador, Covance Laboratories Global Pathology.)
Reconstituind Citoscheletul
Aaron C. Groen,. Timothy J. Mitchison, în Methods in Enzymology, 2014
3.4 Pregătirea glicogenului
Glicogenul din stridie a fost cumpărat de la Sigma-Aldrich. Unele loturi erau impure, după cum se judecă după miros, culoare gălbuie și efecte inhibitoare asupra extractului. Am purificat în mod curent acest glicogen comercial printr-o rundă de precipitații cu etanol. Glicogenul a fost dizolvat în apă la
50 mg/ml, precipitat cu trei volume de etanol și colectat prin centrifugare (5000 × g, 5 min 20 ° C). Supernatantul a fost aruncat și peleta uscată în aer peste noapte. Glicogenul a fost dizolvat în tampon de diluare la 200-300 mg/ml și depozitat în alicote la - 20 ° C. A fost nevoie de ceva timp și de agitație pentru a dizolva complet glicogenul; soluția finală trebuie să fie clară și vâscoasă, fără culoare sau miros. Unele loturi de glicogen comercial ar putea beneficia de o a doua rundă de precipitații cu etanol.
Modele animale de boală umană
Glicogenul este un polimer de glucoză necesar pentru a asigura o sursă continuă de glucoză în timpul postului. Sinteza și degradarea glicogenului sunt strict controlate de mecanisme complexe de reglare și orice perturbare a acestei reglementări poate duce la un rezervor inadecvat de glicogen sau la o acumulare de glicogen în exces sau anormal stocat fie în citosol, fie în lizozomi. Problemele legate de degradarea sau sinteza glicogenului sunt denumite tulburări de stocare a glicogenului (GSD), care sunt boli rare individual, dar colectiv reprezintă o categorie majoră de erori înnăscute ale metabolismului la om. Până în prezent, 11 moduri distincte de GSD sunt reprezentate în modelele animale. Aceste modele oferă un mijloc de a înțelege mecanismele care reglează și execută sinteza și degradarea glicogenului. În această revizuire, rezumăm modele animale care au apărut în mod spontan în natură sau au fost proiectate în laborator prin tehnici de ADN recombinant și clasificăm tulburările metabolismului glicogenului ca tulburări fie de sinteză, fie de degradare.
- Calicivirusul felin - o prezentare generală Subiecte ScienceDirect
- Dermografismul - o prezentare generală Subiecte ScienceDirect
- Dermatofitoza - o prezentare generală a subiectelor ScienceDirect
- Coccus - o prezentare generală a subiectelor ScienceDirect
- Limba geografică - o prezentare generală a subiectelor ScienceDirect