Emulsiile lipidice sunt una dintre ele, care pot îmbunătăți biodisponibilitatea medicamentului prin creșterea permeabilității corneene și/sau prin îmbunătățirea timpului de reținere a formulării în suprafața oculară.
Termeni asociați:
- Anestezie spinală
- Glucoză
- Lipide
- Infuzie
- Nutriție parenterală
- Ulei de soia
- Ulei de pește
- Toxicitate
- Boală de ficat
- Prematuritate
Descărcați în format PDF
Despre această pagină
Un sondaj anual la nivel mondial al noilor date privind reacțiile adverse la medicamente
Sujana Dontukurthy,. Joel Yarmush, în Efectele secundare ale drogurilor Anual, 2015
Eficacitatea resuscitării cu Intralipid
Emulsia lipidică a fost administrată șobolanilor cu toxicitate cardiovasculară tranzitorie indusă de bupivacaină. Viteza de recuperare a fost observată în următoarea ordine: 30% emulsie lipidică> 20% emulsie lipidică> ser fiziologic normal> fără tratament. Autorii au aplicat modelarea farmacocinetică și farmacodinamică pentru a se asigura că emulsia lipidică a avut un efect cardiotonic primar asupra inimii, precum și a provocat o absorbție fizică secundară a anestezicului local (adică teoria scufundării lipidelor) [16 H]. Acest studiu a completat un studiu de modelare anterior care a subliniat teoria scufundării lipidelor și a stabilit că teoria scufundării lipidelor nu a fost singurul efect al emulsiei lipidice asupra anestezicelor locale.
Intoxicația cu medicamente cardiovasculare
Aaron B. Skolnik MD, Susan R. Wilcox MD, în Secretele de îngrijire critică (ediția a cincea), 2013
9 Cum funcționează terapia cu emulsie lipidică intravenoasă (ILE)?
Terapia ILE utilizează administrarea intravenoasă a unei emulsii lipidice de 20% ca antidot polivalent la otrăvirea cu medicamente lipofile. Emulsia, dezvoltată inițial pentru nutriția parenterală, poate acționa ca o „chiuvetă” în plasmă pentru medicamentele lipofile. În diferite modele de animale și rapoarte de caz umane, se pare că medicamentele sunt sechestrate în această fază lipidică și astfel sunt împiedicate să acționeze asupra unor organe țintă potențiale, cum ar fi creierul și inima. Alte mecanisme teoretice de acțiune includ furnizarea de combustibil gratuit pentru acizi grași mitocondriilor cardiace înfometate și creșterea influxului de calciu al miocitelor cardiace. Un volum mare și în creștere de date demonstrează beneficiul ILE pentru mai multe tipuri de medicamente cardiotoxice, inclusiv blocante ale canalelor de sodiu, blocante ale canalelor de calciu și unele blocante β. Luați în considerare administrarea emulsiei lipidice oricărui pacient otrăvit care a ingerat un medicament foarte solubil în lipide și are o instabilitate hemodinamică semnificativă.
Complicații hepatobiliare ale insuficienței intestinale și nutriției parenterale la domiciliu
Angelique Huijbers MD, MSc, Geert J.A. Wanten MD, PhD, MSc și sindromul intestinului scurt pentru adulți, 2019
Deficitul de vitamina E
ILE servesc în primul rând ca sursă de energie și EFA la pacienții cu insuficiență intestinală. Cu toate acestea, ILE sunt, de asemenea, cea mai importantă sursă de vitamina E (tocoferol) la pacienții dependenți de PN. Vitamina E este principalul antioxidant liposolubil și apare în mai multe izoforme, dintre care α-tocoferolul prezintă cea mai mare bioactivitate în ceea ce privește reducerea peroxidării lipidelor (Xu și colab., 2015). Având în vedere tendința unui echilibru (anti) oxidant perturbat în dependența de PN și efectul patogen al peroxidării lipidelor în dezvoltarea și/sau progresia IFALD, deficitul de vitamina E a fost sugerat ca o cauză potențială a IFALD. Cantitatea și tipurile de omologi ai vitaminei E în ILE disponibile comercial variază considerabil, datorită speciilor de ulei utilizate la fabricarea emulsiilor și, de asemenea, datorită adăugării de α-tocoferol exogen, care poate fi adăugat la ILE pentru a minimiza oxidarea FAs. (Vanek și colab., 2012; Xu și colab., 2015).
Până în prezent, aproape niciun studiu nu a evaluat efectul direct al vitaminei E în diferite ILE asupra bolilor hepatice. Un studiu a investigat impactul vitaminei E asupra incidenței IFALD la purceii hrăniți parenteral prematur (Ng și colab., 2016). Alfa-tocoferolul într-un ILE pe bază de FO și adăugarea de α-tocoferol într-un ILE pe bază de SO au împiedicat creșterea serului și a ficatului în markerii biliari și lipidemici ai IFALD, în timp ce adăugarea de fitosteroli la ILE pe bază de FO nu a produs dovezi ale IFALD, oferind unele dovezi că nivelurile scăzute de vitamina E sunt implicate în dezvoltarea IFALD. Cu toate acestea, aceste rezultate nu au fost găsite într-un studiu pe animale efectuat la purcei neonatali pe termen complet (Muto și colab., 2017).
Suport nutrițional la pacientul chirurgical pediatric
Daniel H. Teitelbaum,. Arnold G. Coran, în Chirurgie pediatrică (ediția a șaptea), 2012
Emulsii lipidice
Emulsiile lipidice intravenoase sunt o sursă condensată de energie și acizi grași esențiali, furnizând 9 kcal/g de energie. Valoarea calorică a emulsiilor lipidice variază în funcție de concentrația emulsiei lipidice. Emulsiile lipidice la concentrații de 10%, 20% și 30% produc 1,1 kcal/mL, 2 kcal/mL, respectiv 3 kcal/mL. Emulsiile lipidice intravenoase comercializate în prezent în Statele Unite sunt realizate din trigliceride cu lanț lung (LCT). Lipidele asigură de obicei 30% până la 50% din necesarul caloric fără azot sau aproximativ 20% până la 30% din totalul caloriilor. De obicei, emulsiile lipidice la sugari și copii sunt inițiate la o doză de 1 g/kg/zi și avansate cu 1 g/kg/zi până la maximum 3 g/kg/zi. Creșterea treptată a aportului zilnic de lipide (0,5 sau 1 g/kg/zi) nu pare să îmbunătățească clearance-ul lipidelor. Cu toate acestea, emulsia lipidică este mai bine eliminată 128, 129 și utilizarea lipidelor este îmbunătățită 130 atunci când lipida este perfuzată continuu timp de 24 de ore, mai degrabă decât intermitent sau o parte a zilei. Menținerea ratei de perfuzie intravenoasă a lipidelor sub 0,12 g/kg/oră îmbunătățește clearance-ul lipidelor.
Există, de asemenea, diferențe între degajările emulsiilor lipidice. Emulsia lipidică de 20% este preferată mai degrabă decât emulsia de 10% datorită clearance-ului său mai bun ca urmare a conținutului său mai scăzut de fosfolipide. 131, 132 Deoarece emulsiile lipidice sunt derivate din uleiuri vegetale, ele sunt, de asemenea, o sursă naturală de cantități variabile de izomeri de vitamina K 133 și vitamina E. 134, 135
Un sondaj anual la nivel mondial privind noile date și tendințe în reacțiile și interacțiunile adverse la medicamente
Emulsii de grăsime
Complicațiile metabolice ale nutriției parenterale la domiciliu și ale sindromului intestinului scurt
Manpreet S. Mundi MD,. Dr. Ryan T. Hurt, dr., În sindromul intestinului scurt pentru adulți, 2019
Anomalii ale profilului lipidic
Context și fiziologie
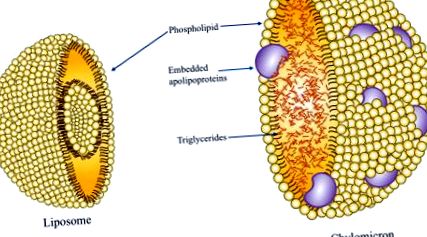
Emulsia de lipide intravenoase (ILE), în special ILE pe bază de ulei de soia (SO), poate fi asociată cu modificări ale profilului lipidic, inclusiv o scădere a lipoproteinelor cu densitate mare (HDL) și o creștere a lipoproteinelor cu densitate mică (LDL) și a trigliceridelor (TG) ) niveluri (Meguid și colab., 1989; Mundi, Salonen și Bonnes, 2016). ILE sunt compuse în mod obișnuit din TG derivate dintr-o sursă de ulei, cum ar fi SO, ulei de măsline (OO), ulei de pește (FO), trigliceride cu lanț mediu (MCT) sau o combinație de diferite uleiuri. Un emulgator fosfolipidic derivat din gălbenușul de ou servește la învelirea miezului TG și îi permite să rămână solubil în amestecul apos PN sub formă de particulă asemănătoare cu chilomicronul (Fig. 9.2) (Ferezou și Bach, 1999; Vinnars și Hammarqvist, 2004). Pentru a se asigura că diametrul mediu al particulelor de tip chilomicron nu depășește 500 nm, se adaugă un exces de emulgator (Ferezou și Bach, 1999). Excesul de emulgator există sub formă de particule bogate în fosfolipide, care sunt în esență lipozomi unilamelari (strat strat de fosfolipide care captează urme de lipide și faza apoasă).
Figura 9.2. Particulă de Chilomicron care conține fosfolipid strat cu apolipoproteine încorporate, colesterol și nucleul trigliceridelor interne. Lipozom constând din bistrat fosfolipidic.
Acești lipozomi joacă un rol semnificativ în anomaliile metabolismului lipidic. Ei dobândesc colesterol și apolipoproteine din HDL în schimbul fosfolipidelor, rezultând o reducere a nivelurilor măsurate de HDL (Ferezou și Bach, 1999). În plus, capacitatea HDL de a absorbi fosfolipidele este saturabilă, ducând la o acumulare de lipozomi în plasmă cu rate de perfuzie excesive (Breckenridge, 1985; Ferezou și Bach, 1999). Lipozomii plasmatici, dacă nu sunt metabolizați de lipoproteina lipază (LPL) și de lipaza hepatică (HL), continuă să se îmbogățească în colesterol până la atingerea unui raport 2: 1 dintre fosfolipide și colesterol. În acest moment, ele prezintă caracteristici ale lipoproteinei-X (LP-X) și, în timp, duc la hipercolesterolemie (Miyahara și colab., 1979). Nivelurile de LP-X sunt, de asemenea, dependente de proporția fosfolipidelor la TG în perfuzie. Tashiro și colab. (1992) au demonstrat că 10% emulsie este asociată cu niveluri mai ridicate de LP-X comparativ cu 20% emulsii, deoarece emulsia 10% (Intralipid) are o cantitate mai mare de lipozomi liberi și are un diametru mai mic (Garcia-de-Lorenzo și colab., 2003). Lipozomii liberi circulanți inhibă, de asemenea, acțiunea LPL și HL asupra chilomicronilor artificiali, rezultând o hidroliză slabă a TG-urilor cauzând hipertrigliceridemie (Lutz și colab., 1990).
Strategii de management
Principala strategie de management pentru anomaliile profilului lipidic asociate HPN este de a se asigura că ILE în exces nu este furnizat și că rata este adecvată pentru a permite o clearance suficientă, în special la persoanele obeze (Mundi și colab., 2016). În plus, utilizarea ILE 10% a fost redusă dramatic, 20% fiind cea mai frecventă utilizare a concentrației în prezent. ILE de 20% tinde să aibă o dimensiune mai mare a particulelor și un raport mai mic de fosfolipid la TG, rezultând un clearance mai rapid (Lutz și colab., 1989; Hailer și colab., 1998).
Utilizarea surselor alternative de TG-uri poate fi, de asemenea, explorată, având în vedere aprobarea recentă pentru ULE mixt (MO) (Smoflipid Fresenius Kabi, Bad Homburg, Germania; 30% SO, 30% MCT, 25% OO și 15% FO) în Statele Unite. Hailer și colab. (1998) au comparat utilizarea concentrației de 10% versus 20% fie a SO ILE, fie a combinației de MCT/SO ILE și au raportat că cele mai ridicate niveluri de LDL împreună cu nivelurile crescute de colesterol din grup primesc 10% SO ILE și cele mai mici niveluri de LP -X din grup primește 20% MCT/SO. O analiză retrospectivă a 38 de pacienți care au fost trecuți de la OO ILE la MO ILE din cauza hipertrigliceridemiei (≥250-400 mg/dL) a arătat că nivelurile de TG au scăzut la 94,7% dintre pacienți cu o reducere medie de 71 mg/dL (Mateu-de Antonio și Florit-Sureda, 2016). Trei studii prospective randomizate care compară MO ILE cu SO și OO/SO ILE au arătat niveluri mai mici de TG în grupul MO ILE, în timp ce trei studii suplimentare nu au găsit diferențe (Schlotzer și Kanning, 2004; Mertes și colab., 2006; Piper și colab., 2009; Tomsits și colab., 2010; Metry și colab., 2014; Wu și colab., 2014). Deși majoritatea acestor studii au limitări ale dimensiunii reduse a eșantionului, siguranța în ceea ce privește neafectarea nivelurilor de lipide este evidentă prin utilizarea emulsiilor MO ILE în comparație cu formulele convenționale.
Midazolam
Hematologic
Emulsiile de grăsime afectează coagularea și fibrinoliza [63]. La 36 de pacienți supuși unei intervenții chirurgicale de by-pass aortocoronar cu anestezie pe bază de midazolam/fentanil sau propofol/alfentanil, concentrațiile factorului XIIa și activitatea asemănătoare calikreinei au fost cu aproximativ 30% mai mari în grupul cu propofol. Autorii au sugerat că a existat o activare mai puternică a fazei de contact la începutul recirculării și o fibrinoliză mai puternică în grupul cu propofol. Ei au găsit, de asemenea, mai multă hipotensiune în grupul cu propofol, despre care au presupus că se datorează eliberării de calikreină, rezultând eliberarea de bradikinină. Nu s-a dovedit că propofolul provoacă sângerări perioperatorii crescute.
La un băiat de 40 de luni, un sindrom de sevraj cu simptome neurologice a fost însoțit de trombocitoză, care a atins un maxim de 1230 × 10 9/l [64]. Recuperarea după sindromul de sevraj a fost însoțită de normalizarea numărului de trombocite. Relevanța acestei modificări a numărului de trombocite nu a fost clară. Băiatului i s-a administrat, de asemenea, fentanil, iar autorii au sugerat că combinația midazolamului cu fentanilul ar trebui utilizată cu precauție.
Nutriție parenterală
Emulsii lipidice
Emulsiile lipidice IV, derivate în general din ulei de șofrănel, ulei de soia sau o combinație a celor două, sunt disponibile în 10% (1,1 kcal/ml), 20% (2,0 kcal/ml) și 30% (3 kcal/ml) concentrații. Concentrațiile mai mari au avantajul de a da o valoare energetică mai mare într-un volum mai mic de lichid. Ele pot fi amestecate cu dextroză și aminoacizi în 3-în-1 sau TNA într-o varietate de concentrații dacă sunt respectate anumite linii directoare. Emulsia lipidică de 30% este aprobată numai pentru compoziție, nu pentru administrare directă. Lipidele reduc osmolalitatea și, prin urmare, natura caustică a concentrațiilor ridicate de dextroză utilizate în nutriția parenterală.
În CPN, emulsiile lipidice trebuie utilizate cel puțin o dată sau de două ori pe săptămână pentru a preveni deficiențele de acizi grași esențiali (EFA). Infuzia continuă de dextroză concentrată și, în consecință, creșterea constantă a nivelurilor de insulină pot preveni mobilizarea depozitelor de țesut adipos endogen de EFA, rezultând dovezi biochimice ale unui deficit de EFA în decurs de 1 sau 2 săptămâni. Emulsiile lipidice previn acest lucru. Atunci când există o contraindicație clară pentru utilizarea emulsiilor lipidice (ceea ce este extrem de rar), o lingură de ulei vegetal, cum ar fi uleiul de șofrănel, frecat zilnic pe piele poate preveni un deficit de EFA, dar acest lucru poate să nu fie suficient pentru a corecta un deficiență preexistentă.
Aportul zilnic de lipide este obligatoriu atunci când este utilizat PPN, deoarece este practic imposibil să îndeplinești cerințele energetice cu soluțiile de glucoză mai diluate necesare în PPN. Fără calorii neproteice adecvate, aminoacizii infuzați vor fi oxidați pentru a furniza energie. Aceasta învinge unul dintre principalele scopuri ale nutriției parenterale, care este de a îndeplini toate cerințele metabolice. În plus, nutriția parenterală este mai fiziologică dacă lipidele sunt furnizate zilnic ca sursă de energie neproteică, așa cum se arată în caseta 14-2 .
La unii pacienți, includerea lipidelor ca sursă zilnică de energie este deosebit de benefică. Pacienții cu intoleranță la glucoză pot obține un control mai bun al glucozei și necesită mai puțină insulină atunci când este administrat mai puțin dextroză. Pacienții cahectici acumulează masă corporală slabă mai eficient și prezintă un risc mai scăzut de a dezvolta complicații de realimentare induse de glucoză, cum ar fi hipofosfatemia (vezi capitolul 11). Pacienții cu insuficiență ventilatorie și retenție de CO2 pot beneficia de faptul că o producție mai mică de CO2 este asociată cu oxidarea lipidelor decât cu oxidarea glucozei (vezi capitolul 24).
Emulsiile lipidice IV au foarte puține efecte adverse, iar documentarea efectelor adverse constă adesea doar în unul sau două rapoarte de cazuri individuale. Deși potențial gravă, hipersensibilitatea (raportată ca dispnee, înroșirea feței, dureri toracice, dureri de spate și urticarie) este rareori suficientă pentru a nu justifica utilizarea unor doze mici de testare înainte de perfuzia lipidică. Hipoxemia poate fi agravată prin perfuzia rapidă de lipide, dacă clearance-ul trigliceridelor circulante este întârziat. Cu toate acestea, această complicație poate fi aproape întotdeauna prevenită prin perfuzarea lipidelor timp de 12 până la 24 de ore. Nivelurile serice de trigliceride mai mari de 500 mg/dl pot provoca pancreatită, deci este prudent să se documenteze nivelurile acceptabile cel puțin o dată în timpul perfuziei lipidice.
Presupunerea obișnuită că dozele standard de emulsii lipidice (de exemplu, 500 ml de lipide 10% pe zi) cauzează sau agravează anomalii ale enzimelor hepatice sau depozitele de grăsime în ficat nu este bine întemeiată. Atunci când sunt asociate cu TPN, aceste anomalii sunt în general rezultatul livrării constante și uneori excesive de glucoză, pe care emulsiile lipidice le pot ameliora. (A se vedea „Complicații” mai târziu în acest capitol).
Lipidele ca sursă de energie pentru neonatul prematur și pe termen lung
Nutriție parenterală totală și grasă (TPN)
Emulsiile de grăsime intravenoasă au fost administrate nou-născuților de câțiva ani. Nu există nicio îndoială că unele dintre grăsimile administrate intravenos sunt utilizate ca sursă de energie, dovadă fiind modificările concentrațiilor de acizi grași liberi și corpuri cetonice 35,36 și modificări ale coeficientului respirator. 36–38 Chiar și atunci când activitatea lipoproteinelor lipazice este afectată în primele zile de viață (în special la greutatea redusă la naștere și mică la sugarii datori), creșterea corpurilor cetonice 35 indică faptul că oxidarea grăsimilor are loc în timpul nutriției parenterale totale. În prezent, se recomandă administrarea de grăsime intravenoasă la o doză de 1 până la 3 g/kg/zi, administrată continuu timp de 20 până la 24 de ore. 39 Cu toate acestea, nu se știe cât din lipida perfuzată este oxidată.
Unele studii au indicat că oxidarea grăsimilor intravenoase poate fi corelată cu aportul total de energie. Așa cum se arată în Figura 42-1, pe măsură ce aportul caloric este crescut, procentul de calorii oxidate derivate din grăsimi scade. Am investigat acest fenomen la două grupuri de sugari hrăniți cu glucoză, aminoacizi și lipide intravenos 40 (Tabelul 42-4); Grupul de studiu I a primit 102 + 12 kcal/kg/zi, iar Grupul de studiu II, 73 + 4 kcal/kg/zi ca energie neproteică. Toți sugarii au fost studiați prin calorimetrie indirectă prin intermediul unui sistem cu circuit deschis pe parcursul mai multor ore. Rezultatele acestui studiu indică faptul că, pe măsură ce aportul de energie din dietă (chiar și ca grăsime) este crescut, porțiunea de cheltuieli energetice derivate din oxidarea grăsimilor și cantitatea netă de grăsimi oxidate sunt scăzute. Aceste informații se corelează cu datele experimentale la adulți care demonstrează că o rată crescută de oxidare a glucozei este urmată de o rată scăzută de oxidare a lipidelor infuzate concomitent. 41 Când o parte importantă a aportului de energie este dată ca glucoză, este probabil ca oxidarea glucozei să afecteze utilizarea lipidelor ca combustibil în timpul TPN. Este interesant de observat că o observație similară a fost făcută la sugarii care primesc nutriție orală (vezi Tabelul 42-1).
Observația că o creștere a aportului de grăsimi nu este urmată de o rată mai mare de oxidare a grăsimilor atunci când aportul total de energie este ridicat înseamnă că este posibil să nu fie adecvată creșterea cantității de lipide intravenoase în timpul nutriției parenterale totale (cel puțin atunci când aportul de energie neproteic depășește 80-90 kcal/kg/zi). Când aportul total de energie neproteică este mai mic, este posibil ca mai multe grăsimi să fie oxidate și, prin urmare, să se furnizeze mai multă energie. Într-adevăr, Rubecz și colegii 38 au demonstrat o rată mai mare de oxidare a grăsimilor atunci când grăsimea intravenoasă a fost singura energie furnizată, iar în acest proiect experimental, 85% din grăsimea perfuzată a fost oxidată.
- Hiperinsulinemia - o prezentare generală a subiectelor ScienceDirect
- Supapă ușoară - o prezentare generală a subiectelor ScienceDirect
- Lactitol - o prezentare generală Subiecte ScienceDirect
- Lactitol - o prezentare generală Subiecte ScienceDirect
- Alimentele cu conținut scăzut de calorii - o prezentare generală Subiecte ScienceDirect