Abstract
fundal
Celulele stem mezenchimale (MSC) dețin un potențial mare ca terapie pentru accident vascular cerebral și s-a demonstrat anterior că promovează recuperarea în modele preclinice de ischemie cerebrală. MSC secretă o gamă largă de factori de creștere, chemokine, citokine și vezicule extracelulare - denumite în mod colectiv secretomul. În acest studiu, am evaluat pentru prima dată eficacitatea secretomului derivat din MSC-primat de IL-1α asupra leziunilor cerebrale și recuperării funcționale după ischemie cerebrală.
Metode
Accidentul vascular cerebral a fost indus la șoareci masculi C57BL/6 folosind modelul de filament intraluminal al ocluziei arterei cerebrale medii. Mediul condiționat din MSC-urile cu IL-1α sau vehiculul a fost administrat în momentul reperfuziei sau la 24 ore post-accident vascular cerebral prin injecție subcutanată.
Rezultate
Tratamentul mediu condiționat derivat din MSC, bazat pe IL-1α, în momentul accidentului vascular cerebral a dus la o
Reducerea cu 30% a volumului leziunii la 48 de ore și a fost asociată cu îmbunătățiri modeste ale creșterii masei corporale, scorului neurologic de 28 de puncte și construcției cuiburilor. Administrarea mediului condiționat derivat din MSC la 24 h post-accident vascular cerebral a condus la îmbunătățirea construcției cuibului și scor neurologic, în ciuda diferențelor observate în volumul leziunii în ziua 2 post-accident vascular cerebral.
Concluzii
Rezultatele noastre arată pentru prima dată că administrarea mediului condiționat din MSC-urile cu IL-1α conduce la îmbunătățiri ale rezultatelor comportamentale independent de neuroprotecție.
fundal
Accidentul vascular cerebral este o problemă de sănătate globală semnificativă care duce la aproximativ 6,7 milioane de decese anual [1]. Pentru cele 33 de milioane de persoane care trăiesc cu accident vascular cerebral, opțiunile de tratament sunt foarte limitate și nu ameliorează pe deplin dizabilitatea cauzată [2]. Prin urmare, există o cerere mare de terapii regenerative pentru a promova repararea și îmbunătățirea dizabilității după accident vascular cerebral ischemic.
O serie de strategii de precondiționare in vitro au fost explorate pentru a spori secretomul MSC, inclusiv cultura 3D [15] și precondiționarea hipoxică [16]. În lucrările noastre anterioare, am demonstrat în mod clar că amorsarea cu interleukina-1 alfa (IL-1α) conduce secretomul MSC către un fenotip mai antiinflamator și pro-trofic care se poate traduce într-o terapie mai bună pentru accidentul vascular cerebral ischemic [17]. În prezent, efectul unor astfel de strategii de precondiționare MSC nu a fost studiat pe larg în modele preclinice de accident vascular cerebral. Într-adevăr, din câte știm, există doar un astfel de studiu, care a evaluat eficacitatea CM derivată din MSC precondiționate hipoxie [13] asupra recuperării motorului și neuroprotecției într-un model de șobolan ischemic. Datele noastre in vitro publicate anterior demonstrează în mod clar că amorsarea IL-1α conduce MSC către un fenotip pro-reparator. Prin urmare, este esențial să se confirme beneficiul amorsării IL-1α într-o paradigmă in vivo relevantă, cu o caracterizare extinsă a repertoriului comportamental post-accident vascular cerebral, așa cum a fost investigat aici într-un model de șoarece de ocluzie a arterei cerebrale medii.
Metode
Caracterizarea MSC
Pentru caracterizare, MSC au fost colorate folosind kitul de analiză BD Stemflow ™ hMSC (BD Biosciences, Marea Britanie) conform instrucțiunilor producătorului. Celulele au fost apoi analizate pe un citometru cu flux invers (BD Biosciences, UK) pentru expresia pozitivă a markerilor de suprafață CD73, CD90 și CD105 și expresia negativă a CD11b, CD19, CD34, CD45 și HLA-DR, așa cum este definit de Societatea Internațională pentru Celulare Terapia ca criteriu minim pentru MSC [18] (Fișier suplimentar 1: Figura S1). Porțile pozitive au fost setate folosind fluorescența minus unu controale. Multipotența MSC a fost, de asemenea, evaluată utilizând un kit disponibil comercial (R&D Systems, UK). Pe scurt, MSC-urile au fost cultivate timp de 21 de zile în medii de diferențiere, cu schimbări de suport la fiecare 2-3 zile. Adipocitele au fost colorate cu Oil Red O (Millipore, UK), iar osteocitele au fost colorate cu Alizarin Red (Millipore, UK). Peletele de chondocite au fost tăiate în secțiuni de 30 μm folosind un microtom de săniuș înghețat (Bright Instruments, UK) apoi colorate cu albastru de toluidină (Sigma-Aldrich, UK). Imaginile au fost achiziționate folosind un microscop inversat (Olympus CK X31) și o cameră Moticam 2300 conectată la software-ul Motic Images Plus 2.0 ML (Motic, Hong Kong).
Cultură de celule stem mezenchimale
Pasajul 5-6 MSC derivate din măduva osoasă umană de la un donator fetal în vârstă de 22 de săptămâni (3H Biomedical, Suedia) au fost utilizate pentru toate experimentele. MSC au fost cultivate ca monostrat în baloane de cultură tisulară (Corning, Marea Britanie) în mediul MesenPRO RS (Invitrogen, Marea Britanie) suplimentat cu 1% penicilină/streptomicină și 2 mM glutamină. Mediul de creștere a fost schimbat la fiecare 4-5 zile până când celulele au fost 70-80% confluente. MSC-urile au fost apoi disociate cu 0,5% tripsină-EDTA (Sigma-Aldrich, Marea Britanie) și numărate. Pentru prepararea CM-α-primed CM (αCM), MSC au fost însămânțate în plăci cu 6 godeuri (Corning, Marea Britanie) la o densitate de 1,75 × 105 celule/godeu și incubate timp de 24 de ore. MSC-urile au fost apoi tratate cu 10 ng/ml IL-1α recombinant uman (R&D Systems, UK) timp de 5 minute. Celulele au fost spălate de două ori cu PBS, apoi s-a adăugat mediu MesenPRO RS fără ser (fără supliment). După 24 de ore, s-a colectat αCM, resturile celulare au fost îndepărtate folosind filtre de seringă de 0,22-μM (Millipore, Marea Britanie) și 10 × concentrate folosind concentratoare centrifuge Vivaspin de 3000 MWCO (Generon, Marea Britanie) conform instrucțiunilor producătorului. Pentru vehicul, mediul MesenPRO RS fără ser a fost, de asemenea, concentrat de 10 ×. Pentru toate experimentele in vivo, tratamentele condiționate de 400 μl derivate din 3,5 × 105 celule au fost preparate în avans și depozitate la - 80 ° C.
Experimente in vivo
Animale
Toate procedurile pentru animale au fost efectuate în conformitate cu legea revizuită privind animalele (procedurile științifice) din 1986, sub licența de proiect a Home Office (Marea Britanie) și aprobate de Comitetul local de revizuire etică pentru bunăstarea animalelor. Animalele au fost adăpostite în grup în Sealsafe Plus Mouse cuști ventilate individual (Techniplast, Italia) la 21 ± 1 ° C, 55 ± 10% umiditate pe un ciclu de 12 ore lumină-întuneric. Toate cuștile au fost furnizate cu material de cuibărit Sizzle Nest (Datesand Ltd., UK) și tuburi de îmbogățire a cartonului (Datesand Ltd., UK). Șoarecii au avut acces ad libitum la dieta standard a rozătoarelor (SDS, UK) și la apă. Șoarecii au fost aclimatizați la instalație timp de cel puțin o săptămână înainte de începerea lucrărilor experimentale.
Ocluzia arterei cerebrale medii (MCAO)
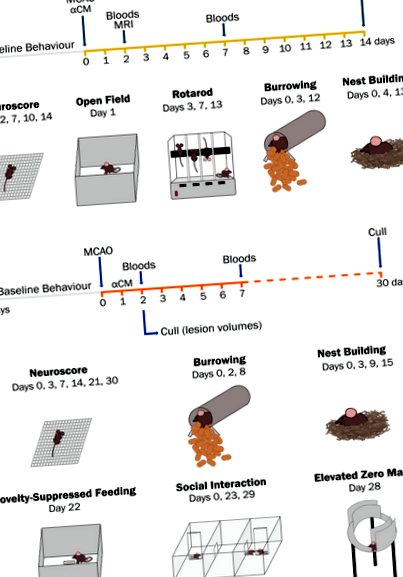
Rezumatul cronologiei studiului accidentului vascular cerebral și testelor comportamentale. În primul studiu, un mediu condiționat din celule stem mezenchimale primite cu IL-1α (αCM) a fost administrat în momentul reperfuziei prin injecție subcutanată, apoi șoarecii au fost recuperați timp de 14 zile (A). În cel de-al doilea studiu, un mediu condiționat a fost administrat 24 de ore după accident vascular cerebral (b). Șoarecii au fost apoi recuperați timp de 30 de zile pentru a facilita evaluarea anxietății post-accident vascular cerebral și a comportamentelor depresive la sfârșitul timpului. Cu excepția câmpului deschis, hrănirea suprimată de noutate și evaluările comportamentale de bază ale labirintului zero au fost efectuate înainte de operația de accident vascular cerebral
Un tratament de 400 μl 10 × αCM concentrat sau MesenPRO (vehicul) a fost administrat prin injecție subcutanată în momentul reperfuziei în studiul 1 și la 24 de ore după MCAO în studiul 2. Animalele au fost excluse din studii dacă ocluzia nu a avut succes (definit ca 0.
Fără manipulare a materialului de cuibărit
Nu există un loc evident de cuib (majoritatea materialului de cuibărit nu este conținut într-un cadran al cuștii)
Cuib prezent dar plat
Cuibul are pereți ridicați ≤ 30 mm înălțime
Pereții cuibului cu înălțimea de 31–49 mm
Pereții cuibului ≥ 50 mm înălțime
Fotografiile au fost făcute pe o cameră smartphone (Xiaomi, China). Fiecare cadran al cuiburilor a fost marcat de un observator orbit de grup și punct de timp, apoi mediat. Orbirea a fost efectuată cerând unui cercetător independent să redenumească fișierul.
Labirint zero ridicat
Aparatul cu labirint zero ridicat (San Diego Instruments, SUA) consta dintr-o pistă inelară din plastic de 600 mm diametru, ridicată la 600 mm deasupra podelei. Acesta este împărțit în patru cadrane: două brațe închise cu pereți de 15 mm și două brațe deschise. Șoarecii au fost introduși într-unul dintre brațele închise și li s-a permis explorarea timp de 5 minute. Software-ul ORICE labirint a fost folosit din nou pentru urmărirea live.
Hrănirea suprimată prin noutate
Hrănirea suprimată cu noutăți este utilizată pe scară largă pentru a evalua anxietatea și a examina noile antidepresive [25]. Acest test măsoară hiponeofagia, inhibarea hrănirii ca răspuns la un mediu nou. Aparatul consta dintr-o arenă pătrată de Perspex (450 × 200 × 450 mm) cu o farfurie de cultură de 35 mm (Corning, Marea Britanie) conținând 1 g lapte condensat îndulcit (Aldi, Germania) în centru. Șoarecii au fost introduși într-un colț și au fost lăsați să exploreze timp de 5 minute. O cameră digitală USB 2.0 CMOS (Stoelting, SUA) poziționată direct deasupra aparatului conectat la un laptop cu ORICE labirint versiunea 6.0 (Stoelting, SUA) a fost utilizată pentru înregistrarea video și urmărirea live. Latența de abordare a alimentelor a fost temporizată manual din videoclipuri de către un observator orbit de momentul și grupul de tratament. Vasul a fost cântărit după testare pentru a calcula masa alimentelor consumate.
Test de interacțiune socială și preferință socială
Imagistică prin rezonanță magnetică
La 48 de ore după accident vascular cerebral, animalele din studiul 1 au fost anesteziate cu 4% izofluran și scanări ponderate T2 au fost efectuate pe consola Bruker Advance III (Bruker Biospin Ltd., Marea Britanie) folosind un magnet 7-T. Au fost achiziționate un total de 14 felii în serie cu o grosime de 1 mm. Volumele leziunilor au fost măsurate folosind ImageJ și corectate din edem.
Cuantificarea volumului leziunii
La 48 de ore, o sub-cohortă de animale din studiul 2 a fost perfuzată intracardic cu soluție salină 0,9% urmată de 4% paraformaldehidă (PFA), în tampon fosfat 0,1 M (PB). Creierele au fost îndepărtate și post-fixate în 4% PFA timp de 24 de ore, apoi transferate la 30% zaharoză înainte de a fi congelate rapid în izopentan. Secțiunile au fost tăiate la o grosime de 30 μm folosind un microtom de sanie de îngheț și montate pe lamele acoperite cu gelatină. Secțiunile au fost apoi colorate cu violet crezil și acoperite cu suport de montare DPX (Sigma-Aldrich, Marea Britanie). Volumul leziunii a fost apoi măsurat folosind ImageJ și corectat pentru edem.
Imunohistochimie
Pentru imunofluorescență, după recuperarea antigenului, așa cum au fost incubate lamele de mai sus, în Ki67 primar (1: 200, BD550609) și NeuN (1: 1000, ab177487) la 4 ° C peste noapte. Diapozitivele au fost apoi incubate în anti-șoarece biotinilat (1: 500, Vector Laboratories, Marea Britanie) și Alexa Fluor ™ 647 anti-iepure (1: 500) timp de 1 oră 30. Pentru a amplifica un kit super boost de tiramidă (B40933) Semnal Ki67 conform protocolului producătorului. Secțiunile au fost contracolorate folosind DAPI (1 μg mL -1, 10 min, D9542) și montate folosind ProLong® Gold Antifade Mountant (Thermo Fisher, Marea Britanie). Imaginile au fost colectate pe un microscop vertical Zeiss Axioimager.D2 folosind un obiectiv Apochromat × 20/0,8 și capturate folosind o cameră Coolsnap HQ2 (Photometrics) prin intermediul software-ului Micromanager v1.4.23. Imaginile au fost apoi procesate și analizate folosind ImageJ de către un experimentator orbit de grupul de tratament.
Analiza datelor și statisticilor
Toate datele sunt exprimate ca medie ± deviație standard (SD). Pentru studiile de accident vascular cerebral, s-a efectuat un calcul al puterii măsurii principale a performanței în sarcina comportamentului vizuinării cu date dobândite anterior folosind un calculator online (https://jackauty.com/power-calculator/). Folosind o medie de 81,2, un SD de 25,9, un alfa de 0,05 și o putere de 0,8, un n din 8 a fost calculat pentru a detecta o îmbunătățire cu 60%. Contabilizarea unei rate de uzură de 30%, an n din 12 a fost ales. Analiza statistică a fost efectuată în RStudio Versiunea 1.1.463 (https://www.rstudio.com) folosind pachetele auto, lme4 și lsmeans. Ipotezele au fost evaluate grafic și, dacă este necesar, datele au fost transformate. Modelarea pe mai multe niveluri a fost utilizată pentru a analiza masa corporală, vizuinarea și datele rotarodului. Dacă s-a obținut semnificația statistică (p
Rezultate
Tratamentul mediu condiționat în momentul accidentului vascular cerebral are un efect neuroprotector și favorizează îmbunătățirea măsurilor de bunăstare
În studiul 1, doi șoareci din grupul AVC + αCM au fost excluși din cauza hemoragiei subarahnoidiene și unul a depășit punctul final uman de> 20% pierdere de masă corporală și a fost sacrificat devreme. În grupul accident vascular cerebral + vehicul, un șoarece a fost sacrificat devreme din cauza pierderii în greutate și doi au fost excluși din cauza Fig. 2
În ziua 14, MCAO a fost asociată cu o expresie crescută a markerului microglial Iba1 atât în cortexul ipsilateral, cât și în striat (p FIG. 3
În ziua 30, MCAO a fost asociată cu creșterea expresiei microgliene Iba1 atât în cortexul ipsilateral, cât și în striat (p FIG. 4
Performanța în testele de anxietate și comportamente depresive la sfârșitul momentelor post-accident vascular cerebral. Latența de a mânca alimente (A) și masa alimentelor consumate (b) în sarcina de hrănire suprimată de noutate în ziua 22 post-accident vascular cerebral. Timpul petrecut în brațe deschise (c) și distanța totală parcursă în labirintul zero ridicat în ziua 28 (d). Datele au fost exprimate ca medie ± SD. Sham + vehicul, n = 12; sham + αCM, n = 11; accident vascular cerebral + vehicul, n = 8; accident vascular cerebral + αCM, n = 9
Discuţie
În acest studiu, oferim o investigație detaliată in vivo a eficacității precondiționării ca strategie de îmbunătățire a potențialului terapeutic al CSM. Mai precis, am demonstrat pentru prima dată că administrarea subcutanată de CM derivată de MSC (αCM) derivată de MSC în momentul reperfuziei a avut un efect neuroprotector semnificativ și a oferit îmbunătățiri modeste în măsurile de bunăstare într-un model de șoarece de ischemie cerebrală focală. Am arătat apoi că întârzierea administrării αCM la 24 h post-accident vascular cerebral a dus la o recuperare funcțională îmbunătățită, evidențiată de scorurile crescute de construcție a cuibului în ziua 9 și îmbunătățirea semnificativă a scorurilor neurologice începând cu ziua 7 încoace, independent de neuroprotecție. În ansamblu, lucrarea noastră indică faptul că secretomul MSC primat de IL-1 ar putea fi o terapie celulară utilă nouă pentru accident vascular cerebral.
Aici, am raportat că MCAO a indus comportamente asemănătoare anxietății din ziua 22 după accident vascular cerebral. Acest lucru este în sprijinul unui studiu anterior care a arătat o latență crescută de a mânca în testul de hrănire suprimat de noutate la 14 săptămâni după accident vascular cerebral într-un model MCAO de șoarece și la 19 zile după leziunea cortexului prefrontal indusă de endotelină [45]. În timp ce am raportat creșterea timpului petrecut în brațul deschis al labirintului zero ridicat, spre deosebire de ceea ce a fost raportat anterior [45,46,47], acest lucru s-ar putea datora hiperactivității. Hiperactivitatea a fost observată până la 8 săptămâni după MCAO la șoareci [48].
Concluzii
În rezumat, rezultatele noastre demonstrează pentru prima dată că administrarea sistemică a CM din MSC-urile cu IL-1α promovează îmbunătățirea recuperării într-un model de șoarece de ischemie cerebrală, independent de neuroprotecție. În timp ce există multe cercetări care trebuie să elucideze pe deplin mecanismele de acțiune și să definească care sunt mediatorii esențiali în promovarea reparării, secretomul MSC-primat cu IL-1 deține un potențial mare ca terapie celulară pentru tratamentul accidentului vascular cerebral ischemic.
- Tratamentul obezității folosind celule stem este subiectul celui mai vizitat comunicat de presă din 2013 pe EurekAlert!
- Celulele stem sunt mai sănătoase cu pierderea în greutate
- Celule stem și pierderea în greutate Denver Colorado Pierdere în greutate
- Revizuirea pacientului despre tratamentul celulelor stem pentru SM în clinica din Moscova Swiss Medica
- Revizuirea tratamentului nechirurgical și chirurgical și a rolului agenților sensibilizatori la insulină în