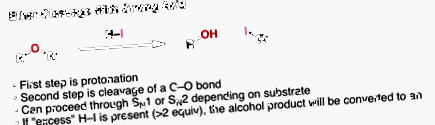Ultima actualizare: 24 iunie 2020 |
Scindarea acidă a eterilor se poate desfășura printr-un mecanism SN2 sau SN1, în funcție de structură
Aștept cu nerăbdare postul de astăzi de multă vreme! Am trecut prin atât de multe moduri diferite de sintetizare a eterilor și, în cele din urmă, vom vorbi despre toate lucrurile interesante pe care le putem face cu ei.
Cuprins
1. Toate reacțiile eterilor într-un singur loc (har!)
Iată-l, momentul pe care l-ai așteptat. Toate reacțiile eterilor într-un singur loc:
Am acoperit acum reacțiile eterilor.
Vă mulțumim pentru atenție.
Asta este? Da într-adevăr: singura reacție semnificativă a eterilor pe care trebuie să o cunoașteți ... este cum să le spargi.
[Tocmai îți trageam piciorul în legătură cu linia „lucruri interesante pe care le facem cu eterii”.]
Face acest lucru eterii cel mai plictisitor grup funcțional existent? Da. (atâta timp cât nu numerați alcani ca „grup funcțional”).
Așadar, s-ar putea să întrebați - ce rost are?
Tot ce voi spune deocamdată este că există anumite momente în care „plictisitorul este bun”. Eterii, așa cum vom învăța mai târziu, pot fi utili ca „grupuri de protecție” pentru mascarea alcoolilor (reactivi). Dar aceasta este o discuție ulterioară. [A se vedea: Protejarea grupurilor pentru alcooli]
Chiar acum, să analizăm cum funcționează această reacție de decupare a eterului, deoarece are de fapt subtilitățile sale. Această discuție ar trebui să fie destul de simplă dacă ați urmărit, totuși, pentru că va implica doar mecanismele familiare de protonație, SN1 și SN2.
2. Primul pas în clivajul acid al eterilor este protonarea oxigenului
Eterii neutri sunt, în general, rezistenți la nucleofili în reacțiile de substituție - asta pentru că grupul părăsit ar trebui să fie RO-, care este o bază foarte puternică.
Din acest motiv, primul pas în orice clivaj eteric este protonarea cu un acid puternic. De ce ne ajută protonația? Amintiți-vă că „acidul conjugat este întotdeauna un grup mai bun de părăsire”. Protonarea eterului permite pierderea ROH ca grup părăsit, care este o bază mult mai slabă decât RO-. Aceasta va stabili următorul nostru pas - clivajul uneia dintre legăturile C-O.
Acidul puternic obișnuit la alegere este de obicei acidul iodiodic (HI). Nu numai că este puternic (pKa de –10), deoarece vom vedea că și ionul contra-ionic joacă un rol.
3. Pentru metil și eteri primari, al doilea pas al clivajului eteric este SN2
După protonare, ce se întâmplă în continuare? Dacă începem cu un eter primar, cum ar fi dietil eterul, vom avea un grup bun de părăsire (ROH) pe un carbon primar în prezența unui nucleofil decent (ion iodură). Suna familiar? Ar trebui - acestea sunt condiții ideale pentru o reacție SN2. Și asta se întâmplă.
Produsul va fi ROH și R-I .
Dacă este prezent un exces (2 echiv sau mai mult) de HI, acel alcool poate fi transformat într-o iodură de alchil prin două etape ulterioare (protonație/SN2).
Această cale „SN2” va fi dominantă pentru eterii primari și metilici.
4. Pentru eterii terțiari, al doilea pas al clivajului eteric este SN1
Dar un eter terțiar simetric ca eterul di-t-butilic?
În mod clar, SN2 nu este în joc aici, deoarece carbonii terțiari sunt mult prea împiedicați pentru un atac din spate. Cu toate acestea, carbocațiile terțiare sunt relativ stabile - iar „ionizarea” (adică pierderea unui grup părăsit) ne lasă cu un alcool (R-OH) și o carbocație terțiară, care poate fi apoi atacată de ionul iodură pentru a da R-I
Din nou, dacă excesul de HI este prezent, alcoolul respectiv va fi transformat într-o halogenură de alchil. Vom avea mai multe despre asta de spus în câteva postări.
5. Pentru eteri secundari, al doilea pas ar putea continua printr-un amestec de oricare cale
Dar cu eterii secundari? Nu am un răspuns bun. SN1 și SN2 sunt un continuum. Veți avea probabil un amestec de căi SN2 și SN1 care funcționează. Dacă cineva îți spune că poate privi un eter precum di-izopropil eterul și căile SN2 sau SN1 vor fi 100% dominante, nu este adevărat.
6. Mecanismul pentru scindarea eterilor nesimetrici este greu de generalizat (cu o singură excepție!)
La fel de complicat precum cazul eterilor secundari este cazul eterilor „amestecați”. Ce se întâmplă dacă aveți două grupuri diferite atașate oxigenului („eteri nesimetrici”). Pe ce cale se va sparge?
De exemplu, ce zici de t-butil metil eter? Când îl tratați cu acid, ce se întâmplă mai întâi? Faceți un SN2 pe gruparea metil cu iodură sau ionizează pentru a da o carbocație terțiară?
Acesta este tipul de întrebare care NU este ușor de răspuns fără a cunoaște rezultatele experimentelor.
Există, totuși, câteva cazuri de eteri mixți în care există un răspuns direct.
Luați această întrebare de exemplu. Ce se întâmplă? Răspunsul este foarte clar și merge 100% într-o direcție. Vezi dacă o poți face.
Dacă sunteți curios cu privire la răspuns, va trebui să lăsați un comentariu.
7. Rezumat: Scindarea acidă a eterilor
O.K. Așadar, eterii, așa cum am vorbit despre ei până acum, sunt destul de plictisitori. Dar (și există întotdeauna un dar) - Există o clasă specială de eteri care este, de fapt, foarte interesantă și foarte reactivă. Dacă ați acoperit alchenele, le-ați mai văzut - dar sub un alt nume. Puteți ghici despre ce grup funcțional vorbesc? Următorul post!
- Determinarea coulometrică a conținutului de acid organic liber în fructele de trandafir sălbatic SpringerLink
- Acid glicolic și alți acizi - Irina Organic Skin Care
- Hidrură de dimagnesiu fier (II), Mg2FeH6, conținând anioni octaedric FeH64- Chimie anorganică
- Comparaţie; Top 7; Seruri de acid hialuronic Recenzii
- Rețetă DIY Detox Body Wrap pentru autoritatea organică a pielii de vară radiantă