Yin-cântec Jiang
1 Departamentul de Medicină de Urgență, Spitalul Afiliat al Universității Shihezi, Shihezi 832002, China
Yu-ying Ma
1 Departamentul de Medicină de Urgență, Spitalul Afiliat al Universității Shihezi, Shihezi 832002, China
Zhan-qing Wang
1 Departamentul de Medicină de Urgență, Spitalul Afiliat al Universității Shihezi, Shihezi 832002, China
Guang-jun Li
2 Luo Zhuang People’s Hospital, Lin Yi 276016, China
Abstract
FUNDAL:
Concentrația plasmatică a paraquatului este strâns legată de prognosticul pacienților cu otrăvire cu paraquat, iar cea mai frecventă cauză de deces prin intoxicație cu paraquat este insuficiența multiplă a organelor (MOF). Acest studiu a avut ca scop evaluarea efectului terapeutic al smecta asupra concentrațiilor plasmatice de paraquat și leziuni multi-organe induse de intoxicația cu paraquat la șobolani.
METODE:
Un total de 76 de șobolani SD sănătoși adulți au fost împărțiți în mod aleatoriu în grupul A (grupul martor, n = 6), grupul B (grup otrăvit, n = 30) și grupul C (grup tratat cu smecta, n = 30). Șobolanii din grupele B și C au fost tratați intragastric cu PQ la 50 mg/kg, iar șobolanii din grupa A au fost tratați intragastric cu soluție salină (1 ml). Șobolanilor din grupul C li s-a administrat smecta intragastric la 400 mg/kg la 10 minute după administrarea PQ, în timp ce șobolanii din alte două grupuri au fost tratați intragastric cu 1 ml soluție salină în același timp. Șobolanii vii din grupele B și C au fost sacrificați la 2, 6, 24, 48, 72 de ore după administrarea PQ pentru determinarea concentrațiilor plasmatice de paraquat și pentru colorarea HE a plămânului, stomacului și jejunului. Șobolanii au fost executați la sfârșitul procesului în același mod în grupa A.
REZULTATE:
Concentrația plasmatică de paraquat (ng/ml) a variat de la 440,314 ± 49,776 la 4320,6150 ± 413,947. S-au observat modificări patologice distincte la nivelul plămânului, stomacului și jejunului din grupul B. Leziunile pulmonare s-au deteriorat treptat, s-au observat edeme, infiltrare leucocitară, pneumoragie, septuri incasate și consolidare pulmonară. Abruptul mucoasei, mucoasei gastrice hiperemice și infiltrarea leucocitelor au fost evidente în stomac. S-au constatat hemoragia mucoasei jejunului, ruperea vilozității, afectarea glandei cu adăugarea infiltrării celulare inflamatorii. Comparativ cu grupul B, concentrația plasmatică de paraquat a scăzut (P CUVINTE CHEIE: Smecta, Paraquat, Schimbare patologică, Traumatism terapeutic
INTRODUCERE
Paraquat (PQ) este un erbicid de contact neselectiv și a fost utilizat pe scară largă în lume, în special în țările în curs de dezvoltare încă din anii 1960. Cu toate acestea, otrăvirea PQ rămâne o cauză majoră de deces în rândul pacienților cu otrăvire acută în Asia [1], iar mortalitatea sa este de până la 80%. [2] PQ este absorbit în principal prin tractul intestinal, nivelul său plasmatic a atins un maxim în 4 ore după administrarea orală. PQ se acumulează extensiv în întregul corp, dar este stocat în principal în plămâni și stomac unde este reținut chiar și concentrația sanguină scade, în cele din urmă fiind excretată de rinichi. [3]
O mulțime de experimente pe animale și studii clinice au dovedit că toxicitatea PQ duce de obicei la leziuni multiorganice. [4-6] Datorită sistemului de absorbție a poliaminei, concentrația pulmonară a PQ este de 6-10 ori mai mare decât cea din plasmă, deci plămânul este organul țintă al otrăvirii PQ. Faza acută, în care leziunea pulmonară este caracterizată de alveolită pulmonară, este urmată de faza proliferativă definită de apariția fibrozei progresive. [7] Kim și colab. [8] au raportat că schimbarea distinctă a fibrozei pulmonare în tomografia computerizată de înaltă rezoluție (HRCT) a fost caracterizată prin opacități de sticlă măcinată (GGO) și acest lucru a sugerat că zona GGO-urilor este un predictor util de supraviețuire Intoxicația PQ, în special la pacienții cu un nivel scăzut al PQ plasmatic. În ceea ce privește simptomele de otrăvire, tractul digestiv a apărut cel mai repede, cum ar fi durerea de stomac, vărsăturile și hemoragia tractului digestiv. Disfuncția gastro-intestinală poate accelera absorbția otrăvii sau poate întârzia excreția otrăvirii, de aceea este necesar ca medicii să ia măsuri eficiente pentru a reduce leziunile gastro-intestinale rezultate din PQ. Cu toate acestea, există puține studii privind protecția structurii gastro-intestinale.
Până în prezent, tratamentul intoxicației cu PQ este încă în stadiul explorator. O serie de metode terapeutice pentru tratamentul intoxicației cu PQ au demonstrat o eficacitate slabă [9, 10] și doar câteva tratamente au evidențiat eficacitatea. [11-13] Studiile [14-16] se concentrează în principal pe spălarea gastrică, purificarea sângelui, glucocorticoidul și ciclofosfamidă, dar există diferite opinii cu privire la aceste metode. S-a raportat că, pentru a preveni absorbția PQ de către tractul gastro-intestinal, pacienților li s-a administrat cărbune activ în 250 ml citrat de magneziu printr-un tub nazogastric, [14] sugerând că adsorbantul superactiv este benefic pentru reducerea concentrației de sânge.
Smecta sau pulbere de smectită, un fel de aluminosilicat natural format dintr-un silicat dublu de aluminiu și magneziu, este alcătuită în principal din particule de montmorillonit octogonale care prezintă structura stratului și distribuția sarcinii de eterogenitate. Una dintre cele mai remarcabile caracteristici farmacologice ale smecta este activitatea sa puternică de adsorbție. [17] Nu numai că adsorbe de opt ori greutatea sa proprie, dar și adsorbe toxine, bacterii și rotavirus, împiedicând factorii de virulență să adere la membranele intestinale. [18-20] În plus, cu capacitatea de a acoperi mucoasa și de a se combina cu glicoproteină mucoasă, smecta întărește bariera mucoasă. [21] Mai mult, smecta nu va trece în circulația sângelui după asocierea cu substanțe morbide și abia scade dinamica intestinală, [22] provocând câteva efecte secundare. Ca adsorbant, smecta a fost utilizat pe scară largă pentru tratarea diferitelor boli, [23-25], inclusiv diaree, sângerări gastro-intestinale și ulcer peptic. Un studiu recent [22] a arătat că smecta la 6 g tid a fost bine tolerată și a redus timpul până la recuperare după un episod acut de diaree apoasă. Chiar dacă eficacitatea Smecta în tratamentul bolilor sistemului digestiv a fost confirmată, studiul privind utilizarea smecta în otrăvirea PQ este rar.
Astfel, acest studiu a urmărit să mărturisească dacă smecta poate reduce concentrația plasmatică determinată de cromatografie lichidă de înaltă performanță (HPLC) [26,27] și de a îmbunătăți deteriorarea patologică a șobolanilor cu intoxicație cu PQ.
METODE
Produse chimice și instrumente
Diclorura de paraquat (HPLC) 99,9% din suprafață, 0,1 g, a fost achiziționată de la Sigma-Aldrich, SUA. Acetonitril (cromatografic pur), alcool metilic (cromatografic pur), trietilamină (analitic pur) și acid tofosforic (analitic pur) au fost achiziționate de la Tianjin Guangfu Reagent Co., Ltd, China. 1-heptanesulfonat de sodiu (puritate analitică pură ≥98%, 20 g) a fost produs de BBI, Canada. Smecta a fost produs de Beauour Ipsen (Tianjin) Pharmaceutical Co., Ltd. Eclipse plus Coloana cromatografică (4,6 × 250 mm, 5 µm) a fost achiziționată de la Agilent, SUA. Cromatograf lichid de înaltă performanță LC-20A, pompă LC-20AT, controler CBM-20A, detector SPD-M20A, autosamplator SIL-20A, cuptor CTO-10AS VP pe coloană au fost cumpărate de la Shimadzu, Japonia.
Animale
Acest studiu a fost realizat folosind șobolani SD masculi adulți (200 ± 20 g) obținuți de la Centrul de Prevenire și Control al Bolii Xinjiang. Șobolanii au fost ținuți în condiții standard de laborator (12/12 h lumină/întuneric, 22 ± 2 ° C temperatura camerei, 50% –60% umiditate) timp de cel puțin 1 săptămână înainte de începerea experimentului. Șobolanilor li s-a permis accesul liber la apa de la robinet și la șobolanii ad libitum în timpul experimentului.
Protocol experimental
Un total de 66 de șobolani SD sănătoși adulți au fost împărțiți în mod aleatoriu în grupul A (grupul martor, n = 6), grupul B (grup otrăvit, n = 30) și grupul C (grup tratat cu smecta, n = 30). Șobolanii din grupele B și C au fost tratați intragastric cu o singură doză de PQ (PQ, 50 mg/kg), iar cei din grupul A au fost tratați intragastric cu 1 ml de soluție salină. Șobolanilor din grupul C li s-a administrat smecta intragastric la 400 mg/kg la 10 minute după administrarea PQ, în timp ce șobolanii din celelalte două grupuri au fost tratați intragastric cu 1 ml de soluție salină în același timp. Șobolanii din grupele B și C au fost sacrificați la 2, 6, 24, 48, 72 de ore după administrarea PQ, respectiv. Șobolanii au fost sacrificați, iar probele lor de sânge au fost prelevate. Serul șobolanilor a fost separat imediat și depozitat la –72 ° C pentru determinarea concentrațiilor plasmatice de PQ. Țesuturile plămânului, stomacului și jejunului au fost luate pentru colorare HE și examen patologic. [28-30] Șobolanii din grupa A au fost executați în mod similar.
Determinarea concentrației plasmatice a PQ
Concentrația PQ a fost determinată cu metodele raportate [26,27] cu modificări minore. Probele de plasmă au fost trimise la Shihezi University College of Pharmacy pentru analize cantitative utilizând HPLC. Pe scurt, s-a adăugat 35% acid percloric (100 pl) într-o eprubetă care conține supernatant plasmatic (0,5 ml), iar lichiorul amestecat de acid percloric și supernatant plasmatic a fost centrifugat și supernatantul lichiorului amestecat a fost analizat prin HPLC. Au fost preparate șase probe de plasmă martor martor (concentrațiile probelor au fost de 20, 50, 100, 500, 1.000, 5.000 ng/ml, respectiv), apoi a fost detectată zona de vârf a acestor probe. Ecuația de regresie a probelor de plasmă PQ, care a fost utilizată pentru a calcula concentrația PQ, poate fi obținută în funcție de aria de vârf (Y) și concentrația (X).
analize statistice
Analiza statistică a fost făcută utilizând SPSS 13.0. Toate datele au fost exprimate ca medii ± deviație standard. Ratele de supraviețuire ale șobolanilor au fost comparate utilizând testul exact al lui Fisher pentru variabile categorice neordonate, scorurile patologice au fost comparate cu testele independente ale testelor t și concentrațiile PQ au fost comparate utilizând analiza varianței (ANOVA) urmată de testul de comparație multiplă LSD. O valoare P mai mică de 0,05 a fost considerată semnificativă statistic.
REZULTATE
Modificări comportamentale ale șobolanilor
La două ore după otrăvirea PQ, simptome, inclusiv respirație rapidă superficială, dispnee, pierderea poftei de mâncare, piloerecție și hemoragie în nară și angulus oris, au fost observate la șobolani din grupul B, comparativ cu șobolanii normali. După ce cavitatea toracică și cavitatea abdominală a șobolanilor din grupa B au fost deschise, s-au observat edem pulmonar, congestie pulmonară, distensie gastrică, timpani intestinali și obstrucție intestinală. Aceste simptome au fost mai puțin marcate în grupul C. La șaptezeci și două de ore după tratament, rata de supraviețuire a șobolanilor din grupul de control a fost de 100%, în timp ce a fost de 90% în grupul B și, respectiv, de 97% în grupul C. Nu au existat modificări în grupa A.
Corelația liniară și concentrația paraquatului
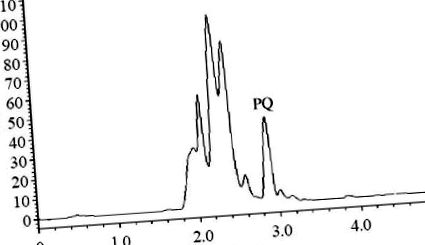
Ecuația de regresie a plasmei PQ: Y = 98,8210 X +5707,5407. Concentrația PQ a variat de la 20 ng/mL la 5000 ng/mL, iar limita minimă de detecție a fost de 20 ng/mL. Cromatogramele HPLC parțiale sunt prezentate în figurile din figurile 1 1 - 3 .
Cromatogramă HPLC a probei de plasmă martor martor în grupul martor (concentrație PQ, 1000 ng/ml).
Cromatogramă HPLC a probei de plasmă din grupa C (2 ore după administrarea PQ).
Cromatogramă HPLC a probei de plasmă din grupa B (2 ore după administrarea PQ).
Comparația leziunii pulmonare între cele trei grupuri 72 de ore după otrăvirea PQ (HE, mărire originală × 100).
S-au observat modificări patologice marcate în țesutul stomacal, cum ar fi abruptia mucoasei, mucoasa gastrică hiperemică și gastroragia în decurs de 24 de ore după otrăvirea PQ. S-au constatat, de asemenea, infiltrarea leucocitelor și afectarea glandelor gastrice. Astfel a fost urmată repararea țesutului stomacal (Figura 6).
Compararea leziunilor stomacale între cele trei grupuri la 2 ore după otrăvirea PQ (HE, mărire originală × 100).
Comparația leziunii cu jejun între cele trei grupuri la 2 ore după otrăvirea PQ (HE, mărire originală × 100).
tabelul 1
Scoruri patologice ale șobolanilor (medie ± SD)
DISCUŢIE
Primul caz de mortalitate cu paraquat a fost publicat în 1966, [31] urmat de un număr mare de rapoarte. Intoxicația PQ ca problemă medicală a devenit o povară socială și a atras multă atenție. Ingerarea a peste 20 mL de PQ poate provoca moartea din cauza insuficienței multi-organe, iar 10-20 mL poate duce la fibroză pulmonară ireversibilă care duce la deces în câteva săptămâni. [32] Suntres [33] a făcut o analiză de probă amplă, arătând că doza letală orală de PQ pentru adulți a fost de 30-40 mg/kg. A existat o relație strânsă între concentrația plasmatică PQ și mortalitate. [34] Tratamentul actual al otrăvirii cu PQ se concentrează pe reducerea absorbției PQ din tractul gastro-intestinal și creșterea eliminării acestuia. [32] Chiar dacă cărbunele activ a fost utilizat pentru tratarea toxicității PQ, [14] dovezile nu au fost suficiente pentru a confirma că cărbunele poate îmbunătăți prognosticul pacienților. Deoarece efectul terapeutic al smecta asupra șobolanilor cu toxicitate PQ a fost rar studiat, am încercat să investigăm dacă smecta poate reduce concentrația plasmatică PQ și poate îmbunătăți modificările patologice ale șobolanilor după otrăvirea PQ.
Farmacocinetica PQ este diferită la oameni și animale. Concentrația plasmatică maximă a pacienților are loc în decurs de 2-4 ore de la ingestia PQ și apoi scade. [35] Scăderea inițială, care se numește faza de distribuție, este mai rapidă și are un timp de înjumătățire de aproximativ 5 ore, în timp ce volumul de distribuție este de aproximativ 1,2-1,6 L/kg. Timpul de înjumătățire în faza de eliminare ulterioară este de aproximativ 84 de ore. Pe de altă parte, concentrația plasmatică maximă apare la câini la aproximativ 60-90 de minute după ingestia PQ și întreruperea barierei mucoasei gastrice. [36,37] Distribuția PQ poate fi descrisă ca un model cu trei compartimente: 1) compartimentul plasmatic; 2) compartiment cu absorbție și îndepărtare rapidă, cum ar fi rinichiul; 3) compartimentul de absorbție lentă, cum ar fi plămânul, atingând o concentrație maximă la 4-5 ore după ingestia de PQ, indiferent de nivelul plasmatic de PQ. Acest model explică modificările unice ale nivelului PQ plasmatic. Cu toate acestea, dinamica PQ la șobolani a fost rar investigată. Studiile [38,39] au arătat că concentrația plasmatică de paraquat a șobolanilor s-a menținut în 24 de ore după otrăvirea cu PQ și a dispărut în 72 de ore, care poate fi detectată în plămâni, stomac și intestin la 10 zile după administrarea PQ.
În studiul nostru, șobolanii morți au fost eliminați. Concentrațiile plasmatice de PQ la șobolani cu intoxicație au scăzut în timp, iar concentrația maximă a avut loc la 2 ore după administrarea PQ și a fost menținută la un nivel mai mare în decurs de 6 ore după intoxicație. După aceea, concentrația plasmatică a PQ a început să scadă și a atins nivelul minim 72 de ore după administrarea PQ (Figura 4). În același timp, concentrația plasmatică a PQ a fost mai mică în grupul tratat cu smecta decât în grupul otrăvit (P Gunnell D, Eddleston M, Phillips MR, Konradsen F. Distribuția globală a auto-otrăvirii fatale a pesticidelor: o analiză sistematică BMC Public Health, 2007; 7: 357. [Articol gratuit PMC] [PubMed] [Google Scholar]
- Cele mai bune 10 surse de alimentare pentru pedale din 2020 revizuiesc efectele dvs. cu puterea noastră recomandată
- Efectele psihologice ale postului pe termen scurt la femeile sănătoase
- Condimente, pudră de curry Informații nutriționale și calorii
- Nutriție sportivă - calciu, efecte, alimente, nevoi, corp, dietă, absorbție, carbohidrați, sănătate
- Cele mai bune 9 surse de alimentare cu pedale din 2020 alegerea noastră de surse de alimentare de top pentru efectele dvs.