Bayarmaa Mandzhieva
1 Medicină internă, AdventHealth Orlando, Orlando, SUA
John Taylor
2 Medicină internă, AdventHealth, Orlando, SUA
Hammad Zafar
3 Medicină internă, Advent Health, Orlando, SUA
Mamoon Ur Rashid
1 Medicină internă, AdventHealth Orlando, Orlando, SUA
Abu H Khan
4 Gastroenterologie, AdventHealth, Orlando, SUA
Abstract
Există diverse etiologii ale leziunilor și inflamației colonului. Cele mai frecvent descrise colitide din practica clinică sunt asociate cu infecții, boli inflamatorii intestinale, ischemie, radiații și medicamente. Peretele colonic are un set limitat de răspunsuri la diferite tipuri de leziuni; prin urmare, există o suprapunere între multe dintre aceste tulburări. Colita activă focală se caracterizează prin criptită neutrofilă izolată cu fundalul mucoasei cu arhitectură normală a criptei. Acest tip inflamator poate fi ușor neobservat de patologi, deoarece la examinarea cu putere redusă mucoasa poate avea un aspect aproape normal. Este posibil ca medicii generaliști să nu fie familiarizați cu acest termen, cu etiologiile subiacente, cu factorii de risc asociați, cu cursul, cu terapiile disponibile și cu urmărirea.
Prezentăm un caz al unei femei de 82 de ani, cu diaree cronică și scădere în greutate. Ea a avut un antrenament infecțios negativ și o serie de radiologie normală. Ulterior, ea a fost supusă unei evaluări endoscopice în locul simptomelor persistente și debilitante, care au dezvăluit descoperiri macroscopice nespecifice, cu patologie care constată colita focală activă. Ea a fost tratată empiric cu un curs de 14 zile de Xifaxan și a răspuns bine la tratament cu o rezolvare aproape completă a simptomelor sale și fără recurență la o urmărire de șase luni.
Introducere
Colita focală activă (FAC) este un termen histologic care descrie constatarea izolată a infiltrării focale a criptelor colonice de către neutrofile. Există încă controverse semnificative în legătură cu implicația clinică a diagnosticului de FAC, care poate fi sau nu relevant din punct de vedere clinic.
Prezentarea cazului
O femeie în vârstă de 82 de ani a prezentat la cabinetul de gastroenterologie plângeri de diaree, greață, crampe abdominale, flatulență crescută și anorexie în ultimele trei luni. De asemenea, a estimat că a pierdut aproape 20 de kilograme în ultimele șase luni, fără să vrea.
Ea a descris diareea ca fiind explozivă și cantitatea de diaree corelată cu cantitatea de mâncare pe care o consuma, dar nu cu tipul de mâncare. Ea a raportat că a luat un curs recent de Flagyl timp de trei zile, fără ameliorarea simptomelor și nici o altă expunere recentă la antibiotice. Încercase Imodium fără ușurare. A negat febră, frisoane, emeză, constipație, icter, melenă, hematochezie, mucus în scaune, tenesm, dureri în piept, simptome respiratorii sau urinare.
Ea a negat episoade similare în trecut, orice modificare recentă a medicamentelor sale, utilizarea antiinflamatoarelor nesteroidiene cronice (AINS), contactele bolnave sau călătoriile internaționale recente. Ea a avut o istorie de infecție cu giardia în urmă cu mai bine de 10 ani și a avut o colonoscopie normală în 2007.
Istoricul ei medical trecut a fost semnificativ pentru carcinomul intraductal in situ al sânului stâng, boala coronariană, hipertensiunea, hiperlipidemia, tirotoxicoza, boala arterelor periferice și osteopenia. Istoricul ei chirurgical din trecut a inclus lumpectomia mamară stângă, histerectomia, colecistectomia, îndepărtarea masei renale stângi și apendicectomia. Istoricul familial a fost negativ pentru bolile inflamatorii intestinale (IBD) și pentru afecțiunile maligne ale tractului gastro-intestinal. Ea a avut antecedente de fumat și a refuzat consumul de alcool sau de droguri ilicite.
La birou la prezentarea inițială, semnele vitale erau în limite normale, iar examinarea fizică nu era remarcabilă. Un număr complet de sânge, un panou metabolic complet și un hormon stimulator al tiroidei au fost normale. A avut studii negative privind scaunele pentru Clostridium difficile și culturi negative de scaune pentru Vibrio, Yersinia, Shigella, Salmonella, Campylobacter și Escherichia coli 0157: H7.
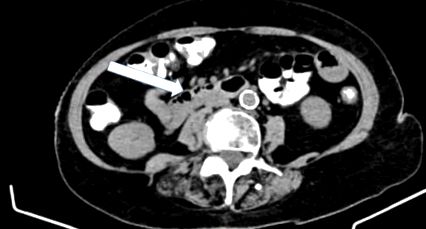
Ea a suferit un CT al abdomenului și pelvisului cu contrast înainte de vizita inițială la cabinet, comandat de urologul său pentru evaluarea durerii de flanc rezolvate, care a fost negativă pentru anomaliile intra-abdominale acute (Figura 1).
Fără îngroșare sau obstrucție a peretelui intestinal. Fără eșantonare mezenterică sau fluid liber.
I s-a recomandat să finalizeze studiile cu scaun cu antigen giardia și examen microscopic cu ovule și paraziți și a fost programată pentru o colonoscopie diagnostic cu biopsii. Studiile privind scaunele au prezentat rezultate negative pentru etiologiile infecțioase. Având în vedere pierderea semnificativă în greutate la un pacient în vârstă, a fost comandată și esofagogastroduodenoscopia (EGD).
Ea a fost tratată empiric cu un studiu cu Xifaxan de trei ori pe zi timp de 14 zile pentru posibilul IBS cu diaree (IBS-D), care a primit un tratament nereușit anterior cu Imodium și Flagyl. De asemenea, i s-au administrat două comprimate FDgard de două ori pe zi pentru tratamentul simptomatic al crampelor abdominale.
Ea a finalizat pregătirea intestinului pentru colonoscopie cu SUPREP® Bowel Prep Kit (Braintree Laboratories, Braintree, MA) (sulfat de sodiu, sulfat de potasiu și sulfat de magneziu).
EGD și colonoscopia cu o bună pregătire a intestinului au observat gastrită ușoară Helicobacter pylori negativă, eritem neuniform în colonul sigmoid (Figura (Figura 2) 2) cu patologie care notează FAC, polip hiperplastic de 5 mm în sigmoid, diverticuloză și hemoroizi interni și externi de dimensiuni medii. Biopsiile intestinului subțire au exclus boala celiacă și mai multe biopsii aleatorii din fiecare segment al colonului au fost negative pentru colita microscopică. Un mic polip sesil de 5 mm în colonul sigmoid a fost complet îndepărtat cu o capcană rece. Două endoclipuri au fost desfășurate profilactic la locul polipectomiei.
Eritem mucos ușor petic care implică colon sigmoid (săgeți gri). Puțini diverticuli împrăștiați (săgeți galbene).
Având în vedere concluziile colonoscopiei, a fost diagnosticată cu colită focală acută și sa luat decizia de a finaliza cursul Xifaxan și de a lua în considerare trecerea la ciprofloxacină și Flagyl în caz de eșec al tratamentului. La întâlnirea de urmărire de două săptămâni, ea a raportat o ameliorare semnificativă a simptomelor sale (în principal diaree, crampe abdominale și flatulență) după cursul de 14 zile de Xifaxan. Pacientul a fost sfătuit să urmeze o dietă bogată în fibre, fără prescripție medicală Benefiber sau Metamucil de două până la trei ori pe zi și cu FODMAP scăzut (oligozaharide fermentabile, dizaharide, monozaharide și polioli).
Discuţie
Modelul FAC se caracterizează printr-un singur focar sau mai multe focare de infiltrare neutrofilă a criptelor cu o mucoasă colonică altfel neremarcabilă. Criptele de fundal sunt bine conservate, fără dovezi ale rănirii cronice [4].
Mai multe entități etiologice pot fi prezentate ca FAC pe rapoartele de patologie. Cele mai frecvente scenarii clinice includ colita infecțioasă acută autolimitată, IBD la începutul cursului său, colita ischemică, IBS, colita Clostridium difficile, medicamente sau leziuni chimice și artefactul de pregătire a intestinului [4]. Medicamentele asociate cu FAC sunt AINS, acid micofenolat și ipilimumab, printre altele [5]. Deși diareea este cel mai frecvent motiv pentru antrenament la majoritatea acestor pacienți, FAC poate fi, de asemenea, o constatare incidentală ca urmare a pregătirii intestinului fosfo-sodic la pacienții asimptomatici supuși colonoscopiei de screening [6]. Ozdil și colab. a constatat că 6,6% dintre pacienții cu IBS aveau FAC și poate fi eligibil să facă o biopsie de rutină la pacienții de sex feminin și la pacienții cu vârsta peste 50 de ani [7].
Osmond și colab. în revizuirea lor retrospectivă a cazurilor de FAC la copii și adolescenți, au raportat următoarele simptome clinice: diaree, sângerări rectale, dureri abdominale, vărsături și altele [8].
Dintre acești pacienți, majoritatea s-au prezentat ca o colită infecțioasă sau acută autolimitată, cu un subgrup semnificativ de pacienți imunocompromiși. În timpul urmăririi ulterioare, niciunul dintre pacienți nu s-a dovedit mai târziu să aibă colită ulcerativă sau CD [1].
Diareea cronică poate fi uneori un scenariu clinic foarte provocator datorită multitudinii de diagnostice diferențiale de luat în considerare. Majoritatea descoperirilor macroscopice din timpul evaluării endoscopice nu sunt remarcabile sau nespecifice [9]. Greenson și colab. în studiul lor asupra populației adulte a raportat că rezultatele endoscopice ale FAC au variat. Unii dintre pacienți au prezentat rezultate endoscopice complet normale, în timp ce alții au prezentat ulcere aftoase împrăștiate pe mucoasa de fond normală sau eritem neuniform [1]. Astfel, istoricul medical trecut al pacientului, analiza medicamentelor și corelația clinică sunt cruciale.
FAC este un diagnostic histopatologic. Semnul distinctiv este criptita neutrofilă care implică mai multe cripte adiacente pe un singur fragment de biopsie. Lamina propria este adesea hipercelulară cu arhitectură normală a fundalului mucoasei și fără metaplazie a celulelor Paneth. Prezența celulelor epliteliale a criptelor apoptotice este variabilă [10].
Caracteristicile histologice nu pot face distincție între FAC incidental și FAC semnificativ clinic. Prin urmare, rămâne o provocare de diagnostic în care caracteristicile patologiei trebuie să se potrivească în mod adecvat prezentării clinice corecte.
Gestionarea FAC în sine nu este bine descrisă. Prin urmare, medicii își folosesc în general judecata clinică și tratamentul disponibil pentru presupusa etiologie subiacentă, cum ar fi IBD, IBS sau colita infecțioasă acută.
Caracteristicile clinicopatologice ale CD și ale anumitor agenți patogeni enterici se pot imita într-o oarecare măsură și se pot prezenta cu o imagine endoscopică a enterocolitei focale/segmentare. Cele mai notabile microorganisme în acest sens sunt infecțiile cu Campylobacter, Salmonella, Shigella, Yersinia, serotipul Escherichia coli O157: H7, Chlamydia trachomatis, Mycobacterium tuberculosis, Actinomyces spp, Entamoeba histolytica, Giardia lamblia și altele [11]. Flora intestinală normală poate deveni patogenă și în anumite circumstanțe.
Există dovezi care susțin ideea că bacteriile acționează ca forță motrice atât pentru inflamația intestinală activă, cât și pentru cea cronică. O ipoteză este că inflamația cronică se poate datora răspunsurilor imune anormale la flora intestinală normală. Aceste noțiuni susțin utilizarea antibioticelor în cazul inflamației intestinale active și, de asemenea, aduce ideea de a manipula flora enterică ca posibilă terapeutică pentru cazurile mai cronice [12].
IBS a fost atribuit multor factori declanșatori, numeroase studii sugerând că până la o treime din cazurile de IBS-D rezultă dintr-o infecție bacteriană anterioară [13].
Utilizarea antibioticelor orale are probabil utilitate terapeutică în condiții enterice multiple având în vedere aceste noțiuni. Cu toate acestea, există mai multe bariere în calea utilizării antibioticelor, cum ar fi preocupările pentru rezistența crescândă a bacteriilor, interacțiunile cu alte medicamente și efectele secundare ale antibioticelor. Utilizarea antibioticelor minim absorbite, care sunt mai mult vizate pentru intestin, poate oferi o soluție la aceste preocupări [14].
Rifaximin (Xifaxan) este un antibiotic sigur, derivat din rifamicină, cu o gamă largă de spectru antimicrobian care acoperă majoritatea bacteriilor Gram-pozitive și Gram-negative, inclusiv aerobii și anaerobii. Are o absorbție sistemică foarte slabă după administrarea orală și o excreție fecală completă ca medicament nemodificat [12].
Rifaximin are mai multe indicații, care includ cazuri selectate de diaree infecțioasă, encefalopatie hepatică și profilaxie chirurgicală. Medicamentul a găsit, de asemenea, utilizarea în prevenirea creșterii bacteriene intestinale subțiri, a colitei asociate cu Clostridium difficile, a bolilor diverticulare și a diareei infecțioase. Poate beneficia și în alte condiții, cum ar fi IBD și IBS [14].
Diferite studii au sugerat că ar putea fi benefic în tratamentul IBD activ refractar la tratamentul standard. De exemplu, Shafran și colab. a prezentat recent un studiu deschis cu privire la eficacitatea și siguranța rifaximinului 600 mg/zi timp de 16 săptămâni în tratamentul CD ușor până la moderat activ. La sfârșitul studiului, 59% dintre pacienți erau în remisie [15].
Rifaximin s-a dovedit mai eficient decât placebo pentru simptomele globale și balonarea la pacienții cu IBS. Câștigul terapeutic modest a fost similar cu cel obținut de alte terapii disponibile în prezent pentru IBS [13].
Banaag și colab. în studiul lor retrospectiv multicentric au arătat că există aproximativ 25% dintre pacienții care prezintă diaree, dureri abdominale și IBS cu constatarea histologică a FAC fără un diagnostic definitiv. Peste 50% dintre pacienții care au avut diaree au avut FAC, iar dintre aceștia 44% au răspuns la acidul 5-aminosalicilic (5ASA), evident prin rezolvarea simptomelor în decurs de două până la șase săptămâni [16].
În rezumat, FAC rămâne o provocare de diagnostic. Trebuie să se includă istoricul de prezentare al pacientului, medicamentele și rezultatele endoscopiei pentru a ajuta la restrângerea diagnosticului diferențial. Histologia poate fi de ajutor; cu toate acestea, nu există nicio constatare sau caracteristică specifică care să poată distinge între FAC incidental și clinic semnificativ (cum ar fi un număr minim de neutrofile).
Ca atare, ar trebui efectuate studii suplimentare pentru a determina modele de boală histologică și/sau un prag de inflamație, astfel încât să se poată prezice traiectoria bolii și să permită o mai bună stratificare a pacientului.
Am prezentat cazul FAC tratat eficient cu rifaximină.
Rifaximin este un agent foarte promițător, cu un profil de siguranță excelent, iar mai multe studii experimentale cu rifaximin în practica clinică vor ajuta la definirea în continuare a rolului acestui antibiotic în gastroenterologie.
Concluzii
Cazul nostru este unic, deoarece agenții patogeni infecțioși nu au fost identificați și nu a avut factori de risc asociați frecvent cu FAC în literatura de specialitate, cum ar fi IBD, utilizarea AINS sau prepararea intestinului cu fosfo-sodă. Ea a obținut o rezolvare semnificativă a diareei în termen de două săptămâni de la tratamentul cu Xifaxan fără reapariție timp de cel puțin șase luni. Pe scurt, FAC ar trebui să fie considerat cu tărie în diagnosticul diferențial la pacienții care prezintă diaree și mucoasă normală macroscopic. Cazul subliniază, de asemenea, necesitatea de a dobândi mai multă experiență în tratamentul FAC cu Xifaxan.
Note
Conținutul publicat în Cureus este rezultatul experienței clinice și/sau al cercetărilor efectuate de persoane sau organizații independente. Cureus nu este responsabil pentru acuratețea științifică sau fiabilitatea datelor sau concluziilor publicate aici. Tot conținutul publicat în cadrul Cureus este destinat numai scopurilor educaționale, de cercetare și de referință. În plus, articolele publicate în cadrul Cureus nu ar trebui considerate un substitut adecvat pentru sfatul unui profesionist calificat din domeniul sănătății. Nu ignorați sau evitați sfatul medicului profesionist din cauza conținutului publicat în cadrul Cureus.
Autorii au declarat că nu există interese concurente.
- Efectul expunerii la solvent organic asupra progresiei bolii cronice renale Cohorta GN-PROGRESS
- Aprovizionarea pentru plimbare ACTIVĂ
- Depresie la pacienții cu boală hepatică grasă nealcoolică și hepatită virală cronică B și C -
- Efectele stresului mental cronic și ale dietei aterogene asupra mediului inflamator imunitar în
- Articolul complet Extracția lichidului supercritic al algelor îmbunătățește nivelurile de active biologice