Ai văzut vreodată o mărgele de apă așezată pe o suprafață? Acest lucru se datorează faptului că apa are o proprietate numită tensiune superficială. Această tensiune face ca apa să formeze o margele pe suprafața unor lucruri precum sticla sau țesătura. Puteți vedea tensiunea superficială la locul de muncă plasând o picătură de apă pe un blat. Picătura își va menține forma și nu se va răspândi.
Pentru a curăța murdăria de pe hainele noastre, apa trebuie să poată ajunge la suprafață. Apa poate ajunge la suprafață dacă tensiunea superficială este redusă. Pentru a face acest lucru, folosim un grup de substanțe chimice numite agenți activi de suprafață sau surfactanți.
Ce este un agent tensioactiv?
Surfactanții schimbă modul în care se comportă apa. Când se adaugă un agent tensioactiv, tensiunea superficială este redusă. Acum apa se poate extinde și uda suprafața (de exemplu, haine, vase, blaturi) pe care încercăm să le curățăm.
Să vedem acum ce se întâmplă la suprafață.
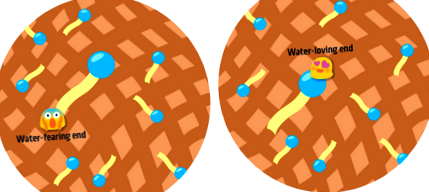
Fiecare agent tensioactiv are două capete. Un capăt vrea să fie în apă, iar celălalt nu.
Capătul care se teme de apă este cunoscut sub numele de capăt hidrofob. Hidrofobul provine din două rădăcini grecești, hidro- (adică apă) și -fobie (adică frică). Ați auzit expresia „uleiul și apa nu se amestecă?” Acest lucru este important aici!
Capătul temător de apă al surfactantului este alcătuit din lanțuri de hidrocarburi. O hidrocarbură este o moleculă care este formată din hidrogen și carbon. Lanțurile adoră uleiul și grăsimile și vor încerca să stea departe de apă.
Capătul iubitor de apă este cunoscut sub numele de capăt hidrofil. Am învățat că hidro- este o rădăcină greacă care înseamnă „apă”. Deci, dacă -fobic înseamnă „teamă”, atunci -filic înseamnă iubire. Capătul iubitor de apă al substanței chimice este atras de apă.
Modul în care aceste două capete interacționează cu solul și apa este secretul modului în care funcționează un agent tensioactiv.
Cum curăță surfactanții
Odată ce surfactantul este adăugat în apă, capetele care se tem de apă încearcă să stea departe de apă. Acestea fac acest lucru organizându-se sub forma unei sfere cu capetele iubitoare de apă în exterior și capetele înfricoșătoare de apă protejate în interior. Această formă sferică a agenților tensioactivi se numește micelă.
Săpun amestecând cu ulei la microscop, formând micele.
Micela este importantă, deoarece este cea care prinde solul. Amintiți-vă, interiorul micelei este hidrofob și nu vrea să fie aproape de apă. Solul este, de asemenea, hidrofob, deci îi place mediul creat de micelă.
Atracția solului către interiorul micelei de surfactant ajută la slăbirea solului de la suprafața sa. Odată ce solul se ridică de pe suprafață, acesta devine suspendat în apa din micelă. Această suspensie este, de asemenea, cunoscută sub numele de emulsificare a unui lichid în altul. Fericit în interiorul micelei, solul nu se va așeza la suprafață.
Acum, când solul este prins în micelă și micelele sunt suspendate în apă, este ușor să spălați solul.
Amintiți-vă că exteriorul micelei noastre iubește apa. Deci, în timp ce clătim, micela plutește și rămânem cu o suprafață curată!
- Curățare de scurgere a furtunilor NAP North American Pipeline Services NJ
- De ce detoxifierea este o necesitate de curățare de primăvară
- De ce gustul alimentelor este atât de delicios științific american
- Tratamente pentru modificarea rozului în vinurile albe American Journal of Enology and Viticulture
- TDA modifică politica nutrițională pentru școlarii din Texas, legea sănătății; Institutul de politici
