Departamentul de Anestezie, Clinica Mayo, 200 First Street SW, Rochester, MN 55905, SUA
autorul corespunzator M. J. Joyner: Clinica Mayo, Departamentul de Anestezie, 200 First Street SW, Rochester, MN 55905, SUA. E-mail: [email protected] Căutați mai multe lucrări ale acestui autor
Departamentul de Biochimie și Biologie Moleculară, Clinica Mayo, 200 First Street SW, Rochester, MN 55905, SUA
Departamentul de Anestezie, Clinica Mayo, 200 First Street SW, Rochester, MN 55905, SUA
autorul corespunzator M. J. Joyner: Clinica Mayo, Departamentul de Anestezie, 200 First Street SW, Rochester, MN 55905, SUA. E-mail: [email protected] Căutați mai multe lucrări ale acestui autor
Departamentul de Biochimie și Biologie Moleculară, Clinica Mayo, 200 First Street SW, Rochester, MN 55905, SUA
Abstract
Introducere
De asemenea, este important să subliniem, înainte de a continua, că conceptul de genă este anterior ADN-ului și a fost inițial definit sau presupus a fi ceva cu un efect fenotipic la nivel înalt în sine (Johannsen, 1911; Gerstein și colab. 2007; Edwards, 2011). Astfel, pare rezonabil să susținem că, din moment ce estimările de eritabilitate statistică timpurie ale lui Galton - Fisher erau ridicate, atunci „genele” în sensul pre ADN conduceau ereditatea. Ar trebui, de asemenea, să subliniem că definiția schimbătoare de-a lungul anilor „ceea ce este o genă” la versiunea actuală centrată pe ADN poate să fi contribuit, de asemenea, la o viziune prea simplificată a relației genotip - fenotip, așa cum se aplică ADN-ului. Problemele asociate cu această viziune prea simplificată au fost apoi susceptibile de a fi amplificate de așa-numita Dogmă Centrală a Biologiei Moleculare care susține că transferul de informații de la ADN la proteine și prin extinderea fenotipului este în esență o stradă cu sens unic (Crick, 1970). Astfel, estimările de eritabilitate statistică și abordările fundamentale pentru realizarea acestora au rămas similare de-a lungul multor ani, în timp ce conceptul de genă s-a schimbat dramatic.
Observațiile și estimările precum acești genetici au stimulat să creadă că un număr potențial mare de alele intra și inter-locus sunt responsabile pentru variația fenotipică a trăsăturilor complexe, iar această căutare a continuat pe măsură ce definiția genei a devenit ADN-centrică (pentru perspectivă vezi Fisher, 1919 și Edwards, 2011).
Dacă sprijinul cercetării continuă la niveluri viguroase, este greu de imaginat că știința genomică nu va dezvălui curând misterele factorilor ereditari în bolile de inimă, cancerul, diabetul, bolile mintale și o serie de alte afecțiuni.
Cu toate acestea, pentru ca viziunea liniară a medicinei personalizate prezentată la începutul acestui eseu să funcționeze pentru bolile comune, se pare că trebuie îndeplinite trei criterii. În primul rând, trebuie identificată o variantă genetică clar identificabilă sau o cale asociată legată în mod clar de o boală. În al doilea rând, această variantă trebuie să poată fi modificată sau acționată de o intervenție preventivă sau terapeutică. În al treilea rând, atunci când astfel de informații sunt disponibile pacienților, clinicienilor individuali și sistemelor de îngrijire a sănătății le vor folosi într-un mod rațional pentru a reduce riscul de boală și/sau pentru a îmbunătăți luarea deciziilor terapeutice. Având aceste comentarii introductive ca fundal, acum ridicăm cinci întrebări pentru domeniul general al medicinei personalizate.
Care este starea actuală a relației genotip - fenotip?
Parantetic, mai multe genotipuri rare au apărut ca cauzele clare ale afecțiunilor medicale catastrofale. Un bun exemplu este cardiomiopatia hipertrofică potențial letală și alte afecțiuni aritmogene care ucid de obicei sportivi tineri aparent sănătoși cu avertisment mic sau deloc. Spre deosebire de speranța timpurie că doar câteva variante necinstite ar fi responsabile pentru aceste condiții, au apărut un număr imens de mutații private (Landstrom & Ackerman, 2010). Mai important, nu toți purtătorii genotipului potențial letal manifestă fenotipul de îngrijorare, evidențiind problema generală a penetranței variabile pentru medicina predictivă pe baza informațiilor genotipice. La indivizii neafectați, probabil că sunt angajate alte căi de protecție sau redundante care fie țin sub control expresia variantei potențial letale, fie o contracarează în alte moduri pentru a atenua letalitatea. Căile moleculare implicate în această atenuare ar putea include transcrierea necodificatoare, modul în care căile interacționează ca rețele și rolul aproape inevitabil al mecanismelor epigenetice.
Într-o notă mai pozitivă, mutațiile rare și, în general, private ar putea explica unele cazuri extreme de longevitate extremă, dar, așa cum este cazul fenotipurilor care sunt susceptibile de a avea cauze complexe, explicațiile genetice clare pentru longevitatea extremă sunt evazive (Christensen și colab. 2009; Sebastiani & Perls, 2012). Astfel, pentru cele mai frecvente boli netransmisibile, înțelegerea rolului variației genotipice ca factor principal al fenotipului rămâne o provocare importantă (Ganesh și colab. 2013). O posibilitate este că rolul variației genotipice în bolile comune netransmisibile este în esență copleșit de factori de mediu, culturali și comportamentali (Marmot și Syme, 1976).
O expansiune complementară este că aceste boli includ de obicei vârsta ca factor major de risc și ideile despre „medicina evoluționistă” sugerează că, pe măsură ce am evoluat, am trăit o viață mai scurtă în medii care sunt radical diferite de lumea actuală pentru majoritatea oamenilor. În acest context, a existat o căutare a „genelor economisitoare” bazată pe ideea că stresul nutrițional frecvent a favorizat selecția genotipurilor care ar putea câștiga în greutate atunci când caloriile erau abundente și astfel ar putea evita moartea din cauza foametei în timpul foametei (McDermott, 1998). Argumente similare au fost aduse pentru selectarea genotipurilor care au favorizat retenția de sare și pentru a păstra volumul de sânge în medii fierbinți (Young, 2007). Cu toate acestea, atunci când aceste genotipuri sunt expuse lumii moderne, o combinație de longevitate plus hrană abundentă și sare duce la o explozie de boli netransmisibile, inclusiv obezitate/diabet și hipertensiune.
Care este statutul actual al ipotezei comune - boală - comună - variantă?
Poate genotipul să informeze luarea deciziilor clinice pentru medicamentele utilizate în mod obișnuit?
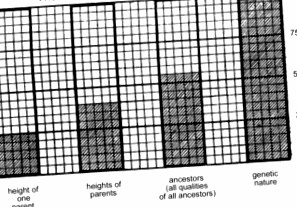
Pentru cele mai frecvente boli, în plus față de generația actuală, datele „omice” pentru prezicerea riscurilor au avut o valoare limitată. Un bun exemplu este că datele de incluziune privind variantele genetice considerate a crește riscul de diabet de tip 2 nu prea ajută la îmbunătățirea valorii predictive a scorurilor de risc pe baza factorilor tradiționali de risc fenotipici (Talmud și colab. 2010). Așa cum s-a menționat mai sus, datele pentru predicția bolii sunt în concordanță cu observația că adăugarea datelor despre variantele genetice contribuie puțin la îmbunătățirea predicției înălțimii adulților dincolo de tehnicile clasice galtoniene care apar din epoca victoriană (Aulchenko și colab. 2009).
Un domeniu în care impactul „omicilor” asupra luării deciziilor clinice a arătat rezultate mixte (inclusiv pozitive) este utilizarea genotipării pentru a prezice răspunsul la medicamente. Exemplele includ determinarea regimurilor optime de dozare pentru 6 - mercaptopurină în leucemia limfoblastică acută și, de asemenea, medicamentul antiplachetar clopidogrel (Lennard și colab. 1990; Scott și colab. 2013). În plus, tratamentul individualizat de variantă genetică pentru terapia cu tamoxifen în cancerul de sân sa dovedit a fi promițător, dar sunt necesare studii mai mari pentru a confirma rezultatele studiilor mai mici (Schroth și colab. 2009; Provincie și colab. 2014). Cu toate acestea, știrile din acest domeniu nu sunt toate pozitive și mai multe studii recente privind varianta genică - dozarea informată a terapiei anticoagulante Coumadin nu a reușit să arate rezultate mai bune comparativ cu schemele de dozare tradiționale bazate pe fenotipul clinic (Furie, 2013).
Un subiect interesant legat de luarea deciziilor clinice, medicina personalizată și doza de medicamente este controversa recentă din jurul „noilor” ghiduri pentru terapia cu statine lansate de American Heart Association și American College of Cardiology (Stone și colab. 2013). S-ar fi putut anticipa pe baza așteptărilor și promisiunilor HGP că noile orientări ar fi conduse parțial de informații genetice individuale sau de alți biomarkeri avansați. În schimb, noile orientări se bazează pe un calculator de risc fenotipic relativ generic, pe o monitorizare mai puțin frecventă sau mai agresivă a nivelului colesterolului din sânge și pe scheme de dozare mai simple. Pe baza acestor caracteristici, noile orientări apar în direcția opusă celei a medicinei personalizate. Răspunsul la noile orientări subliniază, de asemenea, provocările sociale individuale și colective ale orientărilor în general.
Variantele rare vor avea implicații terapeutice?
Vor fi direcționate căile dominante?
În SUA (și în alte țări) a existat un „război împotriva cancerului” care a început în 1971. Unii au susținut că succesul acestui „război”, în special pentru terapia medicamentoasă îndreptată împotriva tumorilor solide, a fost dezamăgitor (Hanahan, 2014) . În acest context, dezvoltarea unei secvențieri genetice foarte rapide și a altor tehnologii „omice” a dus la descoperirea faptului că multe tumori solide cu fenotipuri clinice și histologice similare pot fi conduse sau pot manifesta mutații genetice diferite. La un anumit nivel, acest lucru este foarte interesant, deoarece este o altă provocare pentru ideea că genotipul este factorul de conducere al fenotipului. La un alt nivel, cu suficiente informații „omice” despre o anumită tumoare, ar putea fi posibil să se țintească mai bine terapia anti-neoplazică folosind compuși care afectează mutația genetică, defectul sau produsul genetic care cauzează problema. Succesul imatinibului în tratarea leucemiei mieloide cronice arată atât potențialul de succes, cât și limitările pe termen mai lung cu această abordare (Mahon, 2012). Această abordare generală oferă, de asemenea, unele promisiuni pentru vizarea bolilor rare ne-neoplazice prin găsirea medicamentelor deja aprobate, care ar putea oferi beneficii terapeutice prin așa-numita reutilizare a medicamentelor. Cu toate acestea, exemplul leucemiei mieloide cronice este neobișnuit.
În timp ce terapia individualizată pentru tumorile solide este atrăgătoare, există cel puțin două probleme principale cu aceasta. Primul este practic și se referă la modul cel mai bun de a proiecta studii clinice pentru a testa dacă chimioterapia individualizată este mai eficientă în comparație cu schemele de chimioterapie standard. Al doilea aspect este faptul că majoritatea tumorilor sunt multi-clonale și că, vizând clona dominantă, clonele rezistente care supraviețuiesc vor apărea apoi cu răzbunare (Gatenby, 2009; Hanahan, 2014; Watson, 2013). Pentru ambele scenarii, este pur și simplu prea devreme să spunem și am sugera doar că este posibil să existe o serie de răspunsuri la terapia „omic”. Cu toate acestea, deoarece tumorile sunt multi-clonale, ideea că testarea sensibilității la medicamente similară cu cea utilizată pentru tratamentul antibiotic al infecțiilor microbiene va fi aplicabilă pe scară largă tumorilor solide poate fi o întindere.
rezumat
Închidem acest eseu postulând că a existat o influență omniprezentă a centrismului genetic inerent în sinteza modernă împreună cu Dogma centrală a biologiei moleculare asupra gândirii biomedicale. Credem că această influență a devenit acum contraproductivă. Astfel, este esențial pentru ideile noi care decurg din biologia evoluției evidențiate în acest număr special al Jurnalul de fiziologie și în alte părți pentru a informa mai complet gândirea biomedicală despre relația complexă dintre ADN și fenotip (Müller, 2007; Jablonka, 2012; Noble, 2013; Omholt, 2013). A sosit timpul să nu mai urmărim Mendel.
- Jurnalul de control al infecțiilor și metodele de curățare a sănătății
- Depunerea masei grase în timpul sarcinii utilizând un model cu patru componente Journal of Applied Physiology
- Daily Food Journal Jurnalul zilnic de aporturi Calorii alimentare pentru dietă, pierderea în greutate; Cartea jurnalului nutrițional de
- Clinică cu 40 de ani de experiență în medicina occidentală și holistică
- Terapie de curățare - TME-Centrul de educație medicină tibetană