1 Secția de nutriție, Spitalul Tainan Sin-Lau, nr. 57, secțiunea 1, Dongmen Road, orașul Tainan 70142, Taiwan
2 Secția de Chirurgie, Spitalul Tainan Sin-Lau, nr. 57, secțiunea 1, Dongmen Road, orașul Tainan 70142, Taiwan
3 Secția de asistență medicală, Spitalul Tainan Sin-Lau, nr. 57, secțiunea 1, Dongmen Road, orașul Tainan 70142, Taiwan
4 Departamentul de Științe ale Vieții, Colegiul de Bioștiință și Biotehnologie, Universitatea Națională Cheng Kung, nr. 1, University Road, Tainan City 701, Taiwan
Abstract
Prezentăm un bărbat în vârstă de 50 de ani care a suferit de boală ischemică a intestinului, care a suferit rezecția masivă a intestinului subțire și a valvei ileocecale. A trebuit să facă față jejunului proximal de 40 cm și a rămas colonul distal de 70 cm. În perioada postoperatorie, nutriția parenterală (PN) a fost utilizată imediat pentru susținerea nutriției și corectarea dezechilibrului electrolitic. I-am dat PN acasă ca o recomandare regulată pentru starea intestinului scurt după externarea din spital. Acest pacient a tolerat administrarea orală regulată 2 luni mai târziu și nu a dezvoltat sindrom de intestin scurt semnificativ. Au existat mai multe episoade de infecție cu acces venos care l-au tulburat pe acest pacient și l-au internat pentru tratament în timpul PN la domiciliu. Prin urmare, am schimbat PN-ul de acasă cu un model de conicitate ciclic. Pacientul și-a putut menține nutriția și hidratarea numai cu aport oral, după reducerea PN la domiciliu 15 luni mai târziu. El a supraviețuit mai mult de un an fără sprijin PN și a menținut în continuare 80% din greutatea corporală ideală cu o albumină medie de 3,5 ± 0,2 mg/dL. Deși pacientul a fost internat la fiecare două luni pentru a suplimenta substanțele nutritive, totuși, acest lucru a îmbunătățit foarte mult calitatea vieții.
1. Introducere
Rezecția unei porțiuni mari a intestinului subțire poate provoca malabsorbție severă, malnutriție și dezechilibru electrolitic [1, 2]. Rezultatele rezecției depind de cantitatea de intestin rămasă și de secțiunea specifică rezecată și de conservarea lungimii colonului sau de prezența valvei ileocecale [1]. După îngrijirea postoperatorie imediată, menținerea pacientului în viață prin utilizarea nutriției parenterale (PN) și a agenților antisecretori [3] și promovarea adaptării intestinale prin nutriție orală au fost utilizate în mod obișnuit [4]. Zona minimă de absorbție a intestinului subțire pentru a susține viața variază de la individ la individ.
2. Prezentarea cazului
Un bărbat fără adăpost de 50 de ani a leșinat la stație și a fost trimis la spital de trecător, înălțimea de 153 cm și greutatea corporală obișnuită de 54 kg (acum aproximativ trei luni înainte de internare) și s-a plâns de crampe abdominale intermitente cu apetit slab. pentru mai multe zile. Greutatea corporală a pacientului la internare a fost de 40 kg. El a suferit de boală ischemică a intestinului, după ce a suferit rezecția masivă a intestinului subțire și a valvei ileocecale. El a trebuit să facă față cu jejunul proximal de 40 cm (Figura 1) și cu colonul distal de 70 cm rămas. Postoperator, greutatea sa corporală a fost de 34 kg (spital ziua 3). A slăbit de la 54 kg la 34 kg în 4 luni și a dezvoltat malnutriție severă.
În perioada postoperatorie, PN a fost utilizat imediat pentru susținerea nutriției și corectarea dezechilibrului electrolitic. Hrănirea enterală a început 10 zile mai târziu și medicamentele antidiareice (loperamidă 2 mg bid) au fost utilizate pentru tratarea diareei. Progresul dietei a fost o dietă lichidă limpede (continuați să hrăniți 30 mL/oră timp de 2 zile), dieta elementară diluată (continuați să hrăniți 700 kcal/zi timp de 3 zile) și dieta elementară cu concentrație normală (continuați să alimentați 1200 kcal/zi timp de 20 de zile) dietă cu formule polimerice (continuați să hrăniți 1200 kcal/zi timp de 5 zile). Pacientul a tolerat dieta orală moale și a suplimentat 40 de zile mai târziu. I-am dat PN acasă ca recomandare obișnuită și loperamidă după externarea din spital.
Acest pacient a respectat o dietă cu conținut scăzut de oxalat și minimizarea grăsimii intraluminale. Acești nutrienți stimulează în mod direct adaptarea intestinală. A tolerat aportul oral regulat fără medicamente antidiareice 2 luni mai târziu. El nu a dezvoltat sindrom semnificativ de intestin scurt, cum ar fi creșterea mișcărilor intestinale, malabsorbție, anemie, steatoree și pierderea mușchilor. Șase luni mai târziu, greutatea corporală a pacientului a fost menținută la 42 kg, iar albumina serică a fost de 3,6 mg/dL. Au existat mai multe episoade de infecție cu acces venos care l-au tulburat pe acest pacient și l-au internat pentru tratament în timpul PN la domiciliu. Am evaluat starea nutrițională și am asigurat absorbția eficientă a proteinelor în ciuda intestinului subțire relativ scurt. Prin urmare, am schimbat PN-ul de acasă cu un model de conicitate ciclic și am monitorizat greutatea corporală, albumina, electroliții și nivelul hemoglobinei. Spre surprinderea noastră, pacientul și-a putut menține nutriția și hidratarea numai cu aport oral, după ce s-a diminuat PN acasă 15 luni mai târziu. A supraviețuit mai mult de un an fără sprijin parenteral și a menținut în continuare 80% din greutatea corporală ideală (aproximativ 41%)
42 kg) cu o albumină medie de 3,5 ± 0,2 mg/dL. Deși pacientul a înțărcat suportul PN obișnuit, pacientul a început să dezvolte simptome de anemie și deficit de vitamina B1. Pacientul a fost internat timp de trei zile la fiecare două luni prin nutriție parenterală periferică pentru a suplimenta vitaminele și oligoelementele.
3. Discuție
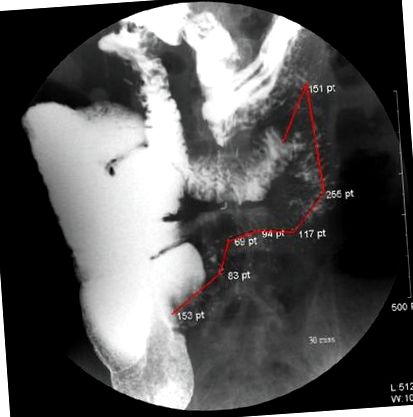
Lungimea intestinală reziduală la acești pacienți înțărcați de la TPN a variat între 27 și 75 cm (medie 57 cm) la copii și adolescenți [5] și de la 57 până la 150 cm (medie 96 cm) la pacienți adulți [6]. Niciunul dintre pacienții adulți cu lungimea reziduală a intestinului subțire mai mică de 40 cm nu a putut realiza o adaptare intestinală completă. Pacientul nostru cu intestin subțire de 40 cm și fără valvă ileocecală a fost înțărcat cu succes din PN. Inspectăm în continuare timpul de tranzit intestinal și seria tractului gastrointestinal scăzut (tractul GI) după administrarea orală a pacientului singur 16 luni. Timpii de tranzit al colonului au fost calculați cu capsule umplute cu radionuclizi și cu raze X abdominale. După 64 de ore, radionuclizii aproape nu au excretat. Seria tractului GI scăzut a arătat că colonul a devenit gros și lung. Lungimea de la 70 cm a devenit de aproximativ 120 cm și abdomenul plin de colon (Figura 2). Administrarea orală a pacientului în libertate, dar el se plânge întotdeauna de distensie, deoarece nutriția promovează adaptarea intestinului subțire și a colonului și creșterea zonei de absorbție. Colonii deosebit de mari, groși și de inerție pentru a prelungi timpul de ședere al alimentelor, care este benefic pentru absorbție.
Mecanismul principal al proteinelor luminale este că acestea sunt digerate în di- și tripeptide pentru absorbție. Transportorul de oligopeptide PepT1 este responsabil pentru transportul di- și tripeptidelor în intestinul mamiferelor [7]. PepT1 este abundent de-a lungul marginii periei intestinului subțire la om, dar este exprimat la niveluri scăzute în celulele absorbante ale colonului. Ziegler și colab. [8] a arătat că reglarea în sus a PepT1 în colonul pacienților cu SBS sugerează că colonul uman poate crește transportul luminal al di- și tripeptidelor în timpul insuficienței intestinale. Acest pacient a menținut o albumină medie de 3,5 ± 0,2 mg/dL. Aceasta a sugerat că expresia crescută a PepT1 colonic este un exemplu de adaptare a intestinului la acest pacient cu intestin scurt.
4. Concluzii
Pacientul cu inerție intestinală scurtă și colonică care primește suport enteral și parenteral timp de câteva luni a crescut în zona absorbantă și funcția intestinului subțire și a colonului. Acest pacient cu intestin scurt funcționează bine numai cu aportul oral, fără nutriție parenterală. Deși pacientul a fost internat la fiecare două luni pentru a suplimenta substanțele nutritive, totuși, acest lucru a îmbunătățit foarte mult calitatea vieții.
Conflict de interese
Autorii declară că nu există conflicte de interese în ceea ce privește publicarea acestei lucrări.
Referințe
- A. Sundaram, P. Koutkia și C. M. Apovian, „Managementul nutrițional al sindromului intestinului scurt la adulți” Jurnalul de Gastroenterologie Clinică, vol. 34, nr. 3, pp. 207–220, 2002. Vizualizare la: Site-ul editorului | Google Scholar
- C. L. Donohoe și J. V. Reynolds, „Sindromul intestinului scurt” Chirurg, vol. 8, nr. 5, pp. 270–279, 2010. Vizualizați la: Site-ul editorului | Google Scholar
- L. M. Nørholk, J. J. Holst și P. B. Jeppesen, „Tratamentul pacienților adulți cu sindrom de intestin scurt cu teduglutidă” Opinia experților privind farmacoterapia, vol. 13, nr. 2, pp. 235–243, 2012. Vizualizați la: Site-ul editorului | Google Scholar
- A. R. Weale, A. G. Edwards, M. Bailey și P. A. Lear, „Adaptarea intestinală după rezecția intestinală masivă” Jurnal medical postuniversitar, vol. 81, nr. 953, pp. 178–184, 2005. Vizualizare la: Site-ul editorului | Google Scholar
- M. Wasa, Y. Takagi, K. Sando, T. Harada și A. Okada, „Adaptarea intestinală la pacienții pediatrici cu sindromul intestinului scurt” Jurnalul European de Chirurgie Pediatrică, vol. 9, nr. 4, pp. 207–209, 1999. Vizualizare la: Google Scholar
- M. Wasa, Y. Takagi, K. Sando, T. Harada și A. Okada, „Rezultatul pe termen lung al sindromului intestinului scurt la pacienții adulți și copii” Journal of Parenteral and Enteral Nutrition, vol. 23, nr. 5, pp. S110 - S112, 1999. Vizualizare la: Google Scholar
- Y.-J. Fei, Y. Kanai, S. Nussberger și colab., „Clonarea expresiei unui transportor oligopeptidic cuplat la protoni de mamifere” Natură, vol. 368, nr. 6471, pp. 563–566, 1994. Vizualizare la: Site-ul editorului | Google Scholar
- T. R. Ziegler, C. Fernández-Estívariz, L. H. Gu și colab., „Distribuția transportorului de H +/peptidă PepT1 în intestinul uman: expresie reglată în sus în mucoasa colonică a pacienților cu sindromul intestinului scurt” American Journal of Clinical Nutrition, vol. 75, nr. 5, pp. 922–930, 2002. Vizualizare la: Google Scholar
- Rețetă canină Appalachian Valley® de rasă mică cu carne de vânat; Fasole Garbanzo Taste of the Wild®
- O notă despre cantitățile mici de produse animale din produsele alimentare PETA
- Înlocuirea valvei aortice sau mitrale cu Biocor și Biocor Supra - Vizualizare text complet
- Bfabulous Diets Sector 18, Noida - Experiența pacientului pentru Bfabulous Diets Noida
- Dincolo de Balet Gras și Subțire, Scurt și Înalt pentru Oameni