Qiming Yang
1 Ministerul Educației (MOE) Laborator cheie pentru standardizarea medicamentelor chineze și Administrația de stat a medicinei tradiționale chineze (SATCM) Laborator cheie pentru noi resurse și evaluarea calității medicamentelor chineze, Institutul de Materia Medica Chineză, Universitatea din Shanghai de Medicină Tradițională Chineză, Shanghai 201203, China; moc.oohay@mct_gnaysalohcin (Q.Y.); moc.361@msunaru (M.Q.); moc.361@239nuyiqgnot (R.T.); moc.621@ddqmzx (D.W.); moc.621@9128lian (L.D.); moc.361@6002nuyezil (Z.L.)
Meng Qi
1 Ministerul Educației (MOE) Laborator cheie pentru standardizarea medicamentelor chineze și Administrația de stat a medicinei tradiționale chineze (SATCM) Laborator cheie pentru noi resurse și evaluarea calității medicamentelor chineze, Institutul de Materia Medica Chineză, Universitatea din Shanghai de Medicină Tradițională Chineză, Shanghai 201203, China; moc.oohay@mct_gnaysalohcin (Q.Y.); moc.361@msunaru (M.Q.); moc.361@239nuyiqgnot (R.T.); moc.621@ddqmzx (D.W.); moc.621@9128lian (L.D.); moc.361@6002nuyezil (Z.L.)
Renchao Tong
1 Ministerul Educației (MOE) Laborator cheie pentru standardizarea medicamentelor chineze și Administrația de stat a medicinei tradiționale chineze (SATCM) Laborator cheie pentru noi resurse și evaluarea calității medicamentelor chineze, Institutul de Materia Medica Chineză, Universitatea din Shanghai de Medicină Tradițională Chineză, Shanghai 201203, China; moc.oohay@mct_gnaysalohcin (Q.Y.); moc.361@msunaru (M.Q.); moc.361@239nuyiqgnot (R.T.); moc.621@ddqmzx (D.W.); moc.621@9128lian (L.D.); moc.361@6002nuyezil (Z.L.)
Dandan Wang
1 Ministerul Educației (MOE) Laborator cheie pentru standardizarea medicamentelor chineze și Administrația de stat a medicinei tradiționale chineze (SATCM) Laborator cheie pentru noi resurse și evaluarea calității medicamentelor chineze, Institutul de Materia Medica Chineză, Universitatea din Shanghai de Medicină Tradițională Chineză, Shanghai 201203, China; moc.oohay@mct_gnaysalohcin (Q.Y.); moc.361@msunaru (M.Q.); moc.361@239nuyiqgnot (R.T.); moc.621@ddqmzx (D.W.); moc.621@9128lian (L.D.); moc.361@6002nuyezil (Z.L.)
Lily Ding
1 Ministerul Educației (MOE) Laborator cheie pentru standardizarea medicamentelor chineze și Administrația de stat a medicinei tradiționale chineze (SATCM) Laborator cheie pentru noi resurse și evaluarea calității medicamentelor chineze, Institutul de Materia Medica Chineză, Universitatea din Shanghai de Medicină Tradițională Chineză, Shanghai 201203, China; moc.oohay@mct_gnaysalohcin (Q.Y.); moc.361@msunaru (M.Q.); moc.361@239nuyiqgnot (R.T.); moc.621@ddqmzx (D.W.); moc.621@9128lian (L.D.); moc.361@6002nuyezil (Z.L.)
Zeyun Li
1 Ministerul Educației (MOE) Laborator cheie pentru standardizarea medicamentelor chineze și Administrația de stat a medicinei tradiționale chineze (SATCM) Laborator cheie pentru noi resurse și evaluarea calității medicamentelor chineze, Institutul de Materia Medica Chineză, Universitatea din Shanghai de Medicină Tradițională Chineză, Shanghai 201203, China; moc.oohay@mct_gnaysalohcin (Q.Y.); moc.361@msunaru (M.Q.); moc.361@239nuyiqgnot (R.T.); moc.621@ddqmzx (D.W.); moc.621@9128lian (L.D.); moc.361@6002nuyezil (Z.L.)
Cheng Huang
2 Școala de farmacie, Universitatea de Medicină Tradițională Chineză din Shanghai, Shanghai 201203, China; [email protected]
Zhengtao Wang
1 Ministerul Educației (MOE) Laborator cheie pentru standardizarea medicamentelor chineze și Administrația de stat a medicinei tradiționale chineze (SATCM) Laborator cheie pentru noi resurse și evaluarea calității medicamentelor chineze, Institutul de Materia Medica Chineză, Universitatea din Shanghai de Medicină Tradițională Chineză, Shanghai 201203, China; moc.oohay@mct_gnaysalohcin (Q.Y.); moc.361@msunaru (M.Q.); moc.361@239nuyiqgnot (R.T.); moc.621@ddqmzx (D.W.); moc.621@9128lian (L.D.); moc.361@6002nuyezil (Z.L.)
Li Yang
1 Ministerul Educației (MOE) Laborator cheie pentru standardizarea medicamentelor chineze și Administrația de stat a medicinei tradiționale chineze (SATCM) Laborator cheie pentru noi resurse și evaluarea calității medicamentelor chineze, Institutul de Materia Medica Chineză, Universitatea din Shanghai de Medicină Tradițională Chineză, Shanghai 201203, China; moc.oohay@mct_gnaysalohcin (Q.Y.); moc.361@msunaru (M.Q.); moc.361@239nuyiqgnot (R.T.); moc.621@ddqmzx (D.W.); moc.621@9128lian (L.D.); moc.361@6002nuyezil (Z.L.)
Date asociate
Abstract
1. Introducere
Obezitatea, care este cauzată de o combinație de aport excesiv de energie alimentară și lipsa exercițiilor fizice, duce în mod normal la riscuri crescute pentru sănătate ale diabetului de tip 2, dislipidemie, ateroscleroză, hipertensiune, boli cardiovasculare sau anumite tipuri de cancer [1,2,3] . Reducerea consumului de alimente bogate în energie și exercițiile fizice sunt principalele tratamente pentru obezitate [4]. În ultimii ani, utilizarea suplimentelor alimentare a devenit o strategie eficientă pentru prevenirea sau tratarea obezității și a tulburărilor metabolice asociate [5,6]. Medicamentele tradiționale pe bază de plante conțin diferiți compuși activi, cum ar fi polizaharidele, flavonoidele, terpenele, alcaloizii și iridoizii, iar mulți dintre ei prezintă efecte anti-obezitate valabile [7,8,9].
Plantago asiatica L. (patlagina chineză) este un medicament pe bază de plante aparținând genului Plantago și este originar din Asia de Est. Această plantă este utilizată în mod tradițional pentru tratarea bolilor hepatice, a problemelor de stomac și a inflamației sistemului urinar [10,11,12]. Frunzele P. asiatica L. sunt consumate ca legume sau ceai în Japonia și nord-estul Chinei. Semința de P. asiatica L., care este înregistrată ca semen Plantaginis în farmacopeea chineză, este bine cunoscută pentru proprietățile sale diuretice, antipiretice, antitusive, antiflogistice și care facilitează defecarea [13,14]. Rapoarte recente au demonstrat că multe specii de Plantago au exercitat efecte terapeutice asupra obezității, diabetului de tip 2 și tulburărilor lipidice [15,16,17]. În studiile anterioare, un extract de metanol din P. asiatica L. a arătat activitate inhibitoare a glicației și a blocat dezvoltarea complicațiilor diabetice [18]. Polizaharidele din semințele de P. asiatica L. au redus absorbția lipidelor aparente la șoareci prin modularea microbiotei colonului [19,20]. Uleiurile esențiale din P. asiatica L. au exercitat efecte hipolipidemice asupra șoarecilor C57BL/6 [21]. Aceste rapoarte au sugerat că semințele de P. asiatica L. ar putea participa potențial la ameliorarea metabolismului glucozei și a lipidelor și a obezității.
2. Rezultate
2.1. Constituenții chimici ai extractului de semințe Plantago asiatica L. (PSE)
Am determinat compoziția chimică a PSE prin cromatografie lichidă ultra-performantă - spectrometrie de masă (UPLC-MS). În profilul cromatografic al PSE (Figura S1), acidul plantagoguanidinic A și acidul cafeic au fost detectate în modul de scanare a ionizării pozitive, în timp ce acidul genipozidic, plantamajozidul, actozidul și izoactozidul au fost detectate în modul negativ. Vârfurile acestor compuși au fost identificate prin comparație cu timpul de retenție UPLC și spectrele MS ale compușilor standard. Cantitățile relative ale compușilor principali ai PSE, și anume acteozidă, acid geniposidic și acid plantagoguanidinic A, au fost, respectiv, 27,7, 42,3 și 6,83 mg/g PSE, care au fost echivalente cu 4,42, 6,77 și 1,09 mg/g în brut P. asiatica L. semințe.
2.2. Efectele PSE asupra greutății corporale, aportului alimentar și acumulării de lipide a obezilor C57BL/6 obezi induse de dietă cu conținut ridicat de grăsimi (HF)
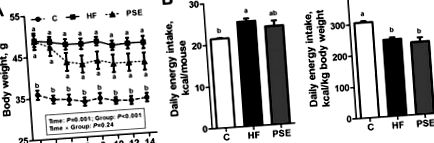
După 16 săptămâni de dietă HF, șoarecii C57BL/6 și-au crescut greutatea corporală cu 39,4% în comparație cu grupul cu diete Chow (p Figura 1 A). S-a detectat o cantitate ușor mai mică de consum absolut de alimente în grupul PSE comparativ cu grupul HF, iar diferența nu a fost semnificativă (p = 0,66); diferența de aport alimentar corectată în funcție de greutatea corporală nu a fost, de asemenea, semnificativă (p = 0,94) (Figura 1 B, C).
Modificări ale greutății corporale (A); aportul mediu de energie pe șoarece (B); și pe kg de greutate corporală (C) a șoarecilor obezi C57BL/6 induse de dietă HF de 16 săptămâni după ce au fost tratați cu PSE timp de două săptămâni. Datele sunt prezentate prin mijloace ± SEM; n = 8 pe grup (A); și n = 10 pe grup (B,C). Greutatea corporală în rândul grupurilor a fost analizată prin măsurători repetate ANOVA cu două căi cu factori subiecți între (grupuri) și în termen de (zile), iar datele privind fiecare zi au fost comparate prin ANOVA multivariat unidirecțional cu testul Bonferroni post hoc. Comparații multiple ale aportului de energie au fost analizate prin ANOVA unidirecțional cu testul Bonferroni post hoc. Mijloace etichetate (B,C); sau înseamnă într-o zi (A) fără o literă comună diferă semnificativ la p b). C, control; HF, bogat în grăsimi; PSE, extract de semințe Plantago asiatica L.
Acumularea remarcabilă de lipide în abdomen a fost afișată cu un raport mai mare al țesutului adipos alb (WAT), adică, greutatea WAT (g) per greutate corporală (100 g), în grupul HF decât în grupul dieta Chow (p Figura 2 A, B ). În examinarea patologică cu hematoxilină și eozină (H&E) și colorare roșie ulei O (Figura 3), tratamentul PSE a atenuat steatoza macrovesiculară indusă de dieta HF. După tratamentul cu PSE timp de două săptămâni, diametrele adipocitelor albe au scăzut de la 124 ± 3,52 μm la 93,0 ± 4,44 μm (p Figura 2 C, D).
Tomografiile computerizate scanează la 8 mm deasupra vârfului osului iliac (A); raporturi WAT abdominale (B); diametrele adipocitelor albe (C); și adipocite maro (D) a șoarecilor obezi C57BL/6 induse de dietă HF de 16 săptămâni după tratamentul cu PSE timp de două săptămâni. Datele sunt prezentate ca mijloace ± SEM; n = 4 pe grup (B); și n = 8 pe grup (C,D). ANOVA unidirecțională cu testul Bonferroni post hoc a fost utilizat pentru analiza statistică. Mijloacele etichetate fără o literă comună diferă semnificativ la p b> c). WAT, țesut adipos alb.
Analiza histologică a ficatului, WAT și BAT după două săptămâni de tratament PSE la șoareci obezi C57BL/6 induse de dietă HF de 16 săptămâni. Secțiunile de țesut hepatic au fost colorate cu roșu ulei O sau H&E (× 200) pentru a observa conținutul de lipide hepatice. WAT și BAT au fost colorate cu H&E (× 200) pentru a observa dimensiunea adipocitelor. BAT, țesut adipos maro; H&E, hematoxilină și eozină. Bara de scalare: 100 µm.
Așa cum se arată în Figura 4, colesterolul total seric (TC) (p = 0,016), trigliceridele (TG) (p b> c). FFA, acid gras liber; HDL-c, colesterol lipoproteic de înaltă densitate; LDL-c, colesterol lipoproteic cu densitate mică; TC, colesterol total; TG, trigliceride.
2.3. Efectele PSE asupra homeostaziei glucozei a șoarecilor obezi C57BL/6 induse de dietă HF
Glicemia în jeun a șoarecilor din grupul HF a fost crescută la 12,8 ± 0,511 mmol/L și cu 43,6% mai mare decât în grupul dieta Chow (p Figura 5 A). După injecțiile cu glucoză în testul de toleranță la glucoză (GTT), concentrațiile de glucoză din sânge din grupul PSE au scăzut semnificativ la 30 min (p = 0,001) și 60 min (p = 0,002) comparativ cu cele din grupul HF (Figura 5 B). Cu toate acestea, grupul PSE nu a prezentat modificări semnificative ale concentrațiilor de glucoză din sânge după injecțiile cu insulină (Figura 5 D). Zonele de sub curbă (ASC) ale GTT-urilor și testelor de toleranță la insulină (ITT-uri) de la 0 la 120 minute în grupurile Chow diet, HF și PSE au prezentat rezultate similare (Figura 5 C, E). Între timp, concentrațiile plasmatice ale insulinei serice au crescut semnificativ la șoarecii obezi induși în dietă HF (p = 0,004), în timp ce nu au scăzut prin administrarea PSE (p = 1,00). Au fost de asemenea calculați indicii HOMA pentru evaluarea rezistenței la insulină (HOMA-IR), sensibilitatea (HOMA-IS) și funcția celulei beta (HOMA-β) [22]. Nu s-au afișat diferențe semnificative ale indicilor HOMA între grupurile HF și PSE (HOMA-IR, p = 1,00; HOMA-IS, p = 1,00; HOMA-β, p = 0,25) așa cum se arată în Figura S2. Rezultatele de mai sus au sugerat că PSE ar putea reduce hiperglicemia indusă de HF, dar nu și hiperinsulinemia.
- Înainte sau după antrenament când trebuie să luați Whey Protein Onnit Academy
- Sursă Ceai de slăbire Ceai de plante Ceai de flori de Calendula pe
- Călătoria mea de pierdere în greutate Cum am slăbit 20 kg; L-a ținut; Healthy Foodie Creations
- Ulei oral care extrage revista Registered Dental Hygienist (RDH)
- Șapte rețete islandeze ușoare pentru începători curajoși Arla UK