Introducere
S-a crezut că dietele ketogenice cu conținut scăzut de carbohidrați și conținut ridicat de grăsimi, urmate pe termen lung, vor încurca hormonii. Criticii nutriției cu conținut scăzut de carbohidrați susțin că dietele cetoase scad activitatea tiroidiană, scad nivelul de testosteron și afectează alți hormoni din corp. Care sunt dovezile?
Și ce zici de deficitul global masiv de iod, indiferent de tipul dietei? Nu este mai indicativ faptul că există probleme cu tiroida și că starea generală de sănătate este slabă?
În cadrul experimentului meu ceto n = 1, care se desfășoară de mai bine de 10 luni, am reușit să-mi dublu nivelul de testosteron, de la
400 ng/dL la 843 ng/dL cu intervenții dietetice și alte intervenții asupra stilului de viață.
Mi-am modificat nivelul de testosteron între mai 2014 și iulie 2014. Bănuiesc că înainte de a începe nutriția ceto la sfârșitul lunii septembrie. 2013, nivelurile mele de T au fost sub 200 ng/dL. Și am câteva motive să cred așa, dar voi vorbi despre asta în Testosteronul R (x), pe care îl voi elibera în viitorul apropiat.
Înapoi la tiroidă
Dacă sunteți o ființă umană sănătoasă și consumați o dietă eucalorică (în care mâncați alimente pentru a vă satisface consumul zilnic de energie), hormonii tiroidieni T3 și T4 vor arăta valori în intervalul normal de 80-170 ng/dL pentru T3 și 4,5 -12,5 ug/dL pentru T4. Acest lucru se întâmplă indiferent de dieta pe care o consumați.
Acum să ne concentrăm pe dieta ketogenică și/sau alte variante ale dietelor cu conținut scăzut de carbohidrați. Dacă mențineți o stare de cetoză pe termen lung, cel mai probabil veți reduce aportul caloric, deoarece unul dintre cele mai mari beneficii ale acestei abordări este protocolul „fără foame, fără pofte”.
Dacă ești ca mine, poți petrece zile fără să mănânci. (Când sunt implicat în proiecte obositoare, sunt complet atractiv și uit de mâncare. Asta nu s-a întâmplat când nu eram în cetoză).
Deci, nu îmi îndeplinesc întotdeauna aportul caloric pentru o zi.
Ce legătură au toate astea cu hormonii tiroidieni?
Să vedem câteva posibile corelații între activitatea tiroidiană, aportul de alimente și aportul de carbohidrați.
Literatura - Variabilitatea concluziilor
Pentru a evalua efectul restricției calorice și al compoziției dietetice asupra circulației T3 și rT3, subiecții obezi au fost studiați după 7-18 zile de post total și în timp ce pe diete hipocalorice randomizate (800 kcal) în care conținutul de carbohidrați a fost variat pentru a furniza de la 0 la 100 % calorii. După cum era anticipat, postul total a dus la o reducere de 53% a T3 seric în asociere cu o creștere reciprocă de 58% a rT3. Subiecții care au primit diete hipocalorice fără carbohidrați timp de două săptămâni au demonstrat o scădere similară cu 47% a serului T3, dar nu a existat nicio modificare semnificativă a rT3 în timp.
În schimb, aceiași subiecți care au primit diete izocalorice conținând cel puțin 50 g de carbohidrați nu au prezentat modificări semnificative nici în concentrația T3, nici în rT3. Scăderea serului T3 în timpul dietei fără carbohidrați s-a corelat semnificativ cu glicemia și cetonele, dar nu a existat nicio corelație cu insulina sau glucagonul.
Concluzionăm că carbohidrații dietetici sunt un factor important de reglementare în producția de T3 la om. În schimb, rT3, concentrația nu este afectată semnificativ de modificările carbohidraților din dietă. Datele noastre sugerează că creșterea rT3 serică în timpul foametei poate fi legată de o restricție calorică mai severă decât cea cauzată de dieta de 800 kcal.
T3 mai mic indică întotdeauna starea bolii? Aș spune că nu. T3 este ajustat în funcție de nevoile corpului și este implicat în mecanismul de feedback care se află între hipotalamus (în special reglarea aportului alimentar) și tiroida.
Dietele izocalorice care conțin cel puțin 50g carbohidrați sunt diete cu același număr de calorii, adică 800 kcals (în acest caz). Deci, T3 nu are o corelație puternică cu dietele cu conținut scăzut de calorii, ci cu cantitatea de carbohidrați din dietă? Dar studiul longitudinal al îmbătrânirii din Baltimore? Vom vedea despre asta mai târziu.
Pentru a evalua efectul înfometării și al alimentării asupra concentrațiilor serice de hormoni tiroidieni și tirotropină (TSH), 45 de subiecți obezi au fost studiați după 4 zile de post și după realimentare cu diete cu compoziție variabilă. Toți subiecții au prezentat o creștere atât a tiroxinei totale serice, cât și a tiroxinei libere (T4) și a scăderii triiodotironinei totale și a serului liber (T3) după post.
Aceste schimbări au fost mai izbitoare la bărbați decât la femei. Serul T3 a scăzut în timpul postului chiar și atunci când subiecților li s-a administrat L-T4 oral, dar nu și când li s-a administrat L-T3 oral. După post, T3 inversă serică (rT3) a crescut, TSH seric a scăzut și răspunsul TSH la hormonul care eliberează tirotropina (TRH) a fost tocit. Realimentarea fie cu o dietă mixtă (n = 22), fie cu o dietă cu carbohidrați (n = 8) a determinat modificările induse de post ale serului T3, T4, rT3 și TSH să revină la valorile de control. În schimb, alimentarea cu proteine (n = 6) nu a determinat o creștere a T3 seric sau a TSH seric la subiecții la jeun, în timp ce a provocat o scădere a rT3 seric către valoarea bazală.
Datele actuale sugerează că: (1) carbohidrații dietetici sunt un factor important în inversarea căderii serului T3 cauzată de post; (2) producția de rT3 nu este la fel de dependentă de carbohidrați ca cea a T3; (3) bărbații prezintă modificări mai semnificative ale concentrațiilor serice de hormoni tiroidieni în timpul postului decât femeile și (4) absorbția T3 nu este modificată în timpul postului.
Nu sunt de acord cu concluzia lor, dar nu par să empatizez cu urgența lor de a ridica T3. Poate fi doar interpretarea mea, dar nu cred că T3 scăzut este rău, atâta timp cât funcția tiroidiană este normală și atât timp cât semnalizarea TSH -> TRH și concentrația T4 funcționează corect.
Știm din manualele de biochimie că T3 funcționează ca un catalizator, crescând sau scăzând viteza cu care au loc reacțiile chimice pe tot corpul. Nu este normal că un aport mai mic sau deloc de alimente duce la niveluri mai scăzute de T3, atâta timp cât orice altceva se află în limite normale?
Nivelurile serice de T3 și T4 sunt interconectate deoarece T4 (tiroxina) curge în concentrații mult mai mari în sânge și este transformat în T3 (forma activă a hormonului tiroidian) ori de câte ori este necesar. În stările de post, deoarece nu este nevoie de T3 ridicat, vor exista niveluri mai ridicate de T4 circulant (deoarece nu este convertit).
Răspunsurile metabolice în timpul unei diete cu conținut scăzut de calorii, compuse din 50% glucoză și 50% proteine, au fost studiate la 18 subiecți cu obezitate severă (greutăți relative 131-205%) timp de 28 de zile. În ultimele 14 zile (perioada 2) opt subiecți (Gp B) au servit drept martori, în timp ce ceilalți zece subiecți (Gp A) în starea T3 scăzută au fost tratați cu supliment de triiodotironină (50 micrograme, de 3 ori pe zi).
În timpul primelor 14 zile (perioada 1) s-a dezvoltat o stare scăzută T3-înaltă rT3; a existat o relație inversă între scăderea absolută a concentrațiilor plasmatice de T3 și echilibrul negativ cumulativ al azotului, precum și concentrațiile de acid beta-hidroxibutirat (BOHB) în perioada de semi-înfometare, indicând un efect de economisire a proteinelor și combustibilului Starea T3.
Pierderea în greutate în perioada de semi-înfometare a fost egală în ambele grupuri; în timpul tratamentului cu T3, rata pierderii în greutate a fost semnificativă statistic (Gp A 6,1 +/- 0,3 kg față de Gp B 4,2 +/- 0,2 kg, P mai puțin de 0,001). În grupul martor a existat un echilibru susținut al azotului după trei săptămâni; în Gp A pierderile de azot au crescut semnificativ în timpul tratamentului cu T3. Comparativ cu grupul martor, în medie s-au pierdut în continuare 45,4 g azot suplimentar, echivalent cu 1,4 kg de țesut fără grăsimi.
Astfel, 74 la sută din pierderea în greutate suplimentară în grupul tratat cu T3 ar putea fi cauzată de pierderea țesutului fără grăsimi. În timpul perioadei de tratament T3 nu s-au produs modificări detectabile în ceea ce privește concentrațiile plasmatice ale trigliceridelor și acizilor grași fără plasmă (FFA); concentrațiile plasmatice de acid BOHB au scăzut semnificativ în comparație cu grupul martor. Concentrațiile plasmatice de glucoză și raportul insulină imunoreactivă (IRI)/glucoză au crescut în Gp A în perioada de tratament T3, reflectând o stare de rezistență la insulină în ceea ce privește utilizarea glucozei.
Rezultatele noastre justifică concluzia că pare să nu existe un loc pentru T3 ca adjuvant la dietă, deoarece îmbunătățește în principal pierderea de proteine corporale și doar într-o mică măsură pierderea de grăsime corporală.
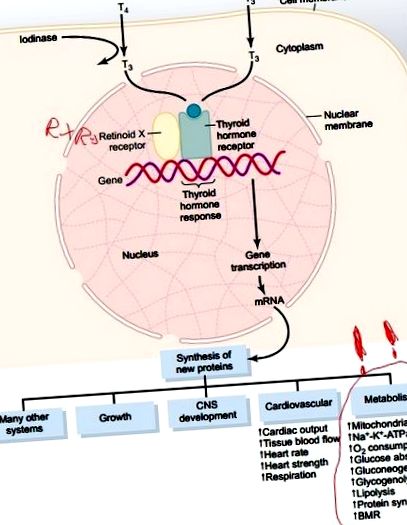
Mulțumiri speciale lui Amber de la Paleohacks pentru sugestia acestor articole. T3, după cum sa explicat anterior, accelerează procesele în întregul corp. Crește utilizarea glucozei, precum și a acizilor grași. Cu toate acestea, acolo unde glucoza nu este disponibilă, aceasta va promova gluconeogeneza prin descompunerea țesutului slab (vezi prima imagine). Nu ar fi nenatural să se completeze cu T3 pentru niveluri mai mici de T3 în regimuri cu restricții calorice.
Conținutul de carbohidrați din dietă este un factor major care determină reglarea endocrină și metabolică. Scopul acestui studiu a fost de a evalua relația dintre nivelurile hormonilor tiroidieni și parametrii metabolici în timpul lipsei eucalorice de carbohidrați.
Am măsurat nivelurile hormonilor tiroidieni, consumul de energie în repaus (prin calorimetrie indirectă) și excreția de azot urinar la șase bărbați sănătoși după 11 zile de trei diete izocalorice conținând 15% din echivalenți energetici ca proteine și 85%, 44% și 2% ca carbohidrați.
Spre deosebire de dietele ridicate și intermediare cu carbohidrați, privarea de carbohidrați a scăzut valorile plasmatice ale T3 (1 · 78 ± 0 · 09 și 1 · 71 ± 0 · 07 vs. 1 · 33 ± 0 · 05 nmol/l, respectiv, P TEE inferior
T3 mai mare în dieta bogată în carbohidrați => TEE mai mare
Există o corelație între carbohidrați și nivelurile T3, dar un TEE mai mare poate produce mai multe ROS (specii reactive de oxigen). Cu toate acestea, dieta bogată în grăsimi, chiar și cu TEE mai scăzută, duce la o scădere mai mare în greutate. Este posibil ca subiecții să nu se fi putut adapta la dietă din cauza duratei scurte de doar câteva zile. Mulți dintre ei au raportat greață și letargie (posibil efecte ale adaptării la ceto).
Douăsprezece femei obeze au fost studiate pentru a determina efectele combinației unui program de exerciții aerobice fie cu o dietă bogată în carbohidrați (HC) foarte slab calorică (VLCD), fie cu o dietă VLCD scăzută în carbohidrați (LC) asupra ratei metabolice de odihnă (RMR), tiroxină serică (T4), 3,5,3'-triiodotironină (T3) și 3,5,3'-triiodotironină (rT3). Răspunsul acestor parametri a fost examinat și atunci când subiecții au trecut de la VLCD la o dietă hipocalorică mixtă. După o perioadă de întreținere, subiecții au consumat unul dintre cele două VLCD-uri timp de 28 de zile.
În plus, toți subiecții au participat la sesiuni de exerciții submaximale de trei ori pe săptămână la 60% din capacitatea aerobă maximă. În urma tratamentelor cu VLCD, participanții au consumat o dietă mixtă de 1.000 kcal în timp ce continuau programul de exerciții timp de o săptămână. Măsurătorile RMR, T4, T3 și rT3 au fost făcute săptămânal. Greutatea a scăzut semnificativ mai mult pentru LC decât HC. Serul T4 nu a fost afectat semnificativ în timpul VLCD. Deși T3 seric a scăzut în timpul VLCD pentru ambele grupuri, scăderea a avut loc mai repede și la o magnitudine mai mare în LC (34,6% scădere medie) decât HC (17,9% scădere medie).
RT3 seric a crescut în mod similar pentru fiecare tratament până în prima săptămână a VLCD. Serul T3 și rT3 din ambele grupuri au revenit la concentrațiile inițiale după o săptămână din dieta de 1.000 kcal. Ambele grupuri au prezentat scăderi progresive similare ale RMR în timpul tratamentului (12,4% pentru LC și 20,8% pentru HC), dar valorile nu au fost semnificativ mai mici decât valoarea inițială până în săptămâna 3 a VLCD. Astfel, deși conținutul de carbohidrați din dietă a avut o influență asupra magnitudinii căderii serului T3, RMR a scăzut în mod similar pentru ambele tratamente dietetice.
Acest studiu arată o corelație între T3 și conținutul de carbohidrați, precum și T3 și restricția calorică. Când urmează o dietă bogată în carbohidrați, subiecții prezintă niveluri mai scăzute de T3, dar nu la fel de scăzute ca cele care urmează o dietă săracă în carbohidrați, consolidând astfel corelația dintre aportul de carbohidrați și nivelurile de T3. Cu toate acestea, acest lucru nu înseamnă încă că nivelurile mai mici de T3 sunt semnul unei stări de boală sau că ceva nu este în regulă în organism.
Îmbătrânirea și nivelurile tiroidiene
CONTEXT:
Restricția calorică (CR) întârzie îmbătrânirea la mamifere. S-a emis ipoteza că o reducere a hormonului T (3) poate crește durata de viață prin conservarea energiei și reducerea producției de radicali liberi.
OBIECTIV:
Obiectivul studiului a fost de a evalua relația dintre RC pe termen lung cu aport adecvat de proteine și micronutrienți asupra funcției tiroidiene la bărbați și femei adulți, sănătoși, cu greutate slabă.
PROIECTARE, CONFIGURARE ȘI PARTICIPANȚI:
În acest studiu, hormonii tiroidieni serici au fost evaluați la 28 de bărbați și femei (vârstă medie, 52 +/- 12 ani) care consumau o dietă CR pentru 3-15 ani (6 +/- 3 ani), 28 de vârstă și sex sedentar (WD) și 28 de subiecți care exercită exerciții corporale (EX) care consumă diete occidentale.
MĂSURI PRINCIPALE DE REZULTAT:
Concentrațiile serice totale și libere T (4), totală și liberă T (3), T inversă (3) și concentrațiile de TSH au fost principalele măsuri de rezultat.
REZULTATE:
Aportul de energie a fost mai mic în grupul CR (1779 +/- 355 kcal/zi) decât grupurile WD (2433 +/- 502 kcal/zi) și EX (2811 +/- 711 kcal/zi) (P mai mare T3) și prezintă, de asemenea, corelație între aportul caloric și nivelurile de T3. Subiecții care restricționează caloriile (dieta hipocalorică) au niveluri T3 circulante mai mici, indiferent de tipul de partiționare a macronutrienților.
O glandă tiroidă hiperactivă poate accelera metabolismul între 60% și 100%, potrivit lui Guyton.
Lipsa completă a secreției tiroidiene determină, de obicei, scăderea ratei metabolice bazale cu 40-50% sub normal, iar excesele extreme de secreție tiroidiană pot crește rata metabolică bazală la 60-100% peste normal.
Deși rata sintezei proteinelor este crescută, în același timp, rata catabolismului proteinelor este, de asemenea, crescută. Rata de creștere a tinerilor este foarte accelerată. Procesele mentale sunt excitate și activitățile majorității celorlalte glande endocrine sunt crescute.
Postul intermitent va scădea cel mai probabil nivelul T3, dar nu ar trebui să afecteze nivelurile TSH și nivelurile T4. Dacă acest lucru ar fi adevărat, toți oamenii care postesc ar suferi de hipotiroidism și mulți dintre noi ar avea gușe.
Aș vrea să atrag atenția asupra consumului de iod. Fără un aport adecvat de iod, tiroida dvs. nu poate funcționa normal și acesta este cazul în care ați vedea niveluri mai mici de T3, precum și T4 mai mic și TSH.
Iodul este foarte important deoarece este necesar pentru a produce hormoni tiroidieni (T1, T2, T3, T4). Iodul se leagă de tirozină pentru a produce acești hormoni.
Pentru a preveni hipotiroidismul, gușa și nanismul, țările din întreaga lume au adăugat iod la sare (sare iodată).
Chiar dacă aceasta nu este cea mai eficientă formă de a obține iod în organism, așa cum Dr. Brownstein crede că doar 10% din iodul din sarea iodată este absorbit, protocolul sării iodate a reușit să eradice epidemia tulburărilor legate de hipotiroidie timp de câteva decenii.
Cu toate acestea, este posibil să fim pe o curbă înclinată în jos, deoarece ne temem să consumăm sare. Suntem constant bombardați de un mesaj pentru a reduce aportul de zahăr, sare și grăsimi.
(Din nou) Sarea de masă (chiar iodată) poate să nu fie cea mai bună alegere pentru aportul de iod. Aș mânca în schimb fructe de mare (alge, alge), deoarece este bogat în acest nutrient extrem de important. Dacă acest lucru nu este posibil, aș completa cu extract de alge sau alte produse care oferă o sursă bună de iod.
Personal nu mi-aș face griji pentru niveluri mai mici de T3 în dietele ketogenice bine formulate și/sau atunci când urmez protocoalele de post/IF, atât timp cât TSH și T4 se încadrează în limite normale. Din nou, pentru a mă asigura că funcționează bine glanda tiroidă, aș asigura un aport adecvat de iod.
După cum am spus, voi stabili un protocol tiroidian complet (Rx), precum și un protocol de testosteron (Rx). Cu toate acestea, efectuez în continuare activități de cercetare și experimentare pe amândouă și vă voi anunța imediat ce le termin.
Editare ulterioară: T- (Rx) este în funcțiune. Urmând linkul ...
Aceasta a fost o postare foarte lungă și, dacă ați reușit până acum, vă rugăm să ne împărtășiți părerile în oricare dintre secțiunile de comentarii de mai jos.
Sugestie: Puteți verifica la fel de bine studiile mai noi în Lecturi suplimentare secțiune.
- Bine ați venit pe blogul Nutrition facts
- Efectul pierderii în greutate asupra nivelurilor hormonilor anti-Müllerian la femeile supraponderale și obeze cu
- Palatul kurd - Partea 2 - KEMSA - Blog nutrițional
- Sfaturi pentru numirea practicii dvs. nutriționale; Blogul oficial Kalix
- Blogul Sunshine Vitamin Invigorate Nutrition - Kirsty Fairbairn