Ce este un raport de patologie?
Un patolog este un medic specializat în diagnosticarea bolilor prin examinarea țesuturilor din corp. Probabil că nu vă veți întâlni niciodată cu patologul, dar probele de țesut de colon, îndepărtate în timpul intervenției chirurgicale sau biopsiei, le vor fi trimise spre examinare. Patologul pregătește un raport al descoperirilor lor. Acesta se numește raportul de patologie. Acest raport conține informații importante despre tumoră și ajută la orientarea deciziilor de tratament. Ar trebui să solicitați o copie a acestui raport și să îl păstrați în fișierele dvs. personale.
Ce veți găsi pe un raport de patologie?
Conținutul real al unui raport poate varia în funcție de locul în care este completat. Raportul este împărțit în câteva secțiuni și poate include:
- Informații demografice despre pacient: numele, data nașterii, numărul dosarului medical, diagnosticul presupus (dacă este cunoscut), numele medicului.
- Descrierea procedurii și modul/de unde a fost obținut specimenul.
- Descriere brută: cum arată specimenul cu ochiul liber. Aceasta poate include greutatea, culoarea și dimensiunea țesutului.
- Descriere microscopică: ceea ce s-a văzut la microscop.
- Tipul de celule tumorale: ce tip de celule alcătuiesc cancerul? Adenocarcinomul este cel mai frecvent tip de cancer de colon.
- Grad histologic: descrie cât de diferite arată celulele în comparație cu celulele normale.
- Invazie limfovasculară: dacă celulele canceroase au pătruns în sistemul limfatic sau sanguin.
- Etapa T: descrie dimensiunea tumorii și cât de departe invadează tumora în peretele colonului.
- Ganglioni limfatici: aceasta indică câte ganglioni limfatici au fost testați și câte au celule canceroase în ele.
- Marje: patologul se uită la marginile eșantionului pentru a fi sigur că nu există celule canceroase lângă margine sau care se extind dincolo.
- Diagnostic: pe baza tuturor informațiilor de mai sus, patologul dă un diagnostic.
Pentru a vă ajuta să înțelegeți mai bine raportul, să parcurgem aceste secțiuni în mod individual.
Descrierea brută
În general, acest lucru nu este atât de important pentru pacient. Este o descriere a probei primite de patolog și a ceea ce văd cu ochiul liber. Într-o biopsie, specimenul este probabil o mică bucată de țesut nedescriptibil, caz în care patologul poate descrie culoarea, forma, senzația și dimensiunea țesutului. După o intervenție chirurgicală pentru cancer, mai multe organe sau țesuturi pot fi prezentate și descrise în raport. Aceasta poate include dimensiunea, culoarea și greutatea. De exemplu, un specimen de colon dintr-o colectomie poate fi descris ca:
„Specimenul # 1 este etichetat„ colon ”și constă dintr-un segment de intestin care măsoară 13 cm lungime după fixare. Specimenul este înconjurat de o cantitate moderată de grăsime pericolonică. Restul mucoasei este extrem de remarcabil. "
Acest lucru ne spune că specimenul era o bucată de colon lungă de 13 cm, cu o tumoare situată la 3 cm de un capăt. Acest lucru nu este foarte util în determinarea etapei sau a tratamentului, așa că să trecem la secțiunea următoare.
Descriere microscopică
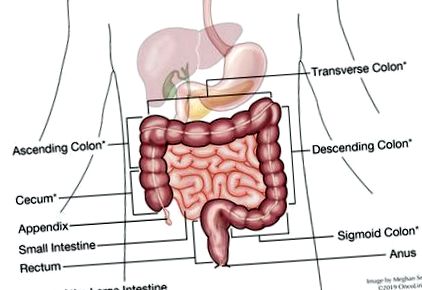
Aceasta este carnea raportului, dar trebuie să știm mai multe despre colon pentru a înțelege această parte a raportului. Colonul sau intestinul gros este un tub care are aproximativ 5 până la 6 picioare în lungime; primele 5 picioare alcătuiesc colonul, care apoi se conectează la aproximativ 6 inci de rect și, în cele din urmă, se termină cu anusul. Colonul este alcătuit din mai multe secțiuni. Raportul dvs. poate specifica în ce secțiune a fost localizată tumora. Aceste secțiuni se numesc cec, ascendent, transvers, descendent și colon sigmoid, rect și anus (vezi diagrama). Flexurile splenice și hepatice sunt zone în care colonul se îndoaie (sau se flexează), numite după organele în care se află.
Colonul, care are forma unui tub, este alcătuit din mai multe straturi, începând cu stratul cel mai interior, mucoasa (care este formată din epiteliu), apoi lamina propria și mucoasa musculară. Acesta este înconjurat de submucoasa, care este înconjurată de două straturi de mușchi (sau muscularis) și, în cele din urmă, stratul seros, care este stratul exterior al tubului. Exteriorul colonului este acoperit cu un strat de grăsime, numit și țesut adipos, care conține ganglioni limfatici și vase de sânge care hrănesc țesutul colonului.
Tipul celulei tumorale
Tipul de tumoare de colon descrie celulele din care apare tumora. Adenocarcinomul este cel mai frecvent tip, reprezentând 95-98% din cancerele de colon. Un adenocarcinom apare din celulele glandulare care acoperă interiorul colonului. Două subtipuri de adenocarcinom sunt inelul cu sigiliu și mucinos, ambele fiind denumite pentru modul în care celulele arată la microscop. Celelalte 2-5% dintre cancerele găsite în colon sunt limfoamele, tumorile stromale gastrointestinale (GIST) și tumorile carcinoide, care nu sunt discutate în acest articol.
Dacă a fost eliminat un polip, această secțiune va descrie tipul de polip. Un polip de colon este o creștere benignă care, în timp, se poate transforma în cancer. Din acest motiv, acestea sunt îndepărtate în timpul colonoscopiei și pot fi trimise la patolog pentru a stabili ce tip de polip este. Există mai multe tipuri de polipi care pot fi găsiți în colon:
- Adenom tubular (numit și polip adenomatos): acesta reprezintă 70% din polipii găsiți în colon și poate evolua în cancer, dar acest lucru se întâmplă de-a lungul mai multor ani. Dacă se găsesc devreme, pot fi îndepărtate în timpul colonoscopiei.
- Adenom vilos: acesta reprezintă 15% din polipii găsiți în colon. Acest tip de polip are cel mai mare risc de a se transforma în cancer. În unele cazuri, acestea pot fi îndepărtate în timpul colonoscopiei, dar în alte cazuri este necesară intervenția chirurgicală.
- Polipi hiperplastici și inflamatori (sau pseudopolipi): este puțin probabil ca aceste două tipuri de polipi să se transforme într-un cancer.
În plus, polipii de colon vin sub două forme, numite pedunculate și sesile. Polipii pedunculați cresc pe o tulpină și arată ca o ciupercă mică, care poate fi îndepărtată cu ușurință în timpul colonoscopiei. Tipul sesil de polip este plat și crește pe peretele colonului. Acestea sunt mult mai dificil de îndepărtat și pot necesita intervenții chirurgicale pentru îndepărtarea întregului polip.
Grad histologic
Pe măsură ce celulele normale se dezvoltă, acestea se „diferențiază” pentru a deveni un tip specific de celule. Gradul histologic descrie cât de mult seamănă celulele tumorale cu celulele normale. Cu cât o celulă tumorală arată mai mult ca o celulă normală, cu atât este mai bine diferențiată. Pe de altă parte, cu cât mai multe celule nu arată ca celule normale (de grad superior), cu atât sunt mai agresive. Se pot dezvolta și răspândi mai repede. Gradul tumoral histologic este defalcat după cum urmează:
- GX: Gradul tumorii nu poate fi identificat.
- G1: Bine diferențiat. Celulele apar cel mai normal.
- G2: Moderat diferențiat. Celulele apar oarecum ca celulele normale.
- G3: slab diferențiat. Celulele arată mai puțin ca celulele normale.
- G4: Nediferențiat. Celulele par cele mai anormale și abia arată ca celulele normale.
Invazie limfovasculară
Când patologul examinează tumoarea și țesutul înconjurător de care dispun, se uită la micile vase de sânge și la drenajul limfatic pentru a vedea dacă celule tumorale le-au invadat. Acest lucru este diferit de ganglionii limfatici și s-ar raporta dacă se observă sau nu invazie limfovasculară. Prezența acesteia poate fi un semn al unei tumori mai agresive sau mai avansate.
T Etapa/Adâncimea invaziei
O tumoare care nu a invadat țesuturile din jur este uneori numită „in situ”, în timp ce tumorile care au pătruns în țesuturile din jur sunt numite invazive. Stadiul T este clasificat ca Tx (tumora nu poate fi măsurată), T0 (fără dovezi de tumoră), T1 (celulele canceroase se găsesc numai în țesutul superficial, adesea numit cancer in-situ sau pre-cancer), T1, T2, T3, T4 descrieți tumora în funcție de mărime și dacă s-a răspândit în țesuturile și structurile înconjurătoare. Câteva exemple includ:
- "Biopsia arată implicarea lamelei proprii mucoasei de către glandele neoplazice. Submucoasa nu este implicată." Această tumoare invadează doar stratul cel mai interior al colonului.
- "Tumora invadeaza prin muscularis propria dar nu in tesutul adipos pericolonic. Suprafata seroasa nu este implicata." Această tumoare invadează stratul muscular, dar nu invadează seroza (stratul exterior al colonului) sau grăsimea din jur.
- "Tumora este invaziva prin muscularis propria in grasimea pericolonica." Această tumoare a pătruns prin peretele colonului și în grăsimea din jur.
Noduli limfatici
Sistemul limfatic este în esență „sistemul de menaj” al corpului. Este o rețea de vase (tuburi) care leagă ganglionii limfatici. Aceste noduri pot varia în dimensiune, dar în mod normal au o lățime de până la aproximativ 2 centimetri. Acestea conțin celule care elimină bacteriile și alte resturi străine din organism. Limfa este un lichid apos care curge între celulele din corp, ridicând resturi străine și ducându-le în ganglionul limfatic pentru filtrare și, în cele din urmă, eliminare de către ficat.
Celulele canceroase folosesc sistemul limfatic ca prim pas pentru a călători în alte zone ale corpului. În timpul unei intervenții chirurgicale pentru cancerul de colon, numeroși ganglioni limfatici sunt îndepărtați și verificați prezența celulelor canceroase. Acest lucru va fi raportat ca număr de ganglioni limfatici care conțineau celule canceroase și câte au fost examinate. De exemplu, raportul ar putea indica „cincisprezece ganglioni limfatici benigni (0/15)” sau „tumoare observată la șaisprezece din cele douăzeci de ganglioni limfatici (16/20)”.
Într-o intervenție chirurgicală pentru cancerul de colon, cu cât mai mulți ganglioni limfatici sunt eliminați, cu atât mai sigur puteți fi că nu sunt implicați ganglioni limfatici. Nu este neobișnuit să fie îndepărtați până la 30 de ganglioni limfatici în timpul unei intervenții chirurgicale de cancer de colon. Acest lucru este diferit de multe alte tipuri de cancer, unde sunt îndepărtați mult mai puține noduri.
Margini
Aceasta este zona de la marginea specimenului care a fost trimis. Atunci când efectuează o intervenție chirurgicală pentru cancer, chirurgul încearcă să îndepărteze întreaga tumoră și unele țesuturi normale care o înconjoară. Această zonă a „țesutului normal” este importantă deoarece orice celule canceroase rătăcite pot fi incluse în aceasta. Dacă marginea (sau marginea) conține o tumoare, este posibil să fi rămas celule canceroase. Scopul operației este de a obține o „marjă clară”, adică liberă de orice celule canceroase.
Punând totul împreună
Toate aceste piese sunt utilizate pentru a determina stadiul cancerului și ce tratament este necesar. Înțelegând elementele de bază ale raportului, veți putea discuta mai bine opțiunile de tratament cu echipa dvs. de asistență medicală. Sistemul de stadializare cel mai frecvent utilizat pentru cancerul de colon este sistemul de stadializare al Comitetului mixt american pentru cancer (AJCC). Acest sistem utilizează extinderea tumorii primare (T0-4), absența sau prezența cancerului în ganglionii limfatici (N0-2) și existența metastazelor (M0 sau 1) pentru a atribui un rating TNM, care corespunde un stagiu. Sistemul de stadializare este destul de complex. Puteți vedea stadializarea completă a TNM pentru cancerul de colon în articolul OncoLink All About Cancer Article.
Marcatori moleculari pentru a oferi îndrumări suplimentare
Un marker molecular este ceva care se găsește în sânge, țesuturi sau alt fluid corporal, care este un semn al unui proces, afecțiune sau boală normală sau anormală. Există substanțe în unele tumori care pot măsura probabilitatea recurenței (marker prognostic) sau pot prezice un răspuns la chimioterapie (marker predictiv). Doi markeri moleculari găsiți în cancerele de colon au atras atenție în ultimii ani; „instabilitate microsatelit” și „18q pierderea heterozigoității”.
Instabilitate microsatelit
ADN-ul microsatelit este format din secvențe de nucleotide, repetate de mai multe ori și legate între ele, care se găsesc în toate genele umane. Testarea moleculară poate identifica instabilitatea sau erorile în ADN-ul microsatelit al tumorilor, cum ar fi o modificare a numărului de secvențe repetate; aceasta se numește instabilitate microsatelită (MSI). MSI este o modalitate de a măsura o deficiență de reparare a nepotrivirii (MMR) în ADN-ul tumorii. Un deficit de MMR are ca rezultat o creștere a mutațiilor din celulele colonului, care contribuie parțial la dezvoltarea cancerului de colon.
Există două motive pentru a testa cancerul colorectal pentru MSI. Primul este identificarea celor cu risc de cancer ereditar non-polipozic ereditar (HNPCC). Al doilea motiv pentru testarea MSI este că cunoașterea unui cancer colorectal în stadiu incipient are MSI poate schimba modul în care este tratat.
HPNCC este o afecțiune ereditară care crește riscul unui purtător pentru alte tipuri de cancer, inclusiv endometrial, ovarian, stomac, pancreas și cancer de rinichi. Persoanele cu HNPCC ar trebui să aibă screening-uri specifice pentru cancer și să ia în considerare pașii preventivi pe baza istoricului lor familial și a riscului personal. În plus, rudele de sânge ale unei persoane cu HNPCC ar putea avea, de asemenea, această mutație genetică. Este posibil să dorească să aibă consiliere genetică și teste pentru a determina modul în care aceasta afectează recomandările lor de screening.
Testarea MSI identifică tumorile ca MSI-H (adică MSI-ridicat), ceea ce înseamnă că le lipsește proteinele MMR sau sunt deficiente în proteine MMR (dMMR), sau MSI-stabile și MSI-scăzute, ceea ce înseamnă că sunt considerate competente în MMR (pMMR) sau conțin majoritatea sau toate proteinele MMR. Aceste informații sunt utile în special pentru cei cu cancer de colon în stadiul II. Studiile au descoperit că tumorile MSI-H sunt asociate cu un prognostic mai bun. Aproximativ 22% din tumorile de colon din stadiul II (dar doar 12% din tumorile din stadiul III) au MSI-H. Mai multe studii au descoperit că pacienții cu tumori MSI-H în stadiul II nu au obținut niciun beneficiu din terapia adjuvantă cu 5-FU și, de fapt, s-au descurcat mai rău dacă au fost tratați cu chimioterapie. Acest lucru a fost adevărat pentru tumorile MSI-H în stadiul III. Cu toate acestea, boala MSI-stabilă poate beneficia de un tratament bazat pe 5-FU. Unii experți recomandă testarea MSI ca un alt instrument pentru a determina necesitatea tratamentului în boala în stadiul II.
Alți markeri
Oamenii au 23 de perechi de cromozomi, pentru un total de 46 de cromozomi, găsiți în fiecare celulă din corp. Fiecare cromozom conține peste 1000 de gene. Cromozomul 18q conține două gene care sunt legate de suprimarea tumorii. De-a lungul vieții unei persoane, acesta poate dezvolta gene sau cromozomi datorate expunerilor, cum ar fi fumatul și virușii. Pierderea unei copii a cromozomului 18q se numește pierderea heterozigozității (LOH). Rezultatele studiilor privind valoarea predictivă a 18qLOH au fost contradictorii. Un studiu a constatat o supraviețuire mult îmbunătățită atunci când nu a existat LOH (96% vs. 54%), dar un studiu ulterior nu a confirmat acest lucru, prin urmare este necesar un studiu suplimentar. În plus, metoda de testare actuală pentru 18q LOH este dificil de realizat. Ar fi necesare tehnici mai eficiente pentru a face fezabilă utilizarea pe scară largă a acestui test.
Alți markeri moleculari studiați includ KRAS, BRAF, un supresor tumoral numit guanilil ciclaza 2, p53 și ERCC-1. Studiile au descoperit că unii dintre acești markeri sunt utili în determinarea tratamentului împotriva cancerului. De exemplu, medicamentele anti-cancer care vizează proteina EGFR, cum ar fi, Cetuximab și Panitumumab, nu vor fi eficiente la persoanele care au o mutație (defect) a genei KRAS sau BRAF. Aceste teste nu sunt standardul în acest moment, dar unii practicanți le folosesc, așa că este posibil să le auziți descriindu-vă.
Resurse pentru mai multe informații
Referințe
Comitetul mixt american pentru cancer (AJCC). (2017). AJCC Cancer Staging Manual, Eigth Edition.www.cancerstaging.net
Rețeaua națională cuprinzătoare de cancer. NCCN Guidelines: Colon Cancer, Version 2.2019 - 15 May 2019.
Fleming, M., Ravula, S., Tatishchev, S. F. și Wang, H. L. (2012). Carcinom colorectal: aspecte patologice. Jurnalul de oncologie gastrointestinală, 3 (3), 153.
Kopetz, S., Tabernero, J., Rosenberg, R., Jiang, Z. Q., Moreno, V., Bachleitner-Hofmann, T.,. & Capellà, G. (2015). Clasificatorul genomic ColoPrint prezice recurența la pacienții cu cancer colorectal în stadiul II mai precis decât factorii clinici. The Oncologist, 20 (2), 127-133.
Taieb, J., Le Malicot, K., Shi, Q., Penault-Llorca, F., Bouché, O., Tabernero, J.,. & Sargent, D. J. (2017). Valoarea prognostică a mutațiilor BRAF și KRAS în cancerul de colon MSI și MSS în stadiul III. JNCI: Jurnalul Institutului Național al Cancerului, 109 (5).
Windera. T. și Lenza, H. (2010). Markeri predictivi și prognostici moleculari în cancerul de colon. Recenzii privind tratamentul cancerului. 36 (7): 550–556.
- Înțelegerea nutriției dvs. Ce sunt polizaharidele; Dr.
- Riscul de cancer al intestinului și sânului - baraj
- Cancerul uterin Care este riscul dvs. Centrul de cancer MD Anderson
- Medicii au aflat cum să prevină cancerul de colon KXan 36 Daily News
- Microbiomul și cancerul - Goodman - 2018 - Jurnalul de patologie - Biblioteca online Wiley