Isabel E. Kenny
un Departament de Științe Clinice, Universitatea din Bergen
Sahrai Saeed
un Departament de Științe Clinice, Universitatea din Bergen
b Departamentul de boli de inimă, Spitalul Universitar Haukeland, Bergen, Norvegia
Eva Gerdts
un Departament de Științe Clinice, Universitatea din Bergen
Helga Midtbø
un Departament de Științe Clinice, Universitatea din Bergen
b Departamentul de boli de inimă, Spitalul Universitar Haukeland, Bergen, Norvegia
Hilde Halland
un Departament de Științe Clinice, Universitatea din Bergen
Mai T. Lønnebakken
un Departament de Științe Clinice, Universitatea din Bergen
Abstract
fundal
Hipertensiunea mascată (MHT), definită ca tensiune arterială normală de birou (TA), dar TA ambulatorie ridicată, a fost asociată cu un risc cardiovascular crescut. Deși MHT a fost asociat cu obezitatea, există cunoștințe limitate cu privire la prevalența și covariabilele MHT în cohorte obeze.
Metode
Înregistrările BP ambulatorii și ambulatorii și alți factori de risc cardiovascular au fost evaluate la 323 de participanți obezi incluși în studiul disfuncției cardiovasculare asociate grăsimii (vârsta medie 48,9 ± 9,0 ani, 55% femei, IMC mediu 32,3 ± 4,4 kg/m 2). Biroul BP 130-139/85-89 mmHg a fost considerat normal normal. Afectarea arterială subclinică a fost identificată ca o viteză a undei pulsului carotidian - femural mai mare de 10 m/s prin tonometrie de aplanare sau placă carotidă cu ultrasunete (intima maximă - grosimea mediului ≥1,5 mm).
Rezultate
MHT a fost prezent la 17,1% din populație. Pacienții cu MHT au avut o prevalență mai mare a sindromului metabolic, cu TA normală și au fost mai des bărbați în comparație cu indivizii normotensivi (NT) (toți P Cuvinte cheie: leziuni arteriale, tensiune arterială, hipertensiune mascată, sindrom metabolic, obezitate, viteza undei pulsului
Introducere
S-a demonstrat că pacienții cu hipertensiune maschată (MHT) prezintă un risc dublu de evenimente cardiovasculare comparativ cu indivizii normotensivi (NT), comparabil cu cel al pacienților cu hipertensiune arterială susținută (SHT) 1-3. MHT a fost asociat cu afectarea organelor țintă în inimă, artere, rinichi și creier în rapoartele anterioare 3-9. Mai mulți factori de risc cardiovascular, cum ar fi obezitatea, sexul masculin, hipertensiunea arterială indusă de efort, fumatul, diabetul și antecedentele familiale de boli cardiovasculare, s-au dovedit a se grupa în MHT 3. Obezitatea este asociată cu modificări metabolice, care pot implica metabolismul glucozei și lipidelor, sistemul fibrinolitic, sistemul nervos autonom și funcția endotelială 10. Toate aceste modificări favorizează inflamația cardiovasculară și dezvoltarea modificărilor structurale și funcționale cardiovasculare 11. Din aceasta, se poate aștepta o prevalență mai mare a MHT în obezitate. Cu toate acestea, puține studii au raportat prevalența și covariabilele MHT în cadrul cohortelor obeze. Acesta a fost scopul prezentului studiu.
Metode
Populația de studiu
Studiul privind disfuncția cardiovasculară asociată cu grăsimea (FATCOR) este în curs de desfășurare din 2009, având ca scop identificarea factorilor determinanți ai afectării subclinice a organelor țintă la pacienții obezi fără boli cardiovasculare cunoscute 12,13. Studiul FATCOR este o colaborare între un centru de medicină generală specializat în gestionarea pacienților obezi, Alfahelse AS și Departamentul de Boli de Inimă, Spitalul Universitar Haukeland, ambele situate în Bergen, Norvegia. Criteriul de includere pentru studiu a fost un IMC mai mare de 27,0 kg/m 2 la persoanele sănătoase cu vârsta cuprinsă între 30-65 de ani. Criteriile de excludere au fost infarctul miocardic anterior, tulburările gastro-intestinale (inclusiv operațiile anterioare de bypass gastric sau mânecă), boala psihiatrică severă sau incapacitatea de a înțelege limba norvegiană 12. Pentru analiza de față, toți indivizii care au avut măsurători atât ale tensiunii arteriale la birou (TA), cât și ale au fost incluse TA ambulatorie, un total de 339 de participanți. Studiul FATCOR a fost aprobat de Comitetul Regional de Etică. Toți participanții au semnat consimțământul scris în conformitate cu declarația de la Helsinki.
Măsurători ale tensiunii arteriale
O examinare clinică standardizată de medicul generalist de la Alfahelse AS a inclus măsurarea TA de birou, în conformitate cu ghidurile Societății Europene de Hipertensiune 14, utilizând un tensiometru digital Omron M4 validat (Omron Healthcare Co., Ltd, Hoofddorp, Olanda) și dimensiunea potrivită a manșetei în raport cu circumferința brațului. TA a fost măsurată de trei ori la intervale de 1 min după ce pacienții s-au odihnit în poziția așezat timp de cel puțin 5 minute. Biroul TA a fost luat ca medie a ultimelor două măsurători la pacientul individual. TA de birou înalt a fost definită ca TA sistolică mai mare sau egală cu 140 mmHg și/sau TA diastolică mai mare sau egală cu 90 mmHg. TA de birou normal normală a fost definită ca TA sistolică 130-139 mmHg și/sau TA diastolică 85-89 mmHg.
Înregistrarea BP ambulatorie 24-H a fost efectuată utilizând un monitor neinvaziv (Diasys Integra II; Novacor, Cedex, Franța) setat în modul auscultator. A fost utilizată o manșetă de dimensiuni adecvate pentru brațul nedominant, iar participanții au fost instruiți să-și relaxeze brațul atunci când a fost inițiată măsurarea. TA a fost măsurată la fiecare 20 de minute în timpul zilei și la fiecare 30 de minute în timpul nopții, rezultând o medie de 78 de măsurători la 24 de ore. Înregistrarea a fost repetată dacă mai puțin de 70% din măsurători au fost tehnic valabile. TA mare de 24 de ore a fost definită ca TA sistolică medie de 24 de ore mai mare sau egală cu 130 mmHg și/sau TA diastolică medie mai mare sau egală cu 80 mmHg 14.
Participanții la studiu au fost grupați în categorii de TA combinând măsurători de birou și ambulatorii. Participanții au fost clasificați ca NT atunci când atât TA de birou, cât și TA ambulatorie erau normale și SHT dacă ambele erau ridicate. Participanții cu TA cu birou înalt, dar cu TA ambulatorie normală au fost clasificați ca având hipertensiune cu strat alb (WCHT). Participanții la MHT aveau TA normală la birou, dar TA ambulatorie ridicată. Toți participanții care utilizează medicamente BP au fost clasificați ca având SHT independent de măsurătorile reale ale TA, chiar dacă WCHT ar putea fi teoretic prezentă la unii dintre acești participanți tratați.
Factori de risc cardiovascular
Un chestionar standardizat a fost utilizat pentru a aduna informații auto-raportate cu privire la caracteristicile demografice și socio-economice ale participanților și istoricul medical, inclusiv utilizarea curentă a medicamentelor și factorii de risc cardiovascular. Informația a fost asigurată de către medicul generalist. S-au obținut probe de sânge venos de post pentru a măsura lipidele serice, glucoza de post și creatinina serică. La pacienții fără diabet, s-a efectuat un test de toleranță orală la glucoză. Raportul de urină albumină - creatinină a fost măsurat într-o probă de urină de dimineață la fața locului și a fost definit până la 3,4 mg/mmol 14.
Obezitatea a fost identificată ca un IMC de cel puțin 30 kg/m 2 conform liniilor directoare de OMS 15. Sindromul metabolic a fost diagnosticat dacă au fost prezente cel puțin trei dintre următoarele caracteristici: (a) circumferința taliei de cel puțin 88 cm la femei și cel puțin 102 cm la bărbați, (b) TA de birou de cel puțin 130/85 mmHg sau tratament antihipertensiv, (c) glucoză serică de post de cel puțin 5,6 mmol/l sau tratament de scădere a zahărului din sânge, (d) trigliceride serice de post de cel puțin 1,7 mmol/l și (e) colesterol seric cu lipoproteine cu densitate ridicată la jeun mai mic de 1,3 mmol/l la femei și mai mic de 1,03 mmol/l la bărbați în conformitate cu American Heart Association/National Heart, Lung and Linii directoare ale Institutului de sânge 16.
Diabetul zaharat a fost definit ca antecedente de diabet zaharat, utilizarea de medicamente antidiabetice, glucoza de post de cel puțin 7,0 mmol/l sau glucoza plasmatică postîncărcată după 2 ore de peste 11,0 mmol/l. Deficiența de toleranță la glucoză a fost definită ca glucoză serică de 7,8-11,0 mmol/l 2 ore după administrarea orală de 75 g glucoză. Deficitul de glucoză în post a fost definit ca glucoză în post de cel puțin 6,1 mmol/l și mai mic de 7,0 mmol/l. Rezistența la insulină a fost determinată din evaluarea modelului homeostatic (HOMA-IR) 17.
Afectare arterială subclinică
Ecografia carotidă a fost efectuată folosind un aparat cu ultrasunete Phillips iE33 (Phillips Healthcare, Best, Olanda) și un traductor cu rețea liniară de 11-3 MHz. Intimitatea carotidă maximă - grosimea mediului (CIMT) a fost măsurată în modul B, atât pe peretele îndepărtat, cât și pe cel apropiat, în artera carotidă comună, bulb carotid și artera carotidă internă pe ambele părți. O placă carotidă a fost definită ca cIMT maximă focală mai mare sau egală cu 1,5 mm 18.
Carotida - viteza undei pulsului femural (PWV) a fost măsurată folosind tonometrie de aplanație (SphygmoCor; AtCor Medical, Sydney, West Ryde, Australia) conform ghidurilor 19. Formele de undă ale pulsului de presiune au fost obținute transcutanat din arterele carotide și femurale comune drept cu înregistrarea simultană a electrocardiograma pentru sincronizarea timpilor de undă a impulsului carotidian și femural, așa cum s-a descris anterior 20. Distanța proximală între situl carotidian și crestătura sternală și distanța distală între crestătura sternală și situsul femural au fost măsurate cu precizie. Pentru a găsi PWV, distanța proximală a fost scăzută de la distanța distală și distanța netă a fost împărțită la timpul de tranzit între cele două site-uri de înregistrare determinate în raport cu unda R pe ECG. PWV mai mare de 10 m/s a fost definit ca leziuni ale organelor arteriale 21, reflectând rigiditate arterială crescută.
Statistici
Gestionarea datelor și analiza statistică au fost efectuate folosind software-ul statistic SPSS, versiunea 22 (IBM SPSS Statistics, Chicago, Illinois, SUA). Populația studiată a fost împărțită în categorii de TA: NT, MHT și SHT. Variabilele continue sunt prezentate ca media ± SD, în timp ce variabilele categorice sunt prezentate ca procente. Grupul MHT a fost comparat cu grupurile NT și SHT folosind testul χ 2 pentru valori categorice și analiza varianței pentru variabilele continue cu testul post-hoc al lui Scheffe. Covariabile univariabile ale MHT au fost identificate prin analize de regresie logistică în cadrul grupurilor de participanți cu TA normală de birou (NT și MHT) și cu TA ambulatorie crescută la 24 de ore (MHT și SHT). Analiza de regresie logistică multinomială folosind un participant MHT ca referință a fost utilizată pentru a identifica covariabile independente ale MHT. Rezultatele au fost raportate ca probabilitate și intervale de încredere de 95%. O valoare P până la 0,05 a fost considerată semnificativă statistic în toate analizele.
Rezultate
Prevalența MHT a fost de 17,1% în totalul populației studiate. Doar 16 (4,7%) participanți au avut WCHT și, prin urmare, această categorie de TA a fost exclusă de la analize suplimentare. Dintre participanții cu BP normal de birou (grupuri NT și MHT), prevalența MHT a fost de 39,2%. În cadrul grupului MHT cinci (9%), participanții au avut TA sistolică de 24 de ore mai mare sau egală cu 130 mmHg, 41 (71%) participanți TA diastolică de 24 de ore au avut mai mult sau egal cu 80 mmHg și 12 (21%) )) participanții au avut atât TA sistolică de 24 de ore mai mare sau egală cu 130 mmHg, cât și TA diastolică de 24 de ore mai mare sau egală cu 80 mmHg. În comparație cu grupul NT, grupul MHT a avut prevalențe mai mari la bărbați, sindrom metabolic și TA normală la nivel normal (tabele (Tabelele 1 1 și 2). 2). Mai mult, comparativ cu pacienții cu NT, PWV a fost mai mare în rândul pacienților cu MHT, în timp ce IMT carotidă și prevalența plăcii carotide nu au diferit (Tabel (Tabelul 1 și Fig. 1). 1). Grupul MHT a avut o peptidă C în post mai mare decât grupul NT, deși glucoza serică în post nu a diferit (Tabel (Tabelul 3). 3). În comparație cu pacienții cu SHT, pacienții cu MHT erau mai tineri și aveau prevalențe mai scăzute de sindrom metabolic, diabet și hemoglobină A1c mai mică (Tabelele (Tabelele 1 1 și 3), 3), precum și prevalențe mai mici de leziuni ale organelor arteriale măsurate prin PWV, creșterea cIMT și placa carotidă (Fig. (Fig.1)).
tabelul 1
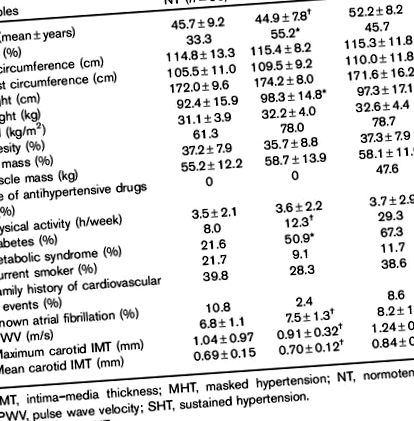
Caracteristici clinice în grupuri cu hipertensiune normotensivă, mascată și hipertensivă susținută
masa 2
Presiunea arterială ambulatorie și ambulatorie în grupuri cu normotensiune, hipertensiune maschată și hipertensiune arterială susținută
Prevalențele bolii arteriale subclinice în hipertensiunea mascată (MHT) comparativ cu grupurile normotensive (NT) și hipertensive susținute (SHT). PWV, viteza undei pulsului; UACR, raportul urină albumină - creatinină.
Tabelul 3
Caracteristici biochimice în grupuri cu normotensiune, hipertensiune maschată și hipertensiune arterială susținută
Covariabile ale hipertensiunii mascate
În analizele de regresie logistică univariabilă, incluzând pacienții cu NT și MHT, sexul masculin, prezența sindromului metabolic, TA normală la nivel înalt și PWV ridicat au fost asociate cu un risc mai mare pentru prezența MHT (toate P (Tabelul 4). În analize de regresie logistică univariabile, incluzând pacienții cu MHT și SHT, MHT a fost asociată cu vârsta mai mică, cu o prevalență mai mică a sindromului metabolic și a diabetului, și cu hemoglobina A1c serică mai scăzută și cu glucoza de repaus alimentar, precum și cu o prevalență mai scăzută a leziunilor arteriale stabilite măsurate prin PWV ridicat și carotidă. placă (toate P (Tabelul 4). 4). Într-o analiză de regresie logistică multinomială, MHT a fost asociată cu prezența sindromului metabolic și a BP de birou normal normal (ambele P (Tabelul 5). 5). În comparație cu pacienții cu SHT, MHT a fost asociată cu PWV mai mic și cu o prevalență mai mică a plăcii carotide (ambele P (Tabelul 5 5).
Tabelul 4
Covariabile semnificative ale hipertensiunii mascate comparativ cu normotensiunea și pacienții cu hipertensiune arterială susținută în analize de regresie logistică univariabile
Tabelul 5
Covariate ale hipertensiunii mascate comparativ cu normotensiunea și pacienții cu hipertensiune arterială susținută în analiza de regresie logistică multinomială multivariabilă
Discuţie
Studiul de față la pacienții supraponderali și obezi, fără boli cardiovasculare cunoscute, arată că MHT a fost frecventă, constatată la 17,1% din populația generală din studiu și la 39,2% în rândul pacienților cu TA normală. În comparație cu pacienții cu NT, MHT a fost asociată în special cu prezența sindromului metabolic și a TA cu normalitate ridicată. În comparație cu pacienții cu SHT, pacienții cu MHT au avut ateroscleroză mai puțin stabilită identificată din rigiditate aortică ridicată (PWV> 10 m/s) sau prezența plăcii carotide.
Studiile anterioare au raportat prevalențe variabile ale MHT: de la 8,5 la 17% în populațiile generale 1,22. Prezentul studiu a constatat o prevalență a MHT comparabilă cu intervalul superior al celor raportate la populațiile generale 3. Tratamentul hipertensiunii arteriale este documentat pentru a reduce în mod eficient afectarea subclinică a organelor țintă și riscul de eveniment cardiovascular asociat 23. Prevalența mai mare a afectării arteriale subclinice raportată anterior în Pacienții cu MHT în unele studii sunt probabil legați de diagnosticul întârziat al hipertensiunii arteriale la acești pacienți 24. Alte studii au arătat, de asemenea, asocierea BP de birou normal normal cu MHT 3,25, sugerând că MHT poate reprezenta un diagnostic ratat de hipertensiune arterială din cauza fluctuațiilor normale în birou BP. Un studiu longitudinal al bărbaților norvegieni cu BP de birou normal la screeningul pentru serviciul militar a arătat o incidență crescută a MHT la acești pacienți atunci când a fost reexaminat 17 ani mai târziu 26, în conformitate cu constatările noastre.
MHT a fost asociată cu gruparea factorilor de risc cardiovascular și metabolismul anormal al carbohidraților în studiile anterioare bazate pe populație 5,6,27-32. Descoperirile noastre într-o cohortă supraponderală și obeză se adaugă la aceste cunoștințe, arătând că caracteristicile clinice specifice, inclusiv prezența sindromului metabolic și TA normală, pot ajuta la identificarea pacienților cu MHT într-un moment în care ateroscleroza clinică nu este încă detectabilă de către cIMT și PWV.
Limitări de studiu
Studiul nostru are mai multe limitări potențiale. Deși chestionarul standardizat pentru colectarea informațiilor de sănătate auto-raportate a fost asigurat de către medicul generalist, este posibil ca problemele de sănătate să fi fost sub-raportate. Există posibilitatea unei părtiniri voluntare, deoarece pacienții incluși în studiul FATCOR au fost recrutați la un centru medical specializat în gestionarea pacienților supraponderali și obezi, recrutând probabil pacienți mai preocupați de sănătatea lor decât pacienții supraponderali și obezi neselectați. Cu toate acestea, mai mult de 50% din SHT a fost diagnosticat prin participarea la studiu, la fel ca mai mult de 20% din diabetul zaharat în totalul populației studiate, indicând valoarea evaluării aprofundate a factorului de risc cardiovascular la pacienții obezi. Studiul FATCOR a inclus pacienți supraponderali și obezi cu vârsta cuprinsă între 30 și 65 de ani, fără boli cardiovasculare cunoscute, iar generalizarea rezultatelor la alte populații ar trebui făcută cu precauție. În cele din urmă, datorită designului transversal, nu este posibil să se deducă cauzalitatea asociațiilor descoperite în acest studiu.
Concluzie
MHT a fost găsit la 17,1% dintre pacienții supraponderali și obezi fără boli cardiovasculare care au participat la studiul FATCOR și la 39,2% dintre pacienții cu TA normală la cabinet, indicând potențialul vast pentru un diagnostic mai oportun al hipertensiunii arteriale la astfel de pacienți dacă se înregistrează TA ambulatorie este utilizat mai larg. În comparație cu pacienții cu NT, MHT a fost deosebit de frecventă la pacienții cu TA normală sau cu sindrom metabolic. În comparație cu pacienții cu SHT, MHT a avut o prevalență semnificativ mai mică a afectării arteriale subclinice.
Mulțumiri
Autorii mulțumesc Autorității Regionale de Sănătate Vest-Norvegiene pentru sprijinul financiar și Simon Fougner Hartmanns Family Fund, Oslo, Norvegia, pentru donarea dispozitivului SphygmoCor. Ei mulțumesc, de asemenea, Marina V. Kokorina, MD, și asistenților medicali de studiu Synnøve Ygre Hauge, RN și Liv Himle, RN, pentru asistență tehnică cu colectarea datelor, înregistrarea și gestionarea pacienților.
Studiul a fost finanțat prin subvenții de la autoritățile regionale de sănătate din Norvegia de Vest.
- Hipertensiune arterială, obezitate, diabet, hiperlipidemie și sindrom metabolic în insuficiența cardiacă - american
- Conținutul de sodiu al țesutului cu text complet gratuit JCM și hipertensiunea arterială la adolescenții obezi
- Afecțiuni cardiace legate de obezitate la copii Știri științifice pentru studenți
- Hormonul ajută la inversarea leziunilor cerebrale cauzate de obezitate
- IJMS Obezitate completă cu text integral, deteriorarea ADN-ului și dezvoltarea bolilor legate de obezitate