Ruby Upadhyay
1 Departamentul de Științe Neurologice, Centrul Medical al Universității Rush, 1725 West Harrison Street, POB Suite 1121, Chicago, IL 60612, SUA
Thomas P. Bleck
2 Rush Medical College, Rush University Medical Center, 600 S. Paulina Street, Chicago, IL 60612, SUA
Katharina M. Busl
3 Departamentul de Neurologie, Divizia de Îngrijire Neurocritică, Universitatea din Florida, McKnight Brain Institute, Camera L3-100, 1149 Newell Drive, Gainesville, FL 32611, SUA
Abstract
Scop. Un bărbat în vârstă de 66 de ani care a prezentat comă sa dovedit a avea hiperamoniemie severă și a fost diagnosticat cu o tulburare a ciclului ureei cu debut tardiv. A fost tratat cu succes și și-a revenit complet. Metode. Raportăm un caz nou de hiperamonemie necirotică și revizuim literatura de specialitate pe această temă. Literatura selectată pentru revizuire a inclus articole în limba engleză referitoare la hiperamonemia folosind termenii de căutare „encefalopatie hiperamonemică”, „encefalopatie non-cirotică”, „encefalopatie hepatică”, „tulburări ale ciclului ureei”, „deficit de ornitină transcarbamilază (OTC)” și „ insuficiență hepatică fulminantă ”. Rezultate. Este prezentat un caz unic de hiperamonemie izolată diagnosticată ca deficit tardiv OTC. Dovezile existente despre hiperamonemia sunt organizate pentru a aborda fiziopatologia, prezentarea clinică, diagnosticul și tratamentul. Raportul de caz este discutat în contextul literaturii revizuite. Concluzie. Deficiența OTC cu debut tardiv, care prezintă encefalopatie hiperammonemică severă și corelat imagistic extins, poate fi complet reversibilă dacă este recunoscută prompt și tratată agresiv.
1. Fundal
Amoniacul este o neurotoxină foarte puternică, bine cunoscută pentru implicația sa în encefalopatia hepatică [1]. Orice caz de stare mentală alterată acută ar trebui să determine o hiperamoniemie ca o cauză potențială. Când se detectează hiperamonemia, trebuie determinată etiologia acumulării acesteia pentru a ghida tratamentul. În timp ce hiperamoniemia la adulți este legată de boală hepatică severă, adesea cirotică, în 90% din cazuri [2], producția crescută de amoniac sau eliminarea scăzută a amoniacului este una dintre etiologiile alternative ale hiperamoniemiei [1]. Conștientizarea hiperamoniemiei în absența unei boli hepatice severe poate duce la diagnosticarea și tratamentul prompt pentru salvarea vieții.
Prezentăm un caz de hiperamonemie acută necirotică severă și revizuim considerațiile sale de fiziopatologie, diagnostic și tratament.
2. Prezentarea cazului
Un manager de afaceri de sex masculin în vârstă de 66 de ani, cu antecedente medicale de hipertensiune arterială, diabet zaharat și sinuzită intermitentă, a fost transferat la centrul nostru de îngrijire terțiară pentru encefalopatie progresivă și îngrijorare pentru starea epileptică neconvulsivă.
Cu trei săptămâni înainte de internare, i s-a prescris un curs de 10 zile de levofloxacină pentru sinuzita presupusă. Deoarece tusea și picurarea postnazală nu s-au îmbunătățit, a fost tratat cu două cursuri de metilprednisolonă în plus față de levofloxacină și ulterior claritromicină. Cu două zile înainte de prezentare, el a dezvoltat dureri de cap și presiune sinusală și s-a plâns de „senzație de oprire”, durere epigastrică și înfundare uscată. În noaptea anterioară prezentării, el s-a trezit frecvent pe tot parcursul nopții, cu o confuzie progresivă. Pacientul nu a avut febră, frisoane sau transpirații. Familia sa a raportat o istorie de anxietate, atacuri de panică, claustrofobie și izbucniri de furie, ultima izbucnire notabilă având loc cu aproximativ 6 luni mai devreme. De remarcat, colegii au găsit la biroul pacientului o colecție de diverse vitamine și suplimente nutritive fără prescripție medicală.
Având în vedere confuzie și agitație din ce în ce mai mare, pacientul a fost dus la un alt spital unde a devenit progresiv mai obscur, necesitând intubație pentru protecția căilor respiratorii. El a început empiric pe vancomicină, ceftriaxonă și aciclovir din cauza meningoencefalitei infecțioase. Analiza LCR a evidențiat proteine totale crescute la 53 mg/dL, glucoză de 160 mg/dl (glucoză serică: 240 mg/dL), lipsită de pleocitoză (1 LBC/mm 3), VDRL LCR negativ, IgM și IgG ale virusului West West negativ, antigen criptococ negativ și culturi fungice și bacteriene negative. Datorită dezvoltării măcinării dinților și preocupării pentru activitatea de convulsii subclinice, a fost efectuată o electroencefalogramă de rutină (EEG) care nu a evidențiat nici o activitate de convulsie, cu toate acestea, rezultatele sunt în concordanță cu disfuncția cerebrală globală. El a început să ia fenitoină și ulterior să ia levetiracetam. Un RMN al creierului a arătat hiperintensități de substanță albă periventriculară cronică ușoară, dar nu s-au găsit rezultate acute. El a fost transferat la centrul nostru de îngrijire terțiară în ziua 3 a spitalului, din cauza îngrijorării stării epileptice neconvulsivante.
La examinare, a fost intubat și ventilat mecanic, fără rezultate fizice generale anormale. La examenul neurologic, el a fost comatos, cu reflexe intacte ale trunchiului cerebral și postură extensoare în toate extremitățile până la stimularea centrală. Lucrările inițiale de laborator au fost remarcabile pentru panoul normal de funcționare hepatică, amoniac seric 120 μg/dL (interval de referință 65-107 μg/dL) și panoul negativ pentru hepatită, precum și alcaloza respiratorie. Analiza repetată a LCR a arătat 3 WBC/mm 3 (76% neutrofile), 1 RBC/mm 3, acid lactic 2,6 meq/L, proteină totală 28,5 mg/dL și PCR cu virus herpes simplex negativ, precum și panou enterovirus negativ și aciclovir a fost întrerupt. Tratamentul cu lactuloză a fost început, dar amoniacul seric a crescut rapid la 494 μg/dL în câteva ore de la sosirea la spitalul nostru. S-au adăugat rifaximină și L-carnitină și s-a inițiat hemodializa emergentă.
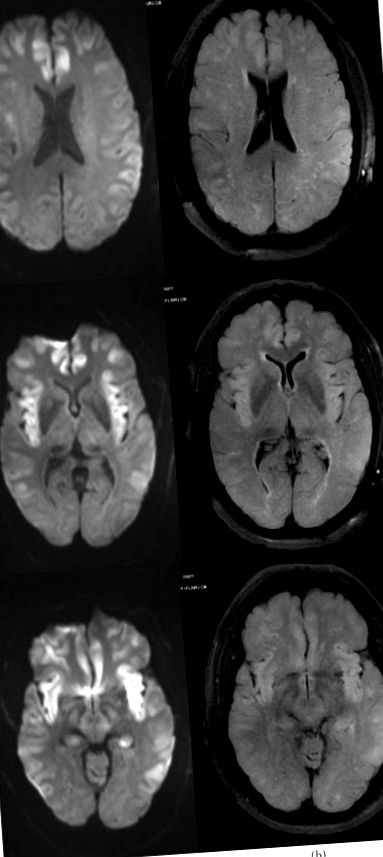
Un RMN al creierului în ziua transferului a arătat zone extinse de difuzie restricționată cu hiperintensitate FLAIR asociată care implică lobi temporali bilaterali și regiuni bilaterale insulare, bilaterale frontale și parietale în zonele corticale și subcorticale și efect ușor difuz al sulurilor cerebrali (Figura 1), fără a spori leziunile. Electroencefalograma continuă (CEEG) pe o durată de 96 de ore a arătat încetinire continuă, neregulată, de joasă tensiune generalizată (Figura 2); totuși, zvâcnirile faciale și ale buzelor observate intermitent nu au avut un corelat electrografic pe cEEG. Rezultatele RMN de implicare a substanței cenușii simetrice în zonele menționate mai sus și în absența insultei hipoxico-ischemice și a activității convulsive, au fost considerate cele mai consistente cu encefalopatia hiperamonemică.
RMN al creierului (a) secvență DWI, (b) secvență FLAIR) în ziua 3 după prezentare, care prezintă zone extinse de difuzie restricționată cu hiperintensitate FLAIR asociată care implică lobi temporali bilaterali, regiuni insulare bilaterale, frontale bilaterale și parietale în corticală și subcorticală zone și eșec ușor difuz al sulcilor cerebrali.
- Dieta Keto 10 lucruri pe care trebuie să le cunoașteți (și probabil nu; t)
- Post intermitent, BCAA și construirea musculară - Ce trebuie să știți Ruperea mușchilor
- Post intermitent Ce trebuie să știți; Dr.
- Post intermitent Ce trebuie să știți MD Anderson Cancer Center
- Dieta Macros Toate lucrurile despre care trebuie să știți