1 Departamentul de Medicină Moleculară, Facultatea de Medicină, Universitatea din Malaya, Kuala Lumpur 50603, Malaezia
Abstract
1. Introducere
2. Materiale și metode
2.1. Materiale vegetale și produse chimice
O. stamineus frunzele plantelor au fost obținute de la Ethno Resource Sdn Bhd. Planta a fost identificată, iar specimenul de voucher a fost păstrat în laboratorul nostru pentru referințe viitoare. Frunzele uscate și pudrate (100 gm) au fost extrase cu 900 ml de etanol 95% timp de 48 de ore, iar extractul de etanol a fost filtrat și evaporat sub presiune scăzută utilizând un evaporator rotativ de tip Buchi pentru a da extractul uscat brut. Randamentul procentual al extractelor de etanol sa dovedit a fi de 8,1% (g/g). Extractul uscat a fost apoi dizolvat în Tween 20 (10% g/v) și administrat oral șobolanilor în concentrații de 100 și 200 mg/kg greutate corporală.
Thioacetamida din (Sigma-Aldrich, Elveția) și toate celelalte substanțe chimice utilizate au fost de calitate analitică și au fost achiziționate mai ales de la Sigma-Aldrich și Fisher. Produsul chimic a fost dizolvat în apă distilată sterilă și injectat intraperitoneal șobolanilor în concentrații de 200 mg/kg greutate corporală [18]. Silimarina (Laboratorul Internațional, SUA) ca medicament standard și a fost dizolvată în Tween 20 (10% g/v) și administrată oral șobolanilor în concentrații de 50 mg/kg greutate corporală [19].
2.2. Determinarea totală fenolică și flavonoidă
O. stamineus extractul a fost evaluat pentru conținutul lor fenolic total utilizând reactiv Folin-Ciocalteu și a fost calculat ca echivalenți de acid galic în mg (GAE)/g de extract conform metodei colorimetrice Folin-Denis [20]. Cu toate acestea, flavonoidele totale au fost determinate utilizând metoda colorimetrică a clorurii de aluminiu și exprimate ca echivalenți de quercetină în mg (QE)/g de extract, așa cum este descris de Dowd [21]. Ambele teste au fost efectuate în trei exemplare.
2.3. Animale
Bărbat adult sănătos Sprague Dawley Șobolani (SD) cu o greutate de 200-250 gm au fost obținuți de la Animal House Unit, Facultatea de Medicină, Universitatea din Malaya, Malaezia. Au fost ținute în cuști cu fund de sârmă la temperatura de 25 ± 3 ° C, 50-60% umiditate și un ciclu de lumină-întuneric de 12 ore timp de cel puțin o săptămână înainte de experiment. Acestea au fost menținute în condiții standard de cazare și acces gratuit la dieta standard și apă ad libitum în timpul experimentului. Protocolul experimental a fost aprobat de Comitetul de etică a animalelor; cu un etic nr. (PM 28/08/2009/MAA (R). Pe parcursul experimentelor au fost aplicate toate criteriile de îngrijire a animalelor pregătite de Academia Națională de Științe și prezentate în „Ghidul pentru îngrijirea și utilizarea animalelor de laborator”.
2.4. Proiectare experimentală
Animalele au fost împărțite aleatoriu în cinci grupuri de câte opt șobolani fiecare și au fost tratați după cum urmează.
Grupa 1
10% Tween 20 (5 ml/kg, po) zilnic timp de 2 luni + apă distilată sterilă (1 ml/kg, i.p) de trei ori pe săptămână timp de 2 luni (grup de control normal).
Grupa 2
10% Tween 20 (5 ml/kg, po) zilnic timp de 2 luni + TAA (200 mg/kg, i.p) de trei ori pe săptămână timp de 2 luni (grup hepatotoxic cu control pozitiv).
Grupa 3
Silimarina (50 mg/kg, po) zilnic timp de 2 luni + TAA (200 mg/kg, i.p) de trei ori pe săptămână timp de 2 luni (bine cunoscut grup de medicamente standard hepatoprotectoare).
Grupa 4
O. stamineus (200 mg/kg, po) zilnic timp de 2 luni + TAA (200 mg/kg, i.p) de trei ori pe săptămână timp de 2 luni (grup de tratament, doză mare).
Grupa 5
O. stamineus (100 mg/kg, po) zilnic timp de 2 luni + TAA (200 mg/kg, i.p) de trei ori pe săptămână timp de 2 luni (grup de tratament, doză mică).
Greutatea corpului tuturor animalelor a fost măsurată în fiecare săptămână. Toți șobolanii au fost sacrificați la 24 de ore după ultimul tratament și au postit peste noapte sub anestezie cu dietil eter. S-au recoltat probe de sânge; serul a fost separat pentru testarea biomarkerului hepatic. Ficatul și splina au fost recoltate, spălate în ser fiziologic normal, șterse cu hârtie de filtru și cântărite. Examinarea grosieră a fost efectuată pentru a examina orice anomalii apărute în organe. Ficatul tuturor animalelor a fost ulterior supus examenului histopatologic într-un mod orbit.
2.5. Examinare biochimică și histopatologică
Probele de sânge colectate au fost separate la 2500 rpm timp de 15 minute după ce au fost complet coagulate. Serul pentru testarea biomarkerilor hepatici precum aspartat aminotransferază (AST), alanin aminotransferază (ALT), fosfatază alcalină (ALP), bilirubină, proteină totală (TP) și albumină a fost testat spectrofotometric prin tehnici automate standard, în conformitate cu procedurile descrise de producătorii din Laboratorul Central de Diagnostic, Centrul Medical al Universității din Malaya. Ficatul a fost feliat și bucățile au fost fixate în soluție de formaldehidă tamponată 10% pentru studiu histologic. Țesuturile fixe au fost procesate de o mașină de prelucrare automată a țesuturilor. Țesuturile au fost încorporate în parafină prin metode convenționale. Secțiuni din 5 μgrosimea m s-a preparat și apoi s-a colorat cu hematoxilin-eozină (HE). După aceea, secțiunile au fost observate la microscop pentru modificări histopatologice, iar fotomicrografiile lor au fost capturate.
2.6. Estimarea malondialdehidei (MDA) în țesutul hepatic
Probele de ficat au fost spălate imediat cu soluție salină rece ca gheața pentru a îndepărta cât mai mult sânge posibil. Omogenatele de ficat (10% g/v) au fost preparate într-un tampon rece de 50 mM fosfat de potasiu (pH 7,4) folosind un omogenizator în gheață. Resturile celulare au fost îndepărtate prin centrifugare la 4500 rpm timp de 15 la 4 ° C folosind o centrifugă refrigerată. Supernatantul a fost utilizat pentru estimarea nivelului de malondialdehidă (MDA) utilizând kitul (Cayman Chemical Company, S.U.A.).
2.7. Analize statistice
Semnificația statistică a fost evaluată utilizând analiza unică a varianței (ANOVA) urmată de testul de comparație multiplă al lui Bonferroni. Toate valorile au fost exprimate ca medie ± S.E.M. și o valoare de
a fost considerat semnificativ în comparație cu grupul de control respectiv folosind programul SPSS pentru versiunea Windows 18 (SPSS Inc. Chicago, IL, SUA).
3. Rezultate
3.1. Greutatea corpului, ficatului și splinei
Înainte de începerea tratamentului șobolanii cântăreau 200-250 g și, după două luni, animalele din grupuri normale, HD, LD și Silimarină au atins greutăți corporale medii de 254,9, 232,7, 263,3 și respectiv 257,0 g. Cu toate acestea, grupul de control TAA pozitiv, greutatea corporală medie a fost redusă la 202,0 g, dar fără o diferență semnificativă în comparație cu grupul de control normal. Nu a existat nicio diferență semnificativă între grupuri, dar administrarea pe termen lung a TAA a dus la o creștere semnificativă a greutății ficatului comparativ cu șobolanii normali. Valorile procentuale ale greutății relative hepatice (LW/BW) procentuale au arătat o diferență semnificativă între grupurile tratate comparativ cu grupul TAA (Tabelul 1).
versus grupul de control normal, b
versus grupul de control TAA și c
3.2. Parametri biochimici și antioxidanți
). În același timp, flavonoidele au fost de 171,4 ± 0,006 mg (echivalenți Quercetin) per g de extracte (ecuația curbei standard:
, ) și un raport de flavonoizi/fenolici de 0,58. Astfel, compușii fenolici au fost componentele antioxidante predominante în O. stamineus extracte, care duc la un efect mai puternic de eliminare a radicalilor.
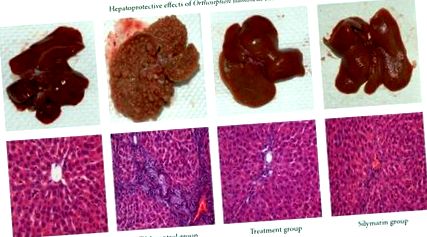
3.3. Examen histopatologic
4. Discutie
În concluzie, acest studiu a arătat că O. stamineus extractele de etanol au efecte hepatoprotectoare care au fost dovedite prin analize biochimice și histopatologice. În consecință, extractele de plante ar putea fi un medicament eficient pentru afectarea hepatică indusă de substanțe chimice, deși această constatare necesită studii suplimentare pentru a cunoaște constituenții activi care par să protejeze ficatul de șobolan împotriva cirozei.
Confirmare
Această lucrare a fost susținută de grantul de cercetare de la Universitatea din Malaya, Malaezia nr. (PS182/2009C).
Referințe
- Extract de boabe de cafea verde Efecte secundare Ziua mea cu cafea
- CAPSULE DE CEAI VERDE De JeaKen - 120 x 850mg Capsule de extract de ceai verde pentru arzător de grăsimi - Pierderea de grăsime
- Capsule de ceai verde 850 mg Extract Slabire Dieta Inghitire usoara Etsy
- Extract de ceai verde Slăbire și scădere în greutate Nature s Best
- Utilizări ale acidului folic, beneficii; Efecte secundare