Instrumente
Urmăriți jurnalul
Creștere, răspuns tumoral și control pe termen lung
Departamentul de Neurologie, Centrul Medical Național al Copiilor și Universitatea George Washington, Washington, D.C.
Departamentul de Neurologie, Centrul Medical Național al Copiilor, 111 Michigan Avenue, Washington, D.C. 20010 === Căutați mai multe lucrări ale acestui autor
Departamentul de Neurologie, Centrul Medical Național al Copiilor și Universitatea George Washington, Washington, D.C.
Departamentul de Oncologie, Centrul Medical Național al Copiilor și Universitatea George Washington, Washington, D.C.
Departamentul de Neuroradiologie, Centrul Medical Național al Copiilor și Universitatea George Washington, Washington, D.C.
Departamentul de Oncologie, Spitalul pentru Copii Riley, Indianapolis, Indiana
Departamentul de Oncologie, Spitalul pentru Copii și Centrul Medical, Seattle, Washington
Departamentul de Oncologie, Spitalul pentru Copii și Centrul Medical, Seattle, Washington
Departamentul de Oncologie, Spitalul de Copii din Pennsylvania, Philadelphia, Pennsylvania
Departamentul de Oncologie, Spitalul de Copii din Pennsylvania, Philadelphia, Pennsylvania
Departamentul de Oncologie Hematologică Pediatrică, Baza Forțelor Aeriene Wright Patterson, Ohio
Departamentul de Oncologie, Centrul Medical Național al Copiilor și Universitatea George Washington, Washington, D.C.
Departamentul de Pediatrie, Memorial Sloan - Kettering Cancer Center, New York, New York
Departamentul de Neurologie, Centrul Medical Național al Copiilor și Universitatea George Washington, Washington, D.C.
Departamentul de Neurologie, Centrul Medical Național al Copiilor, 111 Michigan Avenue, Washington, D.C. 20010 === Căutați mai multe lucrări ale acestui autor
Departamentul de Neurologie, Centrul Medical Național al Copiilor și Universitatea George Washington, Washington, D.C.
Departamentul de Oncologie, Centrul Medical Național al Copiilor și Universitatea George Washington, Washington, D.C.
Departamentul de Neuroradiologie, Centrul Medical Național al Copiilor și Universitatea George Washington, Washington, D.C.
Departamentul de Oncologie, Spitalul pentru Copii Riley, Indianapolis, Indiana
Departamentul de Oncologie, Spitalul pentru Copii și Centrul Medical, Seattle, Washington
Departamentul de Oncologie, Spitalul pentru Copii și Centrul Medical, Seattle, Washington
Departamentul de Oncologie, Spitalul de Copii din Pennsylvania, Philadelphia, Pennsylvania
Departamentul de Oncologie, Spitalul de Copii din Pennsylvania, Philadelphia, Pennsylvania
Departamentul de Oncologie Hematologică Pediatrică, Baza Forțelor Aeriene Wright Patterson, Ohio
Departamentul de Oncologie, Centrul Medical Național al Copiilor și Universitatea George Washington, Washington, D.C.
Departamentul de Pediatrie, Memorial Sloan - Kettering Cancer Center, New York, New York
Prezentat parțial la cea de-a 25-a reuniune anuală a Societății de Neurologie a Copilului, Minneapolis, Minnesota, 23-25 septembrie 1996.
Abstract
FUNDAL
Sindromul diencefalic (DS), care se manifestă prin emaciație progresivă și eșecul de a prospera la un sugar aparent alert, vesel, se datorează de obicei unui gliom hipotalamic de grad scăzut. Tratamentul cu intervenții chirurgicale agresive și/sau radioterapie are un succes variabil în controlul bolii și poate duce la sechele neurologice severe. Chimioterapia s-a dovedit recent a fi eficientă la pacienții cu gliomi de grad scăzut din copilărie, dar este utilizată rar la cei cu DS.
METODE
Autorii au evaluat eficacitatea unui regim de carboplatină și vincristină pentru îmbunătățirea greutății, provocând contracția tumorii și întârzierea necesității terapiilor alternative la șapte copii (cu vârste cuprinse între 9 și 20 de luni; vârstă mediană, cu 11 luni) cu DS. Cinci pacienți au cântărit mai puțin decât percentila a 5-a pentru vârsta lor la începutul studiului, unul a cântărit în percentila a 10-a și unul a cântărit în percentila a 25-a.
REZULTATE
La urmărire (interval, 6-54 luni; mediană, 28 luni), greutățile pacienților crescuseră cu 66-95% (mediană, 80%). La imagistica prin rezonanță magnetică, patru pacienți au avut o reducere> 50% a masei tumorale, unul a avut o reducere de 25-50%, iar doi au avut o boală stabilă. La acei pacienți cu răspuns radiografic la tratament, creșterea în greutate a fost realizată cu hrănirea orală la patru din cinci pacienți, în timp ce cei cu boală stabilă au necesitat suplimentarea tubului nazogastric, nazojejunal sau gastrostomic pentru a menține greutatea. Progresia bolii a avut loc la o medie de 24 de luni de la inițierea chimioterapiei și doi pacienți au rămas liberi de boală progresivă la ultima urmărire. Cinci pacienți erau în viață o medie de 59 de luni de la diagnostic. Nevoia de radiații sau alte terapii a fost întârziată la șase din șapte copii. Terapia a fost tolerată fără toxicități semnificative.
CONCLUZIE
Sindromul diencefalic este o afecțiune rară a copilăriei, caracterizată printr-o emaciație profundă cu eșecul de a prospera, în ciuda aportului caloric aparent normal. Aceasta poate include pierderea persistentă în greutate sau incapacitatea de a câștiga în greutate în perioadele de creștere. Descris pentru prima dată în anii 1930 și ulterior recunoscut și redefinit de Russell în 1951, 1, 2 majoritatea cazurilor de sindrom diencefalic se datorează glioamelor de nivel scăzut ale hipoltalamusului anterior sau ale nervului optic. Astrocitoamele cerebelului și ale celui de-al patrulea ventricul au fost raportate în asociere cu acest sindrom. 3, 4 Trăsăturile clinice asociate includ paloare fără anemie, nistagmus, tremor și dispoziție veselă, chiar euforică. Prezentarea inițială este emaciația, iar diagnosticul poate fi întârziat în absența oricăror descoperiri neurologice.
PACIENTI ȘI METODE
Toți pacienții au efectuat RMN cu sau fără gadoliniu înainte de studiu, după chimioterapie de inducție și după fiecare două cicluri de chimioterapie de întreținere. Toți pacienții au fost obligați să aibă o boală măsurabilă radiografic înainte de inițierea tratamentului. Diagnosticul patologic și răspunsul la terapie au fost determinate de instituția de tratament. Nu a existat histopatologie centrală sau proces de revizuire imagistică. Caracteristicile clinice sau pacienții noștri sunt prezentate în Tabelul 1.
Protocol de tratament
Chimioterapia a fost începută în decurs de 4 săptămâni de la determinarea progresiei tumorii și/sau a biopsiei. Pacienților cu o rezecție mai mică de 50% li s-a permis să înceapă tratamentul după recuperarea după operație. Cei cu o rezecție de 50% sau mai mare trebuie să fi demonstrat progresia tumorală radiografică după operație; înainte de inițiere, erau eligibili pentru chimioterapie. Terapia a fost inițiată cu un regim de inducție a carboplatinei și vincristinei. Carboplatina a fost administrată printr-o perfuzie de 1 oră în doză de 175 mg/m2 săptămânal timp de 4 săptămâni consecutive, urmată de o perioadă de odihnă de 2 săptămâni, apoi a fost reinstituită încă 4 săptămâni. Vincristina în doză de 1,5 mg/m2 (maxim 2 mg) a fost administrată prin apăsare intravenoasă în fiecare săptămână timp de 10 săptămâni. Pacienții cu răspunsuri radiografice obiective sau boală stabilă (definită fie clinic, fie prin neuroimagistică) au fost inițiați chimioterapie de întreținere cu patru doze intravenoase săptămânale de carboplatină 175 mg/m2 și vincristină la 1,5 mg/m2 săptămânal în primele 3 săptămâni din fiecare 4 ciclu săptămânal. A existat o pauză de 3 săptămâni între fiecare ciclu de întreținere și, pentru copiii cu boli stabile sau îmbunătățite, regimul a fost continuat până la 12 cicluri.
Înainte de inițierea fiecărui ciclu de chimioterapie, parametrii hematologici necesari includeau numărul absolut de neutrofile peste 1.500/μl și trombocitele peste 100.000/μl. Pentru acei pacienți cu o întârziere mai mare de 2 săptămâni în tratament, sepsis cu neutropenie sau număr de trombocite mai mic de 20.000/μl, următoarea doză de carboplatină a fost redusă cu 50%. Tratamentul a fost întrerupt pentru febră, neutropenie și/sau sepsis.
Niciunul dintre cei șapte pacienți nu a fost pretratat cu radioterapie. Șase din cei șapte pacienți identificați cu gliom diencefalic nu primiseră chimioterapie anterioară. Pacientul 3 fusese pretratat cu două cicluri de 6 - tioguanină, procarbazină, N‐ (2 - cloretil) ‐N ’- ciclohexil - N - nitrozourea (CCNU) și vincristină înainte de începerea acestui protocol.
Evaluarea răspunsului tumoral
Răspunsurile au fost documentate de către instituția de tratament individuală pe baza constatărilor privind neuroimagistica îmbunătățită prin MR și au fost definite după cum urmează: răspuns complet (CR); dispariția completă a tumorii dispariția tumorii pe studii de imagistică; răspuns parțial (PR); reducere mai mare de 50% a dimensiunii tumorii; răspuns minor (MR); reducere mai mare de 25%, dar mai mică de 50% a dimensiunii tumorii; boală stabilă (SD); fie nici o modificare sau mai puțin de 25% în dimensiunea tumorii; și boală progresivă (PD); mai mare decât o creștere de 25% a dimensiunii. Mărimea leziunii a fost evaluată prin determinarea produsului celor mai mari două dimensiuni observate pe studiile de imagistică în orice plan unic.
REZULTATE
Studiați populația și demografia
În seria noastră de șapte pacienți, erau cinci bărbați și două femei. Vârsta la diagnostic a variat de la 9 luni la 20 de luni, cu o mediană de 12 luni. Toți pacienții nu au reușit să prospere ca simptom de prezentare: nistagmus a apărut la doi pacienți și vărsături au fost raportate la doi pacienți. Patru pacienți au avut biopsii (nici o rezecție mai mare de 50%), iar tumorile au fost astrocitoame pilocitare în toate cele patru. Locul tumorii primare a fost considerat a fi hipotalamusul la cinci pacienți, chiasma la un pacient și talamusul la un pacient; deși atât leziunile chiasmatice, cât și cele talamice au avut implicare hipotalamică. Timpul de urmărire a fost de la 6 luni la 54 de luni, cu o mediană de 26 de luni (Tabelul 1).
Răspunsul și controlul bolilor
Pacienții supraviețuitori studiați au fost urmăriți, pe baza datei ultimei monitorizări de către instituția de tratament, pentru o mediană de 59 de luni de la diagnostic. Răspunsul la tratament este prezentat în Tabelul 1. RMN a dezvăluit contracția tumorii după chimioterapie la cinci din șapte pacienți (patru PR, un RM) și boală stabilă la doi pacienți (Fig. 1 (30K), 241K)). Dintre cei cinci copii care au răspuns la chimioterapie, răspunsul maxim a fost observat în timpul ciclului de chimioterapie de întreținere doi din trei pacienți și în timpul ciclului de întreținere opt la ceilalți doi pacienți cu răspuns.
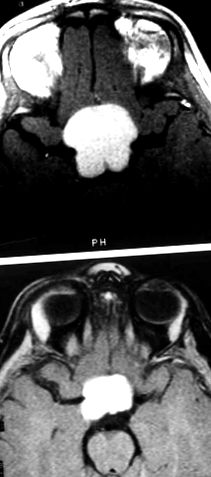
(A) Imagine de rezonanță magnetică ponderată T1 care demonstrează o tumoare supresivă la un pacient cu sindrom diencefalic (DS). Înainte de chimioterapie, tumora măsura 3,3 x 3,3 cm. (B) După tratamentul cu vincristină și carboplatin, tumora măsoară 2,0 x 2,5 cm.
(A) Al doilea pacient care demonstrează o tumoare diencefalică complicată (săgeți). Înainte de inițierea carboplatinului și vincristinei, tumorile măsurau 3,0 x 3,5 cm. (B) Contracție dramatică a tumorii diencefalice (săgeți) după tratamentul cu chimioterapie, cu dimensiuni finale de 0,8 x 0,8 cm, ceea ce reprezintă o contracție mai mare de 50%.
Progresia bolii, determinată de mărirea radiografică a tumorii, a avut loc la o medie de 24 de luni (interval, 6-28 luni) după inițierea chimioterapiei la cinci pacienți. Toți pacienții au recidivat numai la locul tumorii locale și niciunul nu a dezvoltat boală diseminată în momentul recăderii. Progresia bolii nu a avut loc în timpul regimului de chimioterapie de inducție la niciun pacient. Pacientul 1 a demonstrat progresia în timpul celui de-al doilea ciclu de chimioterapie de întreținere, în timp ce ceilalți pacienți care au progresat au făcut acest lucru după finalizarea chimioterapiei de întreținere. Doi pacienți au murit din cauza bolii lor; cinci sunt în viață, o mediană de 59 de luni de la diagnostic (interval, 21-59 luni).
Pacienții cu tumori care au răspuns neuroadiografic la chimioterapie și apoi au progresat au experimentat o perioadă ceva mai lungă de supraviețuire fără progresie decât acei pacienți cu SD care au progresat (24, 24 și 28 luni față de 6 și 13 luni). Doi pacienți sunt încă liberi de progresie la 21 de luni și 54 de luni de la diagnostic. Dintre cei care au recidivat, doi au primit chimioterapie alternativă în momentul primei progresii, dar ambii au progresat aproximativ 1 an mai târziu și au continuat să primească radioterapie locală. Una este stabilă, iar cealaltă a murit de boală progresivă. Doi copii au continuat să primească radioterapie locală imediată și rămân liberi de alte boli progresive. Un copil nu a fost tratat în momentul progresiei la chimioterapia cu carboplatină și vincristină și a murit.
Parametrii de creștere
Curba de creștere reprezentativă pentru pacient care demonstrează răspunsul tumorii la chimioterapie. La diagnostic (săgeată etichetată), greutatea este mai mică decât percentila a 5-a. Cu tratamentul ulterior (săgeată marcată), există o creștere rapidă a greutății până la mai mult de percentila 95. Există relativ puține schimbări în creșterea liniară.
Curba de creștere reprezentativă pentru pacientul care prezintă boală stabilă. Greutatea este mai mică decât percentila a 5-a la diagnostic (săgeată etichetată). Cu toate acestea, spre deosebire de Figura 4, creșterea în greutate este lentă. Pacientul primea, de asemenea, calorii suplimentare sub formă de nutriție parenterală totală (TPN). Deoarece TPN este retras (săgeată etichetată), există o scădere în greutate.
Toxicitate
Chimioterapia a fost bine tolerată și niciun pacient nu a fost eliminat din studiu din cauza toxicităților hematologice, neurologice sau renale. Mai exact, niciunul dintre pacienți nu a prezentat neurotoxicitate de la vincristină. Întârzieri în chimioterapie au fost observate din cauza trombocitopeniei prelungite la un pacient, dar nu a limitat tratamentul. Niciunul dintre pacienți nu a necesitat reducerea dozei de chimioterapie din cauza neurotoxicității. Au existat șapte spitalizări pentru febră, frisoane și neutropenie, cu culturi negative care au apărut la doi copii.
DISCUŢIE
Tratamentul optim al DS rămâne neclar. Dacă nu se administrează tratament după diagnostic, supraviețuirea medie este de obicei mai mică de 12 luni. Chirurgia agresivă poate prelungi supraviețuirea și îmbunătăți creșterea în greutate, dar rezecția chirurgicală totală este rareori posibilă datorită localizării anatomice a tumorii. 5 Într-o serie în care s-au încercat rezecții agresive, 70% dintre copii, în special cei cu vârsta sub 12 luni, s-au descurcat slab doar cu operația. 20 Când rezecția radicală nu poate fi realizată, adăugarea radioterapiei poate crește supraviețuirea pentru o perioadă de timp variabilă. 3, 6, 21 Rezecția parțială urmată de radioterapie sau radioterapie singură poate avea ca rezultat supraviețuirea fără progresie și stabilizarea greutății, totuși efectele dăunătoare ale radiației neuroaxiei într-un sistem nervos central vulnerabil, în dezvoltare, au fost bine recunoscute și descrise. 11-14 Prognosticul slab în aceste cazuri și nevoia de a trata copiii foarte mici, care sunt vulnerabili la sechelele radioterapiei, susțin nevoia de terapii alternative.
Având în vedere rezultatele acestei serii, în special creșterea în greutate susținută la acei copii care răspund la tratament și lipsa relativă de toxicitate, sunt necesare studii suplimentare cu chimioterapie pentru pacienții cu DS. Abordările de tratament trebuie să evalueze nu numai eficacitatea pe termen scurt a tratamentului, ci și capacitatea terapiei de a evita sechelele neurologice pe termen lung.
Mulțumiri
Dr. Olson este Emily Dorfman Fellow al American Brain Tumor Association.
- Care este cea mai bună dietă în timpul tratamentului cancerului ovarian SurvivorNet
- Cancerul amigdalelor Simptome, tratament și prognoză
- Biologia proliferării adipocitelor albe - Hausman - 2001 - Obesity Reviews - Wiley Online
- Suplimente de vitamine și minerale în timpul tratamentului împotriva cancerului
- Cum arată tratamentul pentru cancerul tiroidian papilar