Mattheus K Reinders
1 Farmacie clinică, Atrium Medisch Centrum Parkstad, Heerlen, Olanda
Tim L Th A Jansen
2 Reumatologie, Centrul Medical Leeuwarden, Leeuwarden, Olanda
Abstract
Introducere
Guta este denumirea colectivă a mai multor afecțiuni care se caracterizează prin formarea și depunerea cristalelor de urat monosodic (MSUr). Condiția este asociată cu episoade recurente de durere articulară acută datorită depunerii de cristale MSUr în lichidul sinovial. În plus față de efectele observate la nivelul articulațiilor, pielea/țesutul subcutanat și rinichii pot fi, de asemenea, afectate de depozite topacee, celulită, nefropatie uratică și, respectiv, pietre la rinichi. În majoritatea cazurilor, nu există o cauză identificabilă a gutei, dar sunt prezenți de obicei factori evidenți care pot contribui la creșterea nivelului de urat (acid uric), cum ar fi funcția renală redusă, obezitatea și utilizarea diureticelor. Hiperuricemia poate exista de câțiva ani până la decenii înainte de apariția primelor simptome ale atacurilor de gută; de aceea este o boală asociată și corelată cu îmbătrânirea.
Guta este una dintre cele mai frecvente artrite inflamatorii care afectează vârstnicii; cu toate acestea, în general, pare să fie slab gestionat.1-3 În parte, acest lucru se datorează absenței unor strategii și linii directoare de tratament suficiente. În 2006, Liga Europeană împotriva Reumatismului (EULAR) a publicat primele recomandări internaționale pentru diagnosticul și tratamentul gutei.4,5 Dezvoltarea acestor orientări EULAR și a Societății Britanice de Reumatologie (BSR) a coincis cu îmbunătățirea educației profesionale și a pacienților. ca îndemn pentru îmbunătățirea performanței profesionale. Până de curând, alopurinolul era singurul medicament antihiperuricemic disponibil la nivel mondial. Două uricosurice cu bariere în ceea ce privește disponibilitatea (benzbromaronă și probenecid) sunt disponibile de ani de zile, dar locul lor exact în strategia de tratament nu este clar. În 2008 și, respectiv, 2009, Agenția Europeană pentru Medicamente (EMEA) și Food and Drug Administration (FDA) au aprobat febuxostat, un nou inhibitor selectiv al xantinei, pentru tratamentul hiperuricemiei la pacienții cu gută, respectiv. Febuxostat extinde în mare măsură opțiunile de tratament pentru guta refractară sau cu intoleranță la alopurinol, dată fiind prevalența imensă a tulburării și disponibilitatea bună la nivel mondial a unui singur medicament antihiperuricemic.
Incidența și prevalența gutei la vârstnici este în creștere.1,6,7 Acest lucru apare legat de îmbunătățirea duratei de viață, ceea ce duce la creșteri similare ale bolilor legate de vârstă (de exemplu, boli cardiovasculare) și ale efectelor adverse asociate ale tratamentului (de exemplu, diuretice și salicilați cu doze mici) care pot crește riscul de gută. „Guta cu debut la vârstnici” diferă de guta „clasică” întâlnită la bărbații de vârstă mijlocie în mai multe privințe: nu există predominanță masculină, ci o distribuție egală a sexului, prezentare poliarticulară cu afectarea articulațiilor extremităților superioare, mai puține episoade acute de gută, evoluție clinică indolentă și o incidență crescută a tophi.1,8 Mai multe analize au abordat provocările specifice tratamentului gutei la vârstnici.1,8-11 Această revizuire se va concentra pe febuxostat pentru gestionarea gutei la vârstnici.
Fiziopatologia gutei
Acidul uric se formează din acid nucleic fie endogen din defalcarea celulelor, fie exogen din metabolismul alimentelor. Răcirea și acidificarea micromediului, care poate duce la formarea acută a cristalelor de urat, reduc solubilitatea MSUr. Intestinul excretă o treime din urat, iar două treimi sunt excretate pe cale renală. Transportul de urat renal este de obicei explicat printr-un model cu 4 componente: filtrarea glomerulară, o reabsorbție aproape completă a uratului filtrat, secreția ulterioară și reabsorbția postsecretorie în tubul proximal rămas.12 Recent, mai mulți transportatori de urat noi au fost identificați ca fiind cheia de joc roluri în homeostazia uratului, inclusiv URAT-1 și Glut9.12,13 Reglarea nivelurilor serice de acid uric se află sub un puternic control genetic. O meta-analiză recentă a scanărilor de asociere la nivelul genomului arată că variantele comune de ADN la 9 loci diferiți sunt asociate cu concentrații de acid uric.
Consumul excesiv de alcool (în special bere), băuturi răcoritoare îndulcite, fructoză, carne și fructe de mare poate crește, de asemenea, nivelurile de urat seric (ur).
Inhibarea transportorilor de urați poate fi realizată de uricosurici, iar producția de acid uric poate fi inhibată folosind inhibitori ai xantin oxidazei, cum ar fi alopurinolul. Febuxostat este un nou inhibitor selectiv al xantin oxidazei. Depozitele de acid uric pot fi, de asemenea, lizate de enzima uricază, gena codificatoare pentru care a devenit defectă la om în Miocen din cauza unei mutații evolutive. Absența combinată a uricazei și reabsorbția aproape totală a uratului filtrat explică faptul că oamenii (și maimuțele mai mari) au niveluri de 10 ori mai mari decât cele ale altor mamifere.
Hiperuricemie indusă de medicamente
Terapia diuretică cronică este asociată cu excreția redusă a acidului uric. Mecanismele sunt reabsorbția crescută a acidului uric în tubul proximal secundar epuizării volumului și competiția dintre acidul diuretic și uric pentru mecanismul secretor al acidului organic în tubul proximal.15 Terapia cu diuretice în doze mici la pacienții hipertensivi nu pare să modifice uratul seric. niveluri semnificative.15,16 Într-adevăr, cerința pentru terapia anti-gută la pacienții hipertensivi este dublată pentru dozele tiazidice de ≥25 mg/zi (în echivalenți de hidroclorotiazidă); nu se observă o creștere semnificativă a riscului pentru dozele mai mici.15,17 În mod similar, terapia cu doze mici cu un diuretic buclă nu este asociată cu hiperuricemie.15,18 Cu toate acestea, terapia cu diuretice cu doze mici poate fi eficientă în hipertensiune, dar insuficientă la pacienții cu insuficiență cardiacă cronică care deseori suferă de insuficiență renală cronică.
Se știe că salicilații interacționează cu manipularea uratului renal și dozele mici inhibă excreția de urat. Într-un studiu s-a constatat că chiar și mini-doza de aspirină (75 mg/zi) a fost asociată cu o scădere cu 15% a excreției de urat la pacienții vârstnici.19 Astfel, la persoanele în vârstă cu boli cardiovasculare nu numai diuretice, ci și mini-doze aspirina este importantă.
Caracteristicile prezentării gutei
Guta poate fi diagnosticată cu certitudine numai prin identificarea cristalelor de urat (MSUr), prezente în articulații în timpul atacurilor acute de gută sau în tophi. Practicianul clinic poate confirma prezența și tipul cristalelor prin microscopie de polarizare.4,20,21
Profilul caracteristic al gutei este cel al monoartritei severe care apare în câteva ore. Prima articulație metatarsofalangiană este afectată în 50% din atacurile de gută, iar acest lucru este cunoscut sub numele de podagra. Guta poate fi localizată în alte articulații, dar umerii, șoldurile și coloana vertebrală sunt rareori afectate. Atacul inițial de gută implică de obicei monoartrită, dar gută pe termen lung pe parcursul mai multor ani poate deveni poliarticulară și ar putea duce la creșterea leziunilor articulare. În mod similar, un echilibru pozitiv al acidului uric pe parcursul mai multor ani poate provoca depuneri topacee, posibil cu artrită periodică.
Producția de urat
Guta primară tinde să implice o excreție scăzută de urat, care este originată în primul rând în tubul proximal. Doar o minoritate de cazuri implică supraproducția de urat. În unele tratamente ale cancerului (în special limfoame și leucemii), pacienții pot dezvolta sindrom de liză tumorală, inclusiv hiperuricemie severă cu risc de nefropatie uratică.
Nefropatie uratică în gută
Chimioterapia agresivă la pacienții cu leucemie cronică sau limfom malign ar putea provoca o cantitate excesivă de acid uric, rezultând nefropatie acută de urat datorită depunerii cristalelor de urat în canalele de colectare și uretere. Se pot găsi mai multe tipuri de cristale de urat, inclusiv cristale de acid uric, urat amorf, urat monosodic și cristale de urat de amoniu.
În hiperuricemia cronică, riscul de a dezvolta cristale renale crește pe măsură ce concentrațiile serice de urat cresc. Riscul este de aproximativ 10% cu uratul seric 0,42 - 0,48 mmol/L, dar poate crește până la 50% cu concentrații serice de urat> 0,70 mmol/L. În absența calculilor sau a altor factori de risc (cum ar fi hipertensiunea arterială), riscul de nefropatie uratică a fost în general considerat scăzut.22
Prezentări radiografice de gută
Examinarea cu raze X la debutul inițial al gutei nu a evidențiat nicio anomalie, cu excepția eventualelor artroze preexistente și edem al țesuturilor moi. Cartilajul și osul pot fi afectate de artrita cronică și/sau recurentă și, ulterior, prezintă îngustarea cavității articulare din cauza dispariției cartilajului și eroziuni sau chisturi din cauza contactului cu osul juxta-articular. Aceste anomalii și apariția eroziunilor pot ridica suspiciuni de gută, dar eroziuni sunt o manifestare secundară și caracteristică nediagnostică a gută timpurie. Cu toate acestea, în guta cronică, unele dintre aceste modificări caracteristice pot ajuta la diagnostic.
Strategii de tratament pentru gută
Următoarea este o prezentare generală a diferitelor clase de medicamente și a utilizării potențiale a acestora ca parte a strategiilor de tratament pentru gută. Informațiile despre aceste medicamente sunt prezentate în Tabelul 1, iar strategia terapeutică actuală este rezumată în Tabelul 2 .
tabelul 1
Medicamente antihiperuricemice în gută
| Alopurinol po | XOi: toate | 100–900 mg: 300 mg | Ajustarea dozei la funcția renală |
| Benzbromarone po | transportor de urati: excretor scazut, supus intolerantei sau alergiei la alopurinol | 50–200 mg: 100 mg | Eficacitate slabă în insuficiența severă a funcției renale |
| Febuxostat po | XOi: toate, în special în ceea ce privește intoleranța la alopurinol | 80–120 mg: 80 mg | Nu există ajustare a dozei în insuficiența renală |
| Probenecid după | transportator de urati: excretor scazut | 500-2000 mg: 1000 mg | Eficacitate slabă în funcția renală moderată-severă |
| Rasburicase iv | UrO: efect litic asupra tofilor | Utilizare cu compasiune: de exemplu, 0,2 mg/kg în perfuzie de 60 de minute în ziua 1, apoi 1 × pe săptămână; (+ metilprednisolon 100 mg iv) | Biologic |
Abrevieri: iv, intravenos; po, oral; UrO, urat oxidază; XOi, inhibitor de xantină oxidază.
masa 2
Strategie sugerată bazată pe experiență pentru inițierea terapiei antihiperuricemice
Confirmarea diagnosticului: detectați cristalele de urat prin microscopie de polarizare
Două sau mai multe erupții de gută pe an sau tophi/distrugerea articulațiilor din cauza atacurilor de gută
Sfaturi terapeutice 1: alopurinol 100–300 mg/zi 2
intoleranță la alopurinol: luați în considerare febuxostat
Monitorizarea eficacității în laborator la 6-8 săptămâni: 3
0,30-0,36 mmol/L, dar fără alte atacuri (fără colchicină/AINS/corticosteroizi), apoi continuați cu alopurinolul
sUr> 0,30 mmol/L plus atacuri de gută/tophi persistente și ur> 1,5 mmol/24 ore, mergeți la 5
sUr> 0,30 mmol/L plus atacuri de gută/tophi persistente cu uR 4) după 6 luni: vezi 5
NB: atunci când încercați să eliminați tophi, valoarea țintă este SUr 1 Sub rezerva motivării și toleranței de către pacient.
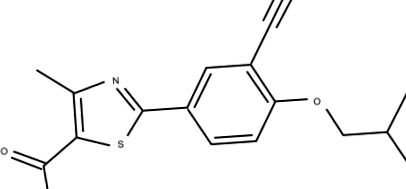
Structura chimică a febuxostatului.
Febuxostat 10 până la 120 mg/zi, în funcție de doză, nivelurile medii de UR reduse de la momentul inițial cu 25% până la 70% la voluntarii sănătoși; Excreția de 24 de ore a acidului uric urinar în ziua 8 a fost redusă cu 46% până la 66% față de placebo.58 Ambele efecte par să se platească la doze> 120 mg/zi. 58 Vârsta (18 până la 40 de ani față de ≥65 ani) și sexul nu a avut niciun efect semnificativ clinic asupra proprietăților farmacocinetice și farmacodinamice ale febuxostatului oral 80 mg/zi la voluntarii sănătoși.59
Absorbția febuxostatului este rapidă, cu un timp până la Cmax de ± 1 oră. Febuxostat poate fi administrat indiferent de aportul de alimente sau antiacide.60 Valorile farmacocinetice sunt liniare în intervalul de 10 până la 120 mg. Febuxostat se leagă foarte mult (> 98%) de proteinele plasmatice umane, în principal la locul de legare a diazepamului. Timpul de înjumătățire prin eliminare al febuxostatului este de aproximativ 12 ore. Febuxostat este eliminat în principal prin glucuronidare în ficat. De asemenea, s-au găsit unii metaboliți activi cuantificabili 67M-1, 67M-2 și 67M-4.61-63 Nu sunt recomandate ajustări ale dozelor la pacienții cu insuficiență renală ușoară până la moderată. Febuxostat inhibă izoenzima 2D6 a citocromului P450, dar interacțiunile cu CYP2D6 nu sunt considerate semnificative clinic. La fel ca în alopurinol, o interacțiune importantă medicament-medicament poate apărea cu mercaptopurina și azatioprina datorită inhibării xantin oxidazei. Deși nu sunt disponibile încă date, trebuie evitată combinația acestor medicamente cu febuxostat.
Două studii de fază I au investigat farmacocinetica, farmacodinamica și siguranța febuxostatului la subiecți de sex masculin și feminin cu insuficiență normală sau ușoară, moderată sau severă a funcției renale.64,65 Un studiu (n = 32) a utilizat febuxostat în doza standard de 80 mg/zi.64 Deși expunerea plasmatică la febuxostat și metaboliții săi a fost, în general, mai mare la subiecții cu grad crescut de insuficiență renală, procentele de scădere a acidului uric seric au fost comparabile, indiferent de grupul funcției renale. O doză o dată pe zi de 80 mg de febuxostat pare a fi sigură și bine tolerată în diferite grupuri de funcții renale și nu pare să necesite nicio ajustare a dozei pe baza diferențelor în funcția renală.64
Un studiu deschis de fază I (n = 27) a investigat farmacocinetica și farmacodinamica, precum și siguranța febuxostatului la subiecți de sex masculin și feminin cu funcție hepatică normală (n = 11) și subiecți cu hepatice ușoare (n = 8) și moderate 8) insuficiență.66 Avertisment: pacienții cu insuficiență hepatică severă, conform clasificării Child-Pugh, au fost excluși, iar febuxostat 80 mg a fost administrat o dată pe zi timp de doar 7 zile. În general, insuficiența hepatică ușoară până la moderată nu a afectat în mod semnificativ expunerea la febuxostat sau la metaboliții săi activi în această perioadă de 1 săptămână.
Eficacitate clinică
Tabelul 3
Eficacitatea și tolerabilitatea febuxostatului în studiile controlate randomizate
- Ultimul număr al revistei Neurosurgical Focus examinează abordările anterioare ale coloanei vertebrale toracolombare
- Cea mai recentă versiune Online Pastile dietetice pentru farmacii Naturale Cel mai sigur - Managementul HazMat
- Schimbarea comportamentului în sănătate pentru managementul obezității - FullText - Obezity Facts 2017, Vol
- Hiperpotasemie (Potasiu ridicat) Management și tratament Clinica Cleveland
- Este timpul pentru centre multidisciplinare de gestionare a obezității - Pories - 2019 - Obezitate - Wiley Online