De la Departamentul de Nefrologie și Endocrinologie, Facultatea de Medicină, Universitatea din Tokyo, Tokyo, Japonia.
Vizualizați cea mai recentă versiune a acestui articol. Versiunile anterioare:
Abstract
Este bine cunoscut faptul că populațiile cu un aport alimentar ridicat de sare au incidențe mai mari de hipertensiune, iar încărcarea sării nu numai că crește tensiunea arterială (TA), ci provoacă leziuni cardiovasculare la animale și oameni. 1-3 Am arătat recent că sarea a exercitat un efect mai dăunător asupra rinichilor și inimii șobolanilor hipertensivi obezi cu sindrom metabolic decât la șobolanii hipertensivi slabi. 4-6 Într-o investigație recentă pentru a identifica mecanismul leziunilor cardiovasculare induse de sare, am descoperit semnalizarea încrucișată între Rac1 și receptorul mineralocorticoid (MR), o cale alternativă care modulează activitatea MR 7 și am obținut dovezi care sugerează că activarea anormală a căii aldosteron/MR este implicată în dezvoltarea hipertensiunii induse de sare și a afectării cardiovasculare în sindromul metabolic. 8.9
Mecanismul hipertensiunii sensibile la sare în sindromul metabolic
TA a pacienților hipertensivi individuali a răspuns diferit la încărcarea cu sare, 1-4, iar factorii genetici și factorii genetici pot fi implicați în sensibilitatea la sare a TA. Studii clinice recente au demonstrat că sindromul metabolic este un factor nongenetic important care crește sensibilitatea la sare a TA. 10.11
Deși mecanismul precis al creșterii BP indusă de sare este încă necunoscut, s-a presupus că alterarea excreției renale de sodiu este principala cauză a hipertensiunii. 12 Pacienții cu hipertensiune arterială sensibilă la sare au curbe anormale ale funcției renale pentru excreția urinară de sodiu. 13 Câțiva factori modulează capacitatea renală de excreție de sodiu: rasă, îmbătrânire, stres psihologic și obezitate. 12 Într-adevăr, curba funcției renale a hipertensivelor obeze este identică cu cea a hipertensivelor de tip sensibil la sare 10 și, în concordanță cu această constatare, pacienții hipertensivi obezi au un răspuns depresor mai mare la restricția sării într-o dietă cu conținut scăzut de sare decât hipertensivul slab. pacienți. 10 În plus, un studiu recent din China a arătat că subiecții cu sindrom metabolic au prezentat un răspuns depresor mai mare la o dietă cu conținut scăzut de sare și un răspuns presor mai mare la o dietă bogată în sare decât un grup de control care nu avea sindrom metabolic. 14 Există o relație strânsă între rezistența la insulină, care este esențială în sindromul metabolic, și sensibilitatea la sare a TA, 10,11, deoarece rezistența la insulină apare la persoanele sensibile la sare comparativ cu subiecții normotensivi rezistenți la sare, 15 și încărcarea cu sare determină dezvoltarea rezistența la insulină la subiecții negri adulți tineri. 16
Conform mecanismului hipertensiunii induse de obezitate, sensibil la sare, mai mulți factori induc natriureză anormală și sensibilitate crescută la sare a TA în sindromul metabolic. Compresia rinichiului, hiperinsulinemia compensatorie din cauza rezistenței la insulină, 17 hiperactivitatea simpatică, 18 activitatea crescută a sistemului renină-angiotensină (RA) și excesul de aldosteron în plasmă s-au dovedit a fi frecvente la persoanele obeze 19 și toți acești parametri modulează natriureza. Hall și colegii 20.21 au demonstrat că administrarea de aldosteron la câini nu numai că a indus retenția de sodiu, ci și-a crescut TA. Am arătat recent că activarea anormală a căii aldosteron/MR poate fi implicată în dezvoltarea leziunilor cardiovasculare, precum și a hipertensiunii sensibile la sare în sindromul metabolic. 4-9
Implicarea excesului de aldosteron în proteinuria indusă de obezitate
S-a crezut mult timp că aldosteronul este un hormon care reglează electroliții, volumul de lichide și homeostazia BP. Cu toate acestea, s-a produs o schimbare de paradigmă în domeniul cercetării aldosteronului, studii recente sugerând că aldosteronul este un mediator important al afectării organelor țintă. 22-25 Aldosteronul acționează direct asupra inimii, creierului și rinichilor, iar excesul de aldosteron provoacă proteinurie și boli cronice de rinichi. Imunomarcarea pentru MR la rinichiul de șobolan a relevat o colorare clară nu numai în canalele colectoare corticale, ci și în glomeruli, 4 și atât ARNm MR, cât și proteinele sunt exprimate în podocite cultivate. Expunerea la aldosteron induce apoptoza la podocitele cultivate, iar administrarea de aldosteron și o dietă bogată în săruri induc proteinurie masivă și imunocolorare mai puțin intensă pentru nefrină, un marker podocit, la șobolanii nefrectomizați unilateral. 26 Aceste descoperiri sugerează că proteinuria indusă de aldosteron și leziunile renale sunt atribuite leziunilor podocitelor, deoarece mai mulți anchetatori au demonstrat că leziunile podocitelor joacă un rol esențial în dezvoltarea albuminuriei și progresia bolii renale. 27
Studiile epidemiologice au arătat că sindromul metabolic crește riscul de microalbuminurie28, iar unii cercetători au raportat în mod clar niveluri crescute de aldosteron plasmatic la subiecții cu obezitate severă. 29 La șobolanii obezi spontan hipertensivi (SHR), un model de sindrom metabolic manifestat printr-un grup de obezitate viscerală, hipertensiune arterială, rezistență la insulină și dislipidemie, s-a constatat că excreția urinară de proteine crește semnificativ într-un mod dependent de vârstă, asociat cu piciorul. eliminarea procesului, sugerând vătămarea podocitelor, în timp ce în SHR-urile neobeze nivelurile de proteine urinare au rămas scăzute și nu au existat modificări ale podocitelor. Interesant este că nivelul aldosteronului seric a fost în mod clar mai ridicat la SHR obezi decât la SHR nonobezi. Expresia genică a kinazei1 induse de ser și glucocorticoizi (Sgk1), o moleculă din aval de semnalizare MR, a fost, de asemenea, reglată în sus în rinichiul SHR obezi. În concordanță cu aceste constatări, administrarea blocantului MR eplerenonă a redus semnificativ proteinuria, sugerând că excesul de aldosteron poate contribui la afectarea renală în SHR obezi. 4
Factori de eliberare a aldosteronului derivați de adipocite
figura 1. Efectele încărcării sării pe rinichi (stânga) și inima (dreapta) șobolanilor hipertensivi obezi. Încărcarea cu sare a șobolanilor hipertensivi obezi nu numai că agravează proteinuria și provoacă leziuni podocitare 9, dar provoacă disfuncții diastolice cardiace și fibroză perivasculară. 10 NS indică o dietă normală cu sare; HS, dietă bogată în sare; Apple, eplerenonă. **P
Astfel, țesutul adipos secretă ARF în sindromul metabolic, iar secreția de aldosteron indusă de ARF nu poate fi suprimată în mod adecvat de o dietă bogată în săruri, sugerând că secreția inadecvată de ARF de către adipocite provoacă hiperaldosteronism (sindrom metabolic de tip 1). Prin urmare, excesul de aldosteron și o dietă bogată în sare pot induce sinergic activarea MR, iar activarea MR duce la dezvoltarea leziunilor renale și a disfuncției cardiace (Figura 2). Sprijinind acest lucru, un studiu epidemiologic 38 a arătat că subiecții obezi pe o dietă bogată în sare au dezvoltat proteinurie într-un mod dependent de aportul de sare, dar că subiecții nonobezi nu au dezvoltat deloc proteinurie. Bănuim că majoritatea subiecților obezi din acel studiu trebuie să fi avut un exces de aldosteron, deși aldosteronul plasmatic nu a fost măsurat în acel studiu. 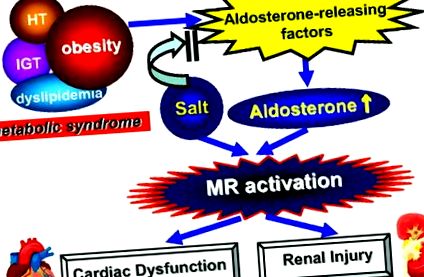
Figura 2. Mecanismul leziunilor renale și al disfuncției cardiace la pacienții obezi cu sindrom metabolic de tip 1 care au hiperaldosteronism. ARF derivate din adipocite stimulează secreția de aldosteron de către cortexul suprarenal. Spre deosebire de sistemul RA-aldosteron, nu există o reglare de feedback negativ a secreției de adipocite ARF prin încărcare de sare. Ca urmare, secreția inadecvată de aldosteron și o dietă bogată în sare induc activarea MR sinergic, iar activarea MR duce la afectarea renală și disfuncție diastolică cardiacă.
Calea alternativă a activării MR
Într-un studiu, o treime dintre subiecții cu sindrom metabolic au avut hiperaldosteronism, dar nu toți subiecții au avut o concentrație plasmatică ridicată de aldosteron. 39 În ciuda absenței hiperaldosteronismului, tratamentul cu un antagonist MR este cel mai eficient mod de a reduce excreția urinară de albumină la hipertensivii diabetici cu albuminurie. Cu toate acestea, trebuie remarcat faptul că nivelurile serice de aldosteron nu sunt întotdeauna predictive pentru eficacitatea antagoniștilor MR, sugerând că activarea MR are loc chiar și în absența excesului de aldosteron, posibil printr-o cale alternativă de activare MR. Este interesant faptul că Quinkler și colab. 41 au demonstrat o creștere de 5 ori a expresiei MR renale la pacienții cu insuficiență renală și proteinurie severă, legând astfel activarea MR de boala renală.
Luată împreună, Rac1 activează MR independent de aldosteron, dar activarea MR indusă de Rac1 este semnificativ îmbunătățită în prezența aldosteronului. Astfel, modificările concentrațiilor plasmatice de aldosteron și activitatea Rac1 pot modula activarea MR, interdependent, ducând la concluzia că activarea MR indusă de Rac1 poate fi implicată în patogeneza bolilor renale proteinurice, atât aldosteron în mod independent, cât și independent. 7
Factori care modifică activarea Rac1
Conform efectului încărcării de sare asupra activării Rac1 și proteinuriei, în studiul nostru Rac1 renal a fost găsit activat de o dietă bogată în sare la șobolanii sensibili la sare Dahl, iar activarea a fost asociată cu proteinurie masivă. Cu toate acestea, administrarea de inhibitori Rac1 a atenuat moderat proteinuria. În concordanță cu aceste constatări, Sgk1, o moleculă din aval de MR, a fost paradoxal reglată în sus prin încărcarea sării, în ciuda suprimării adecvate a aldosteronului plasmatic, dar inhibarea Rac1 a atenuat reglarea în sus, sugerând că încărcarea sării induce activarea MR prin activarea Rac1. În sprijinul acestui fapt, administrarea blocantului MR eplerenonă a redus semnificativ proteinuria. 54
În concluzie, desenul nostru hipotezând implicarea aldosteronului și activării MR în sindromul metabolic - leziuni renale asociate este prezentat în Figura 3. La o treime din pacienții cu sindrom metabolic care au concentrațiile plasmatice crescute de aldosteron (sindromul metabolic de tip 1), creșterea care este atribuibil ARF derivate din adipocite, nu există o reglare negativă a secreției de ARF adipocite printr-o dietă bogată în sare și, prin urmare, secreția de aldosteron neadecvată în timpul încărcării sării activează MR (Figura 2). Cu toate acestea, chiar și în absența excesului de aldosteron (sindromul metabolic de tip 2), anumite citokine derivate din adipocite și o dietă bogată în sare sunt capabile să activeze MR prin activarea Rac1, iar activarea MR duce la boli renale cronice, disfuncții cardiace, și hipertensiune sensibilă la sare (Figura 3).
Figura 3. Implicarea hipotezată a activării căii aldosteronului/MR în dezvoltarea bolilor renale cronice (BCR), a bolilor cardiovasculare (BCV) și a hipertensiunii sensibile la sare la pacienții obezi cu sindrom metabolic de tip 2 care nu au hiperaldosteronism. Atât factorii derivați de adipocite, cât și o dietă bogată în sare sunt capabili să activeze Rac1, iar Rac1 activ, la rândul său, să activeze MR.
În rezumat, am identificat Rac1 ca un activator independent de ligand al MR. Activarea MR indusă de Rac1 joacă de fapt un rol semnificativ în progresia leziunii renale în sindromul metabolic, sugerând posibilitatea de a face din Rac1 o țintă nouă a terapiei pentru bolile renale cronice.
Perspective evolutive asupra sistemului Aldosteron/MR
Se afirmă că aldosteronul a jucat un rol cheie în tranziția filogenică de la peștii acvatici la tetrapodele terestre, având în vedere efectele sale epiteliale majore asupra retenției de sodiu și excreției de potasiu. Astfel, calea aldosteronului/MR a permis animalelor să rețină sodiu în organism pentru a susține viața pe uscat, unde era puțină sare. Cu toate acestea, în societățile noastre industrializate moderne, abundența de sare și o pandemie de obezitate cauzează sinergic activarea inadecvată a sistemului aldosteron/MR, posibil prin activarea Rac1 și care, la rândul său, provoacă hipertensiune arterială sensibilă la sare, boli cardiovasculare și cronice boală de rinichi. Modificările stilului de viață au fost însoțite de o prevalență crescândă a hipertensiunii arteriale asociate cu obezitatea, iar restricția de sare este, prin urmare, cea mai importantă strategie nu numai pentru prevenirea hipertensiunii arteriale la subiecții obezi cu sindrom metabolic, ci și pentru o terapie cardiovasculară eficientă la pacienții hipertensivi obezi.
Acest articol se bazează în principal pe prezentarea conferinței Memorial Arthur C. Corcoran la cea de-a 63-a Conferință a tensiunii arteriale ridicate, 24 septembrie 2009, Chicago, Ill.
- Efectele protectoare ale dietei mediteraneene asupra diabetului de tip 2 și a sindromului metabolic - PubMed
- Mazărea, broccoli poate preveni obezitatea și sindromul metabolic, spune studiul
- Rolul histidinei dietetice în prevenirea obezității și a sindromului metabolic Inima deschisă
- Oxitocina poate juca un rol central în obezitate și sindromul metabolic HCPLive
- Circumferința gâtului legată pozitiv de obezitatea centrală, supraponderalitatea și sindromul metabolic în
