Termeni asociați:
- Biopolimer
- Cazeină
- Pectină
- Polimeri
- Stropi
- Proteine
- Polizaharide
- Proteine din lapte
- Biopolimeri
Descărcați în format PDF
Despre această pagină
Nanotehnologia pentru alimente
III Utilizarea proteinelor în sistemele de livrare la scară nano
Utilizarea interacțiunii proteină - polizaharidă pentru a forma sisteme de încapsulare bazate pe coacervare a fost redusă la scară nanomatică de Huang și Jiang (2004). Studiul lor asupra flavonoidelor care promovează sănătatea sa concentrat pe cea mai activă formă conținută în ceaiul verde, epigalocatechina galat (EGCG). Ceaiul verde a fost folosit mult timp ca băutură, dar biodisponibilitatea redusă este întotdeauna o problemă. Prin urmare, acest grup a sugerat încapsularea catehinelor de ceai pentru a le spori stabilitatea și biodisponibilitatea. Ei au folosit coacervatele formate din complexe proteină - polizaharide ca metodă de încapsulare ieftină pentru catehinele de ceai verde la nivel micro și nanomic.
Yu și colab. (2005) au aplicat nanotuburi peptidice ca suport pentru imobilizarea enzimei. Ei au încapsulat o lipază în interiorul nanotuburilor peptidice și au constatat că activitatea catalitică a enzimelor legate de nanotuburi a fost de fapt mai mare (> 33%) decât lipaza liberă la temperatura camerei. În mod interesant, la 65 ° C, activitatea lipazei în nanotuburi a fost cu 70% mai mare în comparație cu lipazele libere. Au arătat că enzima din interiorul nanotuburilor poate fi reciclată prin fabricarea nanotuburilor magnetice folosind nanocristale superparamagnetice FePt imobilizate la exteriorul nanotuburilor peptidice. Ei au sugerat că intensificarea activității lipazelor în nanotuburile peptidice este probabil indusă de schimbarea conformației lipazelor în forma deschisă (structură activă enzimatic), deoarece lipazele sunt adsorbite pe suprafețele interioare ale nanotuburilor peptidice.
Nohiro și colab. (2006) au utilizat cazeina pentru a forma micele proteice de dimensiuni nano pentru a deține substanțe hidrofobe. Grupul a folosit transglutaminaza pentru a forma micelele de cazeină încapsulate cu ANS cu dimensiunea particulelor de 36 nm, care au reținut ≥ 50% ANS atunci când au fost tratate cu tripsină. Această metodă este utilă pentru fabricarea de soluții transparente suprasaturate prin solubilizarea substanțelor hidrofobe în alimente funcționale și produse farmaceutice.
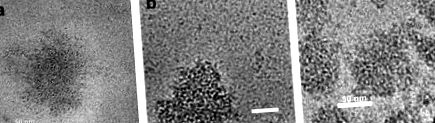
Unul dintre conceptele mai recente introduse de Semo și colab. (2006; condus de Y. Livney) este utilizarea micelelor de cazeină auto-asamblate ca vehicule nanocapsulare. Autorii au realizat că micelele de cazeină (CM) sunt de fapt nanocapsule create de natură pentru a furniza nutrienților, cum ar fi calciu, fosfat și proteine nou-născutului. Astfel, au sugerat utilizarea CM ca sistem auto-asamblat pentru nano-încapsulare și stabilizare a substanțelor nutraceutice hidrofobe pentru îmbogățirea produselor alimentare. Vitamina D2 a fost utilizată ca model pentru compușii nutraceutici hidrofobi. D2-rCM și rCM au avut o morfologie similară, care a fost, de asemenea, tipică în CM care apar în mod natural, așa cum s-a demonstrat în micrografiile Cryo-TEM (Figura 23.2).
Figura 23.2. Imagini Cryo-TEM: (a) CM reasamblat (rCM), (b) Vitamina D2 conținând rCM (D2-rCM), (c) CM naturală în laptele degresat (seturi nepublicate; prin amabilitatea Dr. Livney și Dr. Danino, Facultatea de Biotehnologie și Inginerie Alimentară).
Micelele reasamblate au avut diametre medii de 146 și 152 nm cu și fără vitamina D2, respectiv, similare CM normale, care sunt de obicei 150 nm în medie. S-a demonstrat că un compus nutraceutic poate fi încărcat în CM, utilizând tendința naturală de auto-asamblare a cazeinelor bovine. Concentrația de vitamine din micelă a fost de aproximativ 5,5 ori mai mare decât în ser. Chiar și în ser, vitamina D2 a fost prezentă doar legată de cazeine solubile reziduale. O observație foarte interesantă a fost că morfologia și diametrul mediu al micelelor reasamblate au fost similare cu cele ale CM care apar în mod natural. Micelele au oferit protecție parțială împotriva degradării induse de lumina UV a vitaminei D2. Prin urmare, acest studiu a demonstrat că CM poate fi util ca nanovehicle pentru prinderea nutraceuticelor hidrofobe în produsele alimentare. Astfel de nanocapsule pot fi încorporate în produsele lactate fără a le modifica proprietățile senzoriale.
Recent, Livney și Ron (2007) au demonstrat utilizarea complexelor β-lactoglobulină - polizaharide pentru a transporta nutraceutice hidrofobe. Autorii au profitat de capacitatea beta-lactoglobulinei de a lega moleculele hidrofobe și au adăugat un strat protector secundar prin complexarea sa cu polizaharidă încărcată. Au arătat că, controlând cu atenție potențialul zeta al particulei, se poate produce un vehicul nanosize stabil. Cu toate acestea, trebuie remarcat faptul că, în astfel de cazuri, sarcina bioactivului în veziculă a fost scăzută și efectul de stabilizare nu a fost încă demonstrat. Cu toate acestea, acest control inteligent al proprietăților fizice ale sistemului este un exemplu excelent pentru asamblarea unei vezicule de încapsulare nano-dimensionată pe baza controlului proprietăților fizice.
Volumul 2
Natasha Nayak, Harjinder Singh, în Enciclopedia chimiei alimentelor, 2019
Factori care influențează interacțiunile dintre proteine și polizaharide
Factorii care afectează natura interacțiunilor proteină - polizaharidă și structurile corespunzătoare formate pe baza acestor interacțiuni pot fi clasificați ca factori extrinseci, intrinseci și de procesare. Acești factori pot fi variați pentru a obține funcționalitățile dorite pentru aplicații adaptate (Tabelul 1).
Tabelul 1. Factori care influențează interacțiunile proteine din lapte - polizaharide
| Extrinsec | Raport de amestecare (r) | Afectează structura complexelor sau coacervatelor formate. R mai mic are ca rezultat formarea de coacervate care se unesc rapid, în timp ce r mai mare are ca rezultat coacervate mai stabile. |
| Concentrația moleculară | Coacervarea poate apărea în soluții foarte diluate, în timp ce incompatibilitatea termodinamică este favorizată în sistemele mai concentrate. | |
| pH | La un pH> punctul izoelectric (pI) al proteinei, există o repulsie între proteină și polizaharidă. Lângă pI se formează complexe solubile, în timp ce o reducere suplimentară a pH-ului are ca rezultat formarea de coacervate. | |
| Forța ionică | La o concentrație ridicată de sare, microionii determină o scădere a interacțiunii electrostatice, în timp ce, la o rezistență ionică scăzută, interferența cu formarea complexului proteină - polizaharidă este minimă. | |
| Densitatea încărcării | Coacervarea nu are loc la densități de încărcare scăzute, în timp ce precipitarea complexelor inter-polimerice are loc la densități de încărcare foarte mari. Natura grupului de sarcină (carbonil versus sulfat) influențează puterea interacțiunii. | |
| Intrinsec | Conformația moleculară | Flexibilitatea crescută a lanțului și mobilitatea crescută a sarcinii duc la o legare mai puternică. |
| Distribuirea taxelor | Lanțurile încărcate uniform formează faze mari omogene, în timp ce o distribuție inegală a sarcinii duce la formarea unei mezo-faze cu o structură micelară. | |
| Greutate moleculară | Structura internă și dimensiunea finală a complexelor/coacervatelor pot fi controlate prin ajustarea greutății moleculare a polielectrolitului. | |
| Prelucrare | Foarfeca | Forfecarea poate provoca restructurarea complexelor formate sau poate stabiliza coacervatele împotriva floculării. |
| Presiune | Presiunea determină denaturarea parțială a proteinei, ceea ce întărește interacțiunea în timpul formării complexe. | |
| Temperatura | Denaturarea prin căldură crește flexibilitatea moleculară, ceea ce duce la interacțiuni electrostatice mai puternice, producând complexe mai stabile. | |
| Acidificare | Tipul metodei de acidificare utilizate, de exemplu, acidul clorhidric sau glucono-delta-lactona, influențează structura complexelor formate. |
Syrbe și colab. (1998) au stabilit câteva reguli de bază pentru înțelegerea efectului combinat al pH-ului și puterii ionice asupra comportamentului de amestecare al sistemelor proteină - polizaharide. Pentru sistemele de polizaharide neionice, pH-ul și puterea ionică afectează numai auto-asocierea proteinelor. Incompatibilitatea este direct corelată cu auto-asocierea proteinelor, care este cea mai mare la pI a proteinei și scade către pH-uri acide și alcaline. În sistemele mixte, incompatibilitatea în domeniul pH-ului apropiat de pI este legată de concentrații ionice scăzute, unde ambii biopolimeri sunt neîncărcați, diferența în densitățile de încărcare este zero, iar prezența sării suprima auto-asocierea proteinelor. Prezența grupărilor carboxilate sau sulfatate încărcate face ca polizaharidele ionice să aibă o natură anionică în intervalele de pH care sunt relevante pentru alimente, unde apare complexarea cu proteina încărcată pozitiv.
Interacțiuni proteină - polizaharide și digestia particulelor complexe
Introducere
Există un interes considerabil în prezent în protejarea moleculelor bioactive împotriva eliberării în stomac sau intestin (Singh și Horne, 2009). În același timp, este bine cunoscut faptul că un număr mare de polizaharide (dextran, chitosan, amidon modificat chimic, alginate, pectine, caragenan, xantan etc.) sunt rezistente la acțiunea enzimelor și bacteriilor gastrice și intestinale, în timp ce acestea sunt specific hidrolizat numai de bacteriile colonice. Prin urmare, aceste proprietăți ale polizaharidelor ar putea fi utile, de exemplu, pentru elaborarea materialelor de acoperire și matrice pentru livrarea specifică a moleculelor bioactive către colon (Macleod și colab., 1999; Vandamme și colab., 2002).
Din datele din literatură, pot fi recunoscute două abordări principale pentru utilizarea interacțiunilor proteină-polizaharidă pentru elaborarea purtătorilor „comutați” sensibili la stimul. Una dintre ele, care a fost investigată pe larg, este utilizarea acoperirilor monostrat sau multistrat hidrofil sau hidrofob la suprafețele picăturilor în emulsii (macro) (dimensiune> 0,5 μm), care pot fi utilizate pentru microincapsularea nutraceuticelor hidrofobe și/sau hidrofile (Benichou și colab., 2004; McClements și colab., 2008, 2009; Grigoriev și Miller, 2009). De exemplu, Benichou și colab. (2004) au demonstrat că complexele electrostatice de izolat de proteine din zer (WPI) cu gumă xantan pot fi utilizate cu succes atât pentru acoperirea eficientă pe mai multe straturi a picăturilor multiple (duble) de emulsie, cât și pentru eliberarea controlată a vitaminei B1 prinse în faza apoasă interioară a acestor picături sub variația pH-ului fazei apoase externe.
O altă abordare promițătoare este utilizarea nanocomplexelor proteină-polizaharidă pentru a prinde compuși bioactivi. Zimet și Livney (2009) au folosit această abordare cu succes pentru a prinde acidul docosahexaenoic (DHA) prin utilizarea nanocomplexelor electrostatice ale β-lactoglobulinei cu metoxi pectină scăzută. Nanocomplexele s-au dovedit a avea o stabilitate coloidală remarcabilă (potențial zeta mai negativ decât -50 mV, dimensiunea medie a particulelor ≈100 nm) și capacitatea de protecție împotriva oxidării DHA în timpul testelor de stres accelerat de valabilitate: doar –5-10% a fost pierdut timp de 100 de ore la 40 ° C, comparativ cu ~ 80% atunci când DHA neprotejat a fost monitorizat (Zimet și Livney, 2009).
Toate aceste date arată clar că interacțiunile proteină - polizaharide pot fi utilizate ca un instrument promițător pentru a regla capacitatea proteinei-polizaharide de a se comporta ca un nanovehicul pentru livrarea controlată a diferitelor tipuri de nutraceutice la un anumit loc de acțiune, la un anumit ritm, și/sau ca răspuns la un declanșator specific de mediu (pH, putere ionică, temperatură, acțiune enzimatică).
Dimensiunile la scară nanomatică ale acestor nanovehicule, care sunt tipice moleculelor/asociaților de biopolimeri, pot oferi avantaje suplimentare, deoarece, așa cum a fost sugerat de Acosta (2009), dimensiunea sistemelor de livrare, în special sub 500 nm, a permis promisiunea abordării probleme de biodisponibilitate orală scăzută sau livrare ineficientă de substanțe nutritive/medicamente slab solubile în apă. Aceasta este o consecință a îmbunătățirilor bazate pe următorii factori (Acosta, 2009; Semenova și Dickinson, 2010): (1) solubilitatea aparentă a ingredientelor active; (2) rata transferului de masă; (3) timpul de retenție gastro-intestinală în mucusul care acoperă epiteliul intestinal; (4) rata de eliberare (datorită suprafeței mari); și (5) absorbția directă a particulelor de către epiteliul intestinal (Horn și Rieger, 2001; Chen și colab., 2006; Medina și colab., 2007).
Activitățile de cercetare în domeniul elaborării sistemelor de livrare a nanoparticulelor pentru micronutrienți și nutraceutice, care pot fi încorporate în produsele alimentare, au crescut aproape exponențial în ultimul deceniu (Ransley și colab., 2001; Velikov și Pelan, 2008; McClements și colab., 2008, 2009; Faulks și Southon, 2008; Augustin și Hemar, 2009; Semenova și Dickinson, 2010; Semenova și colab., 2012). Cu toate acestea, factorii fizico-chimici care influențează atât susceptibilitatea nanopurtătorilor de complex biopolimeric la acțiunea enzimatică în condițiile GI simulate, cât și eliberarea controlată (bioaccesibilitate) a nutraceuticelor prinse din acestea nu sunt încă înțelese în mod clar.
Prezenta lucrare încearcă să elucideze baza structurală care stă la baza digestibilității (sub acțiunea enzimelor gastrice și intestinale în condițiile simulate ale tractului GI in vitro) a nanocomplexelor proteine-polizaharide care implică fosfatidilcolină din soia (PC). În paralel, se caută o perspectivă mai penetrantă asupra generalității și diferențelor de comportament ale nanocomplexelor din tractul GI in vitro, pe baza diferitelor tipuri de interacțiuni proteină - polizaharide, în special electrostatică (SCN + sulfat de dextran) și legătură covalentă ( SCN + MD).
Se remarcă faptul că alegerea PC-ului polinesaturat (Lipoid S100 (lecitină)) ca nutraceutic s-a datorat proprietăților sale ca agent anti-îmbătrânire, un protector superior împotriva afectării ficatului (Kidd, 1996, 2000) și furnizor de poliinsaturate esențiale acizi grași (mai mult de 80% din lanțurile de hidrocarburi nesaturate ușor de oxidat ale acizilor grași esențiali precum oleic, linoleic și linolenic, tabelul 6.1). Mai mult decât atât, PC a fost, de asemenea, de interes, deoarece poate forma lipozomi receptivi la mediu într-un mediu apos, ceea ce ar putea fi promițător ca purtători suplimentari atât pentru ingrediente alimentare și medicamente hidrofobe cât și hidrofile (Gennis, 1989).
Tabelul 6.1. Compoziția chimică a fosfatidilcolinei (PC) (Lipoid S 100, Lipoid GmbH, Germania)
- Oat - o prezentare generală Subiecte ScienceDirect
- Maioneză - o prezentare generală Subiecte ScienceDirect
- Salata de îmbrăcăminte - o prezentare generală Subiecte ScienceDirect
- Frunza de zmeură roșie - o prezentare generală Subiecte ScienceDirect
- Amidon de cartofi - o prezentare generală Subiecte ScienceDirect