1 Departamentele de Pediatrie, Biologie Moleculară și Farmacologie și Obstetrică și Ginecologie, Washington University School of Medicine și St. Spitalul de Copii St. Louis, St. Louis, Missouri 63110
1 Departamente de Pediatrie, Biologie Moleculară și Farmacologie, și Obstetrică și Ginecologie, Școala de Medicină a Universității Washington și St. Spitalul de Copii St. Louis, St. Louis, Missouri 63110
1 Departamentele de Pediatrie, Biologie Moleculară și Farmacologie și Obstetrică și Ginecologie, Washington University School of Medicine și St. Spitalul de Copii St. Louis, St. Louis, Missouri 63110
1 Departamentele de Pediatrie, Biologie Moleculară și Farmacologie și Obstetrică și Ginecologie, Washington University School of Medicine și St. Spitalul de Copii St. Louis, St. Louis, Missouri 63110
Abstract
Anorexia și scăderea în greutate sunt complicații frecvente ale infecțiilor acute și cronice și rezultă din inducerea citokinelor, prostaglandinelor și a altor mediatori inflamatori care sunt critici pentru eliminarea agenților patogeni. Atenuarea selectivă a răspunsului hipofagic la infecție și menținerea producției de factori esențiali pentru controlul infecției ar fi un plus util la terapia antimicrobiană în tratamentul bolilor umane. Aici, evaluăm contribuția relativă a prostaglandinelor derivate din ciclooxigenază (COX) -1 și COX-2 la anorexie și la scăderea în greutate precipitată de activarea imună sistemică de către lipopolizaharidă (LPS). Folosind inhibitori farmacologici selectivi ai izoformei COX și șoareci knockout genici, am constatat că inhibarea COX-2 în timpul inflamației induse de LPS are ca rezultat consumul de alimente conservate și menținerea greutății corporale, în timp ce inhibarea COX-1 are ca rezultat pierderea în greutate crescută și prelungită. Reglarea neuropeptidei Y, a hormonului de eliberare a corticotropinei, a leptinei și a interleukinei-6 nu se modifică în funcție de inhibarea COX-2 după administrarea LPS. Datele noastre implică inhibarea COX-2 ca țintă terapeutică pentru menținerea stării nutriționale, permițând în același timp un răspuns normal la citokine în timpul infecției.
activarea sistemului imunitar în timpul infecțiilor acute bacteriene sau virale are ca rezultat generarea de citokine și alți mediatori inflamatori esențiali pentru controlul infecției. Acești mediatori inflamatori au ca rezultat chemotaxia și activarea celulelor mononucleare și modificări locale în fluxul sanguin și permeabilitatea vasculară care facilitează eradicarea agentului patogen. În plus față de aceste acțiuni benefice, factorii induși în timpul infecției sau alte inflamații sistemice prezintă și acțiuni dăunătoare. O consecință importantă a inflamației este anorexia, însoțită de pierderea acută în greutate (17, 19, 37). Cu infecții sau inflamații severe sau prelungite, aceste modificări ale nutriției pot afecta negativ rezolvarea infecției, vindecarea rănilor și creșterea. Abilitatea de a inhiba selectiv răspunsul anorectic păstrând în același timp acțiunile mediatorilor inflamatori necesari eliminării agenților patogeni ar fi o completare foarte utilă la terapia antimicrobiană a infecției.
Lipopolizaharida (LPS), o componentă majoră a peretelui celular exterior al bacteriilor gram-negative, a fost utilizată pe scară largă ca model pentru sepsisul acut. Similar cu infecția bacteriană, administrarea LPS are ca rezultat febră, producție robustă de citokine și anorexie la rozătoare (20, 30). Inhibarea producției de citokine sau acțiunea după LPS, în special factorul de necroză tumorală (TNF) -α și interleukina (IL) -1β, atenuează anorexia indusă de LPS (29, 30). Cu toate acestea, inhibarea acestor mediatori proximali ai cascadei inflamatorii ar fi de așteptat să compromită supraviețuirea în cadrul unui agent patogen viu, replicant, sugerat de susceptibilitatea crescută a șoarecilor cu deficit genetic al receptorului TNF 1 (31), IL-6), și interferon-γ (6) la infecția cu agenți bacterieni precum Listeria monocytogenes.
S-a demonstrat, de asemenea, că inhibarea producției de prostaglandine atenuează răspunsul anorectic la LPS sau IL-1β (18, 33), dar mecanismul prin care se produce acest lucru și consecințele pentru generarea unui răspuns inflamator protector rămân neclare. Primul pas angajat în sinteza prostaglandinelor, catalizat de sintagazele prostaglandinei H, sau ciclooxigenazele, a servit ca o țintă terapeutică importantă pentru tratamentul bolilor inflamatorii (36). Medicamentele antiinflamatoare nesteroidiene (AINS) dezvoltate recent sunt capabile să inhibe selectiv funcția uneia dintre cele două izoforme ale ciclooxigenazei (COX), COX-1 sau COX-2 (21, 22,36). Înțelegerea îmbunătățită a rolurilor fiziologice ale acestor izoforme COX va permite noi aplicații ale medicamentelor selective COX, cu mai puține sechele adverse, cum ar fi gastrita și nefrotoxicitatea, decât inhibitorii neselectivi.
În acest studiu, testăm ipoteza că inhibarea COX-selectivă va fi eficientă în atenuarea răspunsului anorectic care însoțește activarea sistemului imunitar fără a modifica răspunsurile citokinice sau suprarenale. Folosind agenți farmacologici selectivi COX-1 și COX-2 și șoareci knockout, vom determina contribuția relativă a fiecărei izoforme la anorexia indusă de inflamație.
Găzduirea animalelor.
Șoarecii de tip sălbatic (WT), COX-1-deficient knockout (KO) (16) și COX-2 KO (26) au fost adăpostiți pe un ciclu de lumină-întuneric 12: 12-h cu acces ad libitum la chow-ul rozătoarelor, cu excepția cazului în care altfel indicat. Pentru studii cu inhibitori farmacologici, au fost evaluați șoareci masculi C3H/HeN (Harlan Sprague Dawley, Indianapolis, IN) cu vârsta cuprinsă între 10 și 12 săptămâni (11, 34). Șoarecii masculi COX-1 și COX-2 KO, evaluați la vârsta de 8-14 săptămâni, au fost de un fundal C57BL/6 × 129 învechit menținut de împerecherile femele KO masculine × heterozigote pentru alele COX-1 KO și heterozigote × heterozigote pentru alela COX-2 KO. Șoarecii martori desemnați „WT” pentru experimentele COX KO au fost WT și heterozigoți coechipieri care provin din împerecherile heterozigoți COX-2. Toate protocoalele mouse-ului au fost în conformitate cu liniile directoare ale Institutului Național de Sănătate (NIH) și au fost aprobate de Comitetul de îngrijire și utilizare a animalelor de la Washington University School of Medicine.
Anorexia indusă de LPS.
Măsurătorile plasmatice ale corticosteronului, leptinei, glucozei și IL-6.
Plasma pentru măsurarea corticosteronului, leptinei, glucozei și IL-6 a fost obținută de la șoareci masculi C3H/HeN găzduiți individual (n = 3-5 pentru fiecare grup) prin flebotomie retroorbitală rapidă în tuburi capilare heparinizate, cu un timp total de la prima manipulare a animalului până la finalizarea sângerării de maximum 30 s. Linia de bazăt = 0 probă a fost obținută la 1000 la șoareci hrăniți ad libitum. La 1400, șoarecilor li s-a administrat vehicul sau SC-236 prin gavaj, iar mâncarea a fost îndepărtată din cușcă pentru restul experimentului. Șoarecii au fost supuși injecției intraperitoneale a vehiculului sau LPS la 30 de minute după tratamentul vehiculului sau SC-236. Probele de sânge suplimentare au fost apoi colectate la 3 și 16 ore după injecția LPS la animalele postite. Sângele a fost colectat pe gheață, iar plasma a fost separată prin centrifugare și depozitată la -80 ° C până la testare. Concentrația plasmatică de corticosteron (ICN Biomedicals, Costa Mesa, CA) a fost determinată prin radioimunotest, așa cum s-a descris anterior (3, 13). Concentrațiile plasmatice de IL-6 (Pharmingen, San Diego, CA) și leptină (R&D Systems, Minneapolis, MN) au fost măsurate de ELISA conform instrucțiunilor producătorului. Concentrația de glucoză plasmatică a fost măsurată pe un analizor de glucoză din sânge HemoCue (HemoCue, Mission Viejo, CA).
Hibridizarea hipotalamică a ARNm in situ.
metode statistice.
Toate rezultatele sunt exprimate ca medii ± SE. Analiza statistică a fost realizată de ANOVA, cu P ≤ 0,05 considerat semnificativ.
FIG. 1.Inhibarea sintezei farmacologice a prostaglandinelor atenuează pierderea în greutate indusă de lipopolizaharidă (LPS). A: modificări ale greutății corporale după administrarea vehiculului (n = 7), indometacin (Indo, n = 4), sau inhibitori ai ciclooxigenazei (COX) izoform selectivin = 4-5) fără administrare LPS. B: modificări ale greutății corporale după administrarea vehiculului (n = 11), Indon = 5), sau inhibitori COX selectivi ai izoformei (n = 10-12) cu administrare LPS. Modificări semnificative statistic: zi (d) 1, P
Pentru a confirma în continuare efectele diferențiale ale COX-1- vs. Prostaglandinele derivate din COX-2 la scăderea în greutate după activarea imună sistemică, am evaluat șoarecii WT, COX-1 și COX-2 KO după administrarea LPS. Pentru aceste experimente, șoarecii femele au fost folosiți deoarece șoarecii masculi COX-2 KO au o mortalitate precoce (26), excluzând achiziția unui număr adecvat de bărbați adulți sănătoși COX-2 KO pentru studiile noastre. În conformitate cu experimentele de mai sus care utilizează inhibitori selectivi COX, șoarecii COX-2 KO au demonstrat o pierdere în greutate semnificativ mai mică decât șoarecii COX-1 KO la o zi după administrarea LPS (P 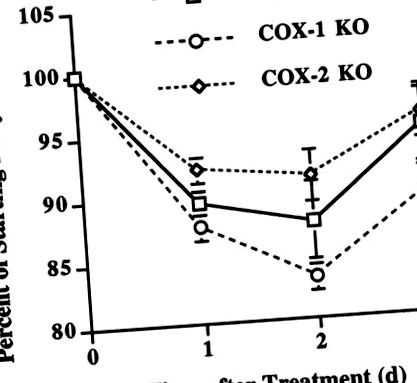
FIG. 2.Inhibarea sintezei genetice a prostaglandinelor atenuează pierderea în greutate indusă de LPS. Șoarecii COX-2 knockout (KO) au avut tendința de a pierde mai puțin în greutate decât șoarecii de tip sălbatic (WT) la 1 zi după administrarea LPSP = 0,08) și o scădere semnificativ mai mică în greutate decât șoarecii COX-1 KO atât pe o zi (P
Schimbările fie în aportul de energie, fie în utilizarea energiei ar putea contribui la atenuarea pierderii în greutate asociată cu inhibarea sau deficiența selectivă a COX-2. Pentru a evalua efectul inhibiției COX-2 asupra poftei de mâncare, am măsurat consumul de alimente la șoareci tratați cu LPS cu sau fără inhibare simultană a COX-2 de către SC-236 (Fig.3A). Administrarea numai a LPS a dus la o reducere de 60% a consumului de alimente, comparativ cu șoarecii tratați cu vehicul, în perioada de 24 de ore după inducerea activării sistemului imunitar sistemic. În schimb, administrarea SC-236 la animalele tratate cu LPS a atenuat răspunsul hipofagic, aportul de alimente crescând cu 50% comparativ cu șoarecii care primesc LPS singuri. În concordanță cu atenuarea pierderii în greutate după LPS, SC-236 a atenuat, dar nu a blocat complet, răspunsul hipofagic. În susținerea în continuare a observației că efectul SC-236 în reducerea pierderii în greutate depinde de menținerea consumului de alimente, mai degrabă decât de modificările în utilizarea energiei, șoarecii care au fost tratați cu vehicul sau SC-236 și apoi au postit 16 ore după administrarea LPS pierdere în greutate identică (Fig. 3B).
FIG. 3.Modificarea apetitului și a ratei metabolice după administrarea LPS cu inhibare COX-2. A: aport alimentar în perioada de 24 de ore după administrarea LPS. *P
Menținerea greutății corporale, a consumului de alimente și a stării nutriționale generale în cadrul infecției bacteriene acute sau al bolilor inflamatorii cronice ar fi un beneficiu substanțial pentru sănătate. Cu toate acestea, dacă menținerea aportului alimentar și a greutății corporale după LPS a avut loc ca o consecință a inhibării răspunsului citokinelor la inflamație, capacitatea organismului de a combate infecția și de a nu ceda la sepsis ar putea fi compromisă. Pentru a determina consecințele inhibării COX-2 asupra producției de citokine, am măsurat concentrația plasmatică de IL-6 după administrarea LPS. Producția normală de IL-6 ca răspuns la LPS necesită inducerea prealabilă atât a TNF-α cât și a IL-1β, iar IL-6 rămâne crescută pentru o perioadă prelungită, oferind un marker util pentru integrarea răspunsului citokinelor (1, 31, 40). După cum era de așteptat, IL-6 a crescut dramatic după administrarea LPS (Fig. 4A). Administrarea SC-236 împreună cu LPS nu a condus la nicio modificare a amplorii inducției timpurii a IL-6 măsurată la 3 ore după LPS sau la creșterile susținute ale IL-6 la 16 ore după LPS.
FIG. 4.Inducerea hormonului plasmatic după administrarea LPS.A: interleukină plasmatică (IL) -6 măsurători după administrarea LPSn = 3-5 pe grup).Ora 0 iar concentrațiile IL-6 vehicul/vehicul au fost sub limita de detectare a testului de 0,1 ng/ml. B: măsurători ale corticosteronului plasmatic după administrarea LPS (n= 4-5 per grup). *P
Ca dovadă suplimentară că specificitatea relativă a consecințelor inhibiției COX-2 după LPS a fost mai degrabă asupra răspunsului hipofagic decât asupra răspunsului global citokinic și inflamator, am evaluat activitatea axei hipotalamo-hipofizo-suprarenale. Stimularea eliberării glucocorticoidelor suprarenale în timpul inflamației reflectă acțiunile citokinelor la nivelul situsului nervos central, hipofizar și suprarenal și oferă o măsură utilă integrată de stimulare și amortizare a răspunsului inflamator (3, 5, 23, 38). Administrarea LPS a dus la creșterea marcată a concentrațiilor plasmatice de corticosteron la 3 ore, care a fost susținută la 16 ore după administrare (Fig. 4B). O mică creștere a corticosteronului plasmatic a fost observată la a 3-a oră la șoareci care nu au primit LPS, deoarece acest moment coincide cu vârful circadian normal în producția de glucocorticoizi. Nu a existat nicio diferență în amploarea sau durata activării suprarenalei la șoarecii tratați cu LPS și SC-236. În concordanță cu creșterea susținută a producției de glucocorticoizi suprarenali după LPS, mRNA CRH în nucleul paraventricular al hipotalamusului a fost crescut de aproximativ trei ori atât în grupurile LPS, cât și în grupurile SC-236/LPS (Fig. 5).
FIG. 5.Analiza de hibridizare in situ a hormonului hipotalamic de eliberare a corticotropinei (CRH) și a neuropeptidei Y (NPY).A: autoradiograme reprezentative ale secțiunilor coronare prin nucleul hipotalamic paraventricular (pvn) pentru CRH și nucleul arcuat (arc) pentru detectarea ARNm NPY. Imagini cu mărire redusă a secțiunilor coronale întregi (panourile din stânga pentru fiecare sondă) și imagini cu mărire mare a nucleilor paraventriculari sau arcuați pentru hibridizări CRH și respectiv NPY (panouri din cutie dreapta pentru fiecare sondă), sunt prezentate. Nucleul central al amigdalei (am) demonstrează, de asemenea, hibridizarea CRH mARN. V, vehicul. B: analiza densitometrică cantitativă a CRH și NPY in situ autoradiograme (n = 3 pe grup). *P
Pentru a determina dacă prostaglandinele generate de COX-2 au avut efecte directe asupra poftei de mâncare sau au acționat indirect asupra centrelor poftei de mâncare prin modularea neuropeptidelor sau a altor molecule, am măsurat mRNA NPY în nucleul arcuit al hipotalamusului și concentrația serică de leptină. În ciuda nivelurilor crescute de citokine și a inducerii neuropeptidei anorexice CRH (7), nivelurile de NPY nu au diferit la șoarecii care au primit sau nu au primit LPS (Fig. 5). În schimb, concentrația serică de leptină a fost mărită prin administrarea de LPS (Fig. 4C), în concordanță cu rapoartele anterioare (2, 12). Amploarea inducției leptinei nu a diferit între grupurile vehicul/LPS și SC-236/LPS. Glucoza plasmatică a scăzut ca răspuns la administrarea LPS, dar acest răspuns hipoglicemiant nu a diferit între grupurile vehicul/LPS și SC-236/LPS (Fig. 4D).
Datele prezentate în acest studiu demonstrează că blocarea selectivă farmacologică sau genetică a prostaglandinelor generate de COX-2 atenuează în mod eficient răspunsul hipofagic la inflamația sistemică indusă de LPS. Spre deosebire de alți agenți care atenuează anorexia provocată de inflamație, cum ar fi inhibitorul fosfodiesterazei pentoxifilină, blocantele canalelor de calciu și glucocorticoizii care blochează evenimentele proximale în răspunsul la LPS (17, 18, 30), medicamentele selective COX-2 scad anorexia fără a diminua răspunsul citokinei. Studiile anterioare au demonstrat că AINS pot crește, mai degrabă decât să scadă, evenimentele proximale ale răspunsului în timpul inflamației, cum ar fi inducerea TNF-α (25), iar datele noastre extind această analiză prin demonstrarea unei reduceri pe termen mediu și lung a Producția IL-6. Deoarece descoperim că inhibarea COX-2 nu modifică expresia neuropeptidelor anorexice precum CRH, neuropeptidele orexice precum NPY sau leptina după administrarea LPS, prostaglandinele generate de COX-2 sunt susceptibile de a modula în mod direct centrele centrale ale apetitului. Alternativ, COX-2 ar putea modula în mod indirect apetitul prin acțiune pe una dintre mai multe căi de neuropeptide care nu au fost evaluate în prezentul studiu.
Mulțumim Dr. Scott Morham pentru furnizarea șoarecilor COX-1 KO și COX-2 KO, Monsanto-Pharmacia pentru furnizarea SC-236 și SC-560, Laboratorul de bază al Centrului de cercetare și formare a diabetului pentru măsurarea leptinei și Dr. J. Gitlin, D. Rudnick și K. Bethin pentru analiza manuscriselor.
NOTĂ DE PICIOASĂ
Această lucrare a fost susținută de subvenții din cadrul programului de cercetare biomedicală Monsanto-Pharmacia/Washington University și March of Dimes (către L. J. Muglia) și Institutul Național de Granturi de Instruire în Imunologie a Sănătății 5 T32 HD-07507 (către P. M. Johnson).
Adresa pentru cereri de reimprimare și alte corespondențe: L. J. Muglia, Washington Univ. Școala de Medicină, 660 S. Euclid Ave., Box 8208, St. Louis, MO 63110 (E-mail: [email protected] wustl. Edu).
- Extrem de acalazie care se prezintă ca anorexie nervoasă
- De la anorexie la bulimie până la recuperare, un cont personal al unei călătorii imperfecte de Maria Mutia
- Tulburări de alimentație Anorexia nervoasă (auto-înfometare; malnutriție; scădere extremă în greutate) Sănătate Motor
- Luptați împotriva inflamației cu acest curcum și elixir de dimineață de lămâie
- Sportivele de sex feminin cu mult de pierdut sănătatea Bătăile ascunse ale anorexiei și bulimiei devin
