Diana E. Pankevich
Departamentul de Biologie Animală, Universitatea din Pennsylvania, Philadelphia, Pennsylvania 19104
Sarah L. Teegarden
Departamentul de Biologie Animală, Universitatea din Pennsylvania, Philadelphia, Pennsylvania 19104
Andrew D. Hedin
Departamentul de Biologie Animală, Universitatea din Pennsylvania, Philadelphia, Pennsylvania 19104
Catherine L. Jensen
Departamentul de Biologie Animală, Universitatea din Pennsylvania, Philadelphia, Pennsylvania 19104
Tracy L. Bale
Departamentul de Biologie Animală, Universitatea din Pennsylvania, Philadelphia, Pennsylvania 19104
Abstract
Introducere
Dietele ca mod de modificare a comportamentului în gestionarea greutății s-au dovedit a avea puțin succes pe termen lung, cu o rată de eșec> 80% (Wing și Phelan, 2005). Greutatea ridicată recâștigă și crește riscul de diabet și boli metabolice asociate după dietă, fac identificarea unor ținte terapeutice noi critice (Lissner și colab., 1991; Brownell și Rodin, 1994; Guagnano și colab., 2000). Tratamentele actuale se concentrează în principal pe reducerea poftei de mâncare, deși se știe mai puțin în ceea ce privește mecanismele centrale care contribuie la rezistența și eșecul tratamentului, în special la implicarea căilor de stres.
Deoarece stresul și hormonul stresului factorul de eliberare a corticotropinei (CRF) sunt promotori cunoscuți ai consumului crescut de alimente dense caloric, reprogramarea circuitelor de stres poate fi un mecanism central care determină o dietă repetată sau efectul „yo-yo”, rezultând o creștere risc pentru creșterea în greutate mai mare și obezitate ulterioară (Epel și colab., 2001; Dallman și colab., 2006; Amigo și Fernández, 2007; Teegarden și Bale, 2008). Activarea indusă de stres a axei de stres hipotalamo-hipofizo-suprarenală (HPA) și eliberarea CRF crește comportamentele de căutare a recompensei (Dallman și colab., 2005; Ghitza și colab., 2006). Antagonismul CRF în nucleul de pat al striei terminale (BNST) scade restabilirea medicamentului indus de stres, în timp ce injecția CRF promovează căutarea de droguri, demonstrând o intersecție a căilor de stres și recompensă (Erb și Stewart, 1999; Koob, 2009). Dovezile din aceste studii și din alte studii sugerează că stresul joacă un rol critic în creșterea comportamentului consumator al substanțelor recompensatoare, inclusiv a alimentelor dense caloric (Shaham și colab., 2000; Sinha, 2001; Wang și colab., 2005; Dallman și colab., 2006 Teegarden și Bale, 2008).
Am emis ipoteza că experiența anterioară de restricție ar produce modificări în neurocircuitarea stresului, ducând la o sensibilitate la stres crescută ulterior și la tendința de a consuma în exces alimente bogate în grăsimi. Pentru a examina această ipoteză, am comparat răspunsurile la stres fiziologic și comportamental într-un model de restricție calorică la șoarece care produce o reducere cu 10-15% a greutății corporale, niveluri tipice de scădere în greutate umană în timpul dietei (Redman și colab., 2007; Sarwer și colab. ., 2009). Au fost determinate impactul pe termen lung și efectul de programare al acestei restricții moderate asupra măsurilor comportamentale și a reacției la stres. Din punct de vedere mecanic, s-a examinat expresia CRF și metilarea promotorului. În plus față de reducerea caloriilor, o componentă majoră a dietei umane este scăderea conținutului de grăsimi și a gustului dietei. Am demonstrat anterior la șoareci că retragerea dintr-o dietă bogată în grăsimi crește starea relativă de stres și promovează comportamentele de reintegrare în care șoarecii selectează un mediu aversiv pentru a avea acces la dieta preferată bogată în grăsimi (Teegarden și Bale, 2007). Prin urmare, am comparat în mod similar expresia CRF și modelele de metilare până la 8 săptămâni după retragerea dintr-o dietă bogată în grăsimi, demonstrând programarea pe termen lung care are loc.
Pentru a explora impactul comportamental al modificărilor epigenetice în circuitele de stres asupra consumului de alimente, am examinat consumul excesiv al unei diete bogate în grăsimi după stres cronic la șoareci restricționați anterior. În plus, a fost evaluată sensibilitatea la un antagonist al receptorului-1 al hormonului concentrator de melanină (MCH) asupra acestui comportament. Împreună, aceste rezultate pot oferi noi direcții terapeutice prin care sunt concepute tratamente mai eficiente și mai durabile de gestionare a greutății.
Materiale și metode
Animale
Toți șoarecii din aceste studii au fost bărbați (C57BL/6J; vârsta de 7-8 săptămâni) obținuți de la laboratorul Jackson și găzduiți individual pe un program de 12 ore de lumină/întuneric cu hrană și apă disponibile ad libitum, cu excepția cazului în care se menționează altfel. Chow-ul de casă conținea 28% proteine, 60% carbohidrați și 12% grăsimi în calorii și 4,00 kcal/g (dieta Purina Lab). Dieta bogată în grăsimi conținea 20% proteine, 35% carbohidrați și 45% grăsimi în calorii și 4,73 kcal/g (Research Diets). Această dietă este foarte preferată pentru a adăposti chow la șoareci C57BL/6J (Teegarden și Bale, 2007). Toate studiile au fost făcute în conformitate cu resursele pentru animale de laborator ale Universității din Pennsylvania și cu standardele și orientările Comitetului instituțional de îngrijire și utilizare a animalelor.
Restricție calorică
Consumul mediu zilnic de alimente a fost stabilit peste 10 zile. Șoarecii au fost repartizați aleatoriu cu restricție calorică (Rstr), 75% din aportul caloric mediu sau grupuri de tratament ad libitum (Rstr, n = 41; ad libitum, n = 37). Această reducere a fost selectată pentru a produce 10-15% pierderea în greutate corporală pentru a imita regimurile dietetice tipice la om. Pentru grupurile restricționate, peletele de chow preweighed de casă au fost plasate în cuști cu 2,5 ore înainte de stingerea luminilor timp de 21 de zile. Acest program a fost folosit pentru a se asigura că șoarecii au acces la alimente înainte și după ce se aprind când se produce majoritatea consumului de alimente și pentru a evita oscilatoarele antrenate de alimente, permițând consumul în timpul fazei întunecate (Mendoza, 2007). Greutățile corporale au fost înregistrate la fiecare 2-3 zile.
Leptina
Pentru a determina impactul restricției calorice și al alimentării cu diete bogate în grăsimi sau chow asupra nivelului de leptină, a fost obținută o probă de sânge la momentul uciderii într-un subset de șoareci (ad libitum, n = 11; Rstr, n = 12). Probele au fost centrifugate, iar plasma a fost colectată și congelată la -80 ° C până la analiză. Nivelurile plasmatice au fost măsurate prin setul de radioimunotest pentru leptină (LINCO Research). Protocolul a fost modificat pentru a utiliza 50 μl de plasmă pentru fiecare test și fiecare probă a fost evaluată în duplicat. Coeficientul de variație intra-test a fost (−ΔCT) pentru fiecare probă și a normalizat fiecare valoare la media pentru controlul chow.
Analiza metilării ADN-ului.
Au fost analizate impactul restricției calorice, al alimentării cu chow sau al sevrajului cu conținut ridicat de grăsimi asupra stării de metilare a dinucleotidelor CpG specifice din regiunea promotor a CRF de șoarece (McGill și colab., 2006). ADN-ul genomic din CeA și BNST a fost izolat din micropunches. Pe scurt, țesutul a fost adăugat direct la tamponul de extracție a ADN-ului cu greutate moleculară mare (1 m Tris-HCI, EDTA, SDS și apă) plus RNază A și incubat timp de 1 oră la 37 ° C, urmat de adăugarea proteinazei K și incubare peste noapte la 55 ° C. Apoi, s-a efectuat o extracție cloroform/alcool izoamilic înainte ca ADN-ul să fie precipitat cu acetat de sodiu și glicogen la -80 ° C timp de 1 oră urmat de centrifugare (10 min, 12.000 rpm, temperatura camerei). Peleta a fost salvată și resuspendată în tampon TE. Pirosequencing-ul a fost efectuat de EpigenDx așa cum s-a descris anterior (Kim și colab., 2007; Liu și colab., 2007). Pe scurt, s-a efectuat modificarea bisulfatului, transformând citozina nemetilată în uracil. Secvența promotor pentru gena CRF a fost amplificată prin PCR și produsul biotinilat purificat pentru pirozecvențiere. Primerii specifici site-ului au fost proiectați pentru a determina starea de metilare a dinucleotidelor CpG.
Mâncarea excesivă indusă de stres
Inversarea renunțării la o dietă bogată în grăsimi a indus consumul excesiv
analize statistice
Diferențele în greutate și nivelurile plasmatice de leptină au fost analizate fie prin testul t Student, fie prin ANOVA unidirecțional. Datele despre corticosteron au fost analizate folosind ANOVA cu măsuri repetate bidirecționale pentru restricție și timp. Pentru TST, datele au fost analizate folosind testul t Student. Pentru expresia genei CRF după restricție calorică sau retragere cu conținut ridicat de grăsimi, datele au fost analizate utilizând un ANOVA unidirecțional cu teste post-hoc Fisher's PLSD. Datele de metilare au fost analizate folosind un ANOVA unidirecțional pentru a determina diferența dintre grupurile din cadrul fiecărui sit GpC și metilarea generală a promotorului. Pentru consumul de 10 d binge consumat de stres, datele au fost analizate folosind un ANOVA cu măsuri repetate unidirecționale cu grupuri de control și CVS analizate separat. Datele privind aportul caloric total în timpul consumului excesiv au fost analizate folosind testul t Student. Pentru analiza expresiei genice a hormonilor orexigenici, modificările de ori au fost calculate în raport cu controalele ad libitum chow și s-a utilizat un ANOVA bidirecțional cu testele post-hoc Fisher's PLSD. Pentru inversarea consumului excesiv de induse de retragere cu conținut ridicat de grăsimi, datele din primele 3 zile au fost analizate folosind un ANOVA cu măsuri repetate unidirecționale, iar datele din a patra zi au fost analizate folosind un ANOVA bidirecțional cu teste post-hoc Fisher's PLSD . Toate analizele statistice au fost efectuate folosind SigmaStat (Systat Software).
Rezultate
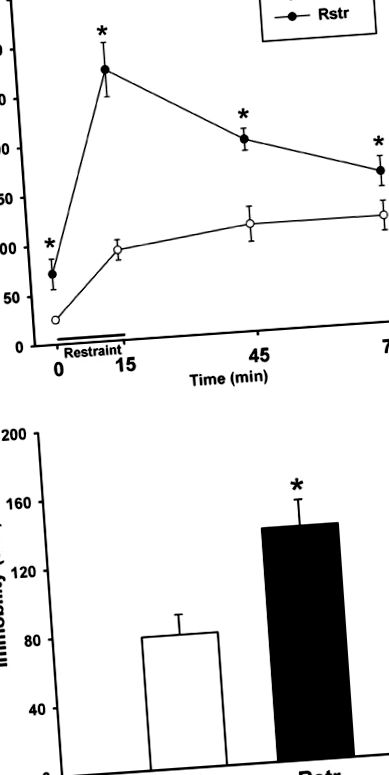
Restricția calorică a indus sensibilitatea la stres
Greutăți corporale și leptină
Șoarecii masculi restricționați caloric la 75% din aportul normal de chow prezintă o pierdere semnificativă în greutate la sfârșitul celor 3 săptămâni de restricție. În perioada de 3 săptămâni, șoarecii martor au câștigat în greutate (t (20) = -4.294; p ≤ 0,001), în timp ce șoarecii restrânși au pierdut în greutate (t (22) = 8,214; p ≤ 0,001); astfel, la sfârșitul restricției, greutățile au fost semnificativ diferite (t (21) = 11,815; p ≤ 0,001). Nivelurile de leptină plasmatică au fost măsurate dintr-un subset de șoareci uciși la sfârșitul perioadei de restricție de 3 săptămâni. Șoarecii cu restricții calorice au prezentat niveluri semnificativ mai mici de leptină (t (8) = 2,715; p = 0,03) (Tabelul 1).
tabelul 1.
Greutăți corporale și niveluri de leptină după restricție calorică
| Ad libitum | 25,7 ± 0,2 | 27,3 ± 0,3 | 10,4 ± 1,1 |
| Rstr | 26,3 ± 0,3 | 22,7 ± 0,3 * | 7,0 ± 0,5 * |
Expresie CRF
Reprogramarea retragerii bogate în grăsimi a căilor de stres
Expresie CRF
Mâncarea excesivă indusă de stres
Greutăți corporale
După restricție calorică, șoarecii martor au cântărit semnificativ mai mult decât șoarecii cu restricție calorică (t (34) = 6,971; p ≤ 0,001). După 3 săptămâni de restricție, șoarecii au fost așezați din nou pe chit ad libitum (reîncărcare) până când diferența semnificativă de greutate dintre șoareci martor și restrânși nu a mai fost prezentă înainte de începerea accesului limitat pentru a se asigura că diferențele de aport nu au fost atribuite diferențelor de greutate. Greutățile au fost monitorizate continuu și în timpul accesului limitat și nu au existat diferențe semnificative în timpul sau la sfârșitul acestor studii (Tabelul 2).
masa 2.
Greutăți corporale după consumul excesiv de grăsimi
| Ad libitum | 24,5 ± 0,3 | 26,9 ± 0,4 | 27,4 ± 0,3 |
| Rstr | 23,0 ± 0,3 * | 26,6 ± 0,4 | 27,1 ± 0,4 |
* Efectul restricției calorice (p ≤ 0,001).
Acces limitat
Tabelul 3.
Greutăți corporale după 1 săptămână ad libitum cu conținut ridicat de grăsimi
| Ad libitum | 24,9 ± 0,4 | 26,7 ± 1,1 |
| Rstr | 23,8 ± 0,2 * | 27,5 ± 0,5 |
* Efectul restricției calorice (p Fig. 5 A). Analiza expresiei genei orexinei a relevat o interacțiune între restricție și dietă (F (1,12) = 16,577; p Fig. 5 B).
Reducerea anterioară a caloriilor îmbunătățește semnificativ răspunsurile hormonului orexigen la dieta bogată în grăsimi. A, Nivelurile de MCH în LH au crescut semnificativ la șoarecii cu restricții calorice alimentate cu o dietă bogată în grăsimi, comparativ cu șoarecii ad libitum alimentați cu grăsimi bogate (n = 4-5) (* p Fig. 6). Restricția calorică anterioară nu a crescut aportul de chow (Fig. 6 C) sau aportul caloric total (Fig. 6 E). Nu a existat niciun efect al vreunui medicament asupra aportului caloric bogat în grăsimi în a patra zi de acces limitat; cu toate acestea, efectul restricției a rămas la șoarecii restricționați anterior din punct de vedere caloric, având un aport caloric mai mare de pelete bogate în grăsimi în comparație cu martorii (F (1.41) = 9.072; p Fig. 6 B). Consumul de chow de 24 de ore a fost semnificativ modificat prin tratamentul medicamentos (F (2.41) = 3.678; p Fig. 6 D). Aportul caloric total de 24 de ore a fost modificat semnificativ prin tratamentul medicamentos (F (2.41) = 4.128; p Fig. 6 F).
- Restricție calorică și regenerare musculară Harvard Stem Cell Institute (HSCI)
- Restricția calorică inversează inflamația glandei mamare indusă de obezitate la șoareci - PubMed
- Binge Eating și Secret Mâncare; Nutri Low Down
- Restricția de calorii Mâncați mai puțin face ca maimuțele să trăiască mai mult timp
- O dependență de social media este ca și cum ai mânca în exces