Departamentul de farmacologie, Universitatea din Melbourne, Parkville, Victoria 3010, Australia
Departamentul de farmacologie, Universitatea din Melbourne, Parkville, Victoria 3010, Australia
Departamentul de Biochimie și Biologie Moleculară, Universitatea Monash, Clayton, Victoria 3800, Australia
Departamentul de farmacologie, Universitatea din Melbourne, Parkville, Victoria 3010, Australia
Departamentul de farmacologie, Universitatea din Melbourne, Parkville, Victoria 3010, Australia
Departamentul de Biochimie și Biologie Moleculară, Universitatea Monash, Clayton, Victoria 3800, Australia
Abstract
Impactul cardiovascular al obezității
Obezitatea este o problemă de sănătate a prevalenței în creștere pe fiecare continent și reprezintă o problemă majoră de sănătate publică. În timp ce multe studii indică faptul că obezitatea este un factor major de risc pentru morbiditatea și mortalitatea cardiovasculară, relația dintre obezitate și hipertensiune este neclară și ar putea reflecta factori genetici, de mediu, hormonali și hemodinamici (Redon, 2001).
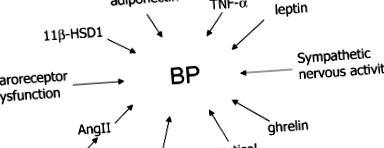
Așa cum se arată în FIG. 1, alți hormoni circulanți și mediatori produși de țesutul adipos, au potențialul de a regla tensiunea arterială prin modularea tonusului vascular sau a volumului intravascular (Lyon și colab. 2003; Rajala & Scherer, 2003; Fruhbeck, 2004). Adipocitokinele, cum ar fi adiponectina, care este redusă în obezitatea umană, interleukina-6 (Il-6) și factorul de necroză tumorală α (TNF-α) eliberată din țesutul adipos, pot contribui la disfuncția endotelială, crescând astfel riscul de ateroscleroză și colab. 2003). În plus, enzima 11β-hidroxisteroid dehidrogenază tip 1 (11β-HSD1) și angiotensinogenul sunt exprimate de țesutul adipos și acestea pot juca un rol cheie în riscul cardiovascular asociat cu obezitatea viscerală. 11β - HSD1 transformă cortizonul în forma sa activă, cortizolul. Șoarecii transgenici care supraexprimă 11β - HSD1 în țesutul adipos au hipertensiune însoțită de acumularea de grăsime viscerală și rezistență la insulină și leptină (Masuzaki și colab. 2003).
Obezitatea este asociată cu modificări ale hormonilor și mediatorilor derivați din țesutul adipos, care pot afecta tensiunea arterială (TA) și funcția vasculară Activarea simpatică și disfuncția baroreceptorului au un impact asupra TA. Leptina din țesutul adipos, insulina și angiotensina II (AngII) poate crește activitatea simpatică, crescând astfel TA. 11β - hidroxisteroid dehidrogenază de tip 1 (11β - HSD1) derivat din adipoză promovează conversia cortizonului în cortizol activ. Reducerea adiponectinei derivate din adipoză și creșterea interleukinei 6 (IL-6) și a factorului de necroză tumorală α (TNF-α) ar favoriza ateroscleroza. Grelina poate influența reglarea TA, deoarece s-a demonstrat că exercită efecte depresive în SNC.
Obezitate la debutul adulților
Pentru a investiga legătura dintre obezitate și hipertensiune, laboratorul nostru a dezvoltat diete gustoase cu conținut ridicat de grăsimi pentru rozătoare care pot fi aplicate la vârsta adultă tânără, permițându-ne să examinăm consecințele cardiovasculare/metabolice ale supraalimentării voluntare (Hansen și colab. 2001, 2004). Grupuri de șobolani masculi (200 g) potrivite în funcție de greutate au primit chow standard (12% calorii sub formă de grăsime) sau o dietă foarte gustoasă în stil cafenea (constând din chow suplimentat, plăcinte cu carne, paste și prăjituri, 30% calorii ca grăsime; și colab. 2004). Animalele pot fi urmărite pentru diferite perioade de intervenție dietetică (Hansen și colab. 2001, 2004). Măsurătorile tensiunii arteriale prin pletismografie, precum și probele de sânge ale venei cozii, sunt luate la intervale regulate. În timp ce greutatea corporală, masa grasă și leptina plasmatică cresc imediat după implementarea dietei (Hansen și Morris, 2002), creșterea tensiunii arteriale devine evidentă doar după aproximativ 10 săptămâni. Nivelurile NPY hipotalamice au scăzut odată cu hrănirea cronică cu conținut ridicat de grăsimi și am observat corelații negative semnificative între NPY hipotalamic total și leptina plasmatică (Hansen și Morris, 2002).
Obezitate infantila
Obezitatea la copii este, de asemenea, în creștere în întreaga lume (Kohn & Booth, 2003; Slyper, 2004) și datele demografice sugerează că sunt implicate influențele de mediu care funcționează devreme în viață. Obezitatea infantilă este asociată cu hiperlipidemie ulterioară, intoleranță la glucoză și hipertensiune (Caprio și colab. 1996). Multe dintre consecințele cardiovasculare care caracterizează obezitatea la adulți sunt precedate de anomalii care încep în copilărie. Gestionarea obezității infantile și a consecințelor acesteia necesită înțelegerea schimbărilor fiziopatologice care stau la baza obezității cu debut precoce. La rozătoare, reducerea dimensiunii deșeurilor postnatal crește disponibilitatea alimentelor și este utilizată pentru a studia consecințele supranutriției timpurii (Plagemann și colab. 1999). În secțiunea următoare descriem studiile din laboratorul nostru în care am investigat consecințele metabolice și cardiovasculare pe termen lung ale supraalimentării preîncărcării, care până în prezent au fost puțin examinate.
Pe lângă examinarea impactului cronic al unei perioade scurte de supraalimentare (folosind ajustarea deșeurilor), am examinat și impactul supranutriției continue de la naștere, indus de dimensiunea redusă a așternutului urmată de o dietă bogată în grăsimi.
Modelarea obezității cu debut precoce
Reglarea deșeurilor
Metodele utilizate pentru modelarea supra-alimentației cu debut precoce sunt prezentate în Fig. 2. În ziua 1 de viață, puii de șobolan au fost ajustați la 3 (așternut mic) sau 12 animale masculi (așternut normal) cu greutăți corporale similare, pentru a induce supranutriție postnatală timpurie sau, respectiv, nutriție normală. Animalele din litiere mici erau semnificativ mai grele decât cele din litiere normale până în ziua 14 (41,1 ± 0,8 contra 32,9 ± 0,5 g, P
Protocol experimental de intervenție nutrițională timpurie Mărimea așternuturilor este ajustată la 12 pui (martor) și 3 pui (supranutriți) pe mamă. La înțărcare, șobolanii au ad libitum acces la o dietă plăcută cu conținut ridicat de grăsimi (30% calorii sub formă de grăsime) sau o dietă standard de chow (12% calorii sub formă de grăsime). Greutatea corporală, aportul alimentar și tensiunea arterială sunt măsurate la intervale regulate și se analizează neuropeptida hipotalamică Y, hormonii plasmatici și mediatorii derivați de adipoză.
Concentrațiile plasmatice de leptină la înțărcare, la vârsta de 8 și 16 săptămâni (A) și expresia ARNm 11β - HSD1 în țesutul adipos alb retroperitoneal (B) la vârsta de 16 săptămâni la șobolani de la hrană normală (□) și cu puiet mic (▪) Rezultatele sunt exprimate ca mijloace ± s.e.m. a expresiei relative a 11β - HSD1 la GAPDH. Datele au fost analizate folosind studiile nepereche t Test. *P
În timp ce greutatea corporală nu a rămas semnificativ crescută la 16 săptămâni după supraalimentare ca pui, am observat în mod constant o greutate corporală cu 5% mai mare la șobolanii crescuți în puieturi mici; în funcție de cohorta specială, s-au observat creșteri modeste ale tensiunii arteriale a coamei de la 10 mmHg. Pe baza populației, modificări relativ mici, cum ar fi acestea, pot fi relevante pentru bolile cardiovasculare.
Ajustarea deșeurilor, urmată de o dietă normală sau bogată în grăsimi
Într-un studiu ulterior, la înțărcare (ziua 24), puii cu ambele dimensiuni ale așternutului au fost împărțiți în grupuri care au primit chow standard (12% calorii sub formă de grăsime) sau dietă bogată în grăsimi (30% calorii sub formă de grăsimi; vezi Fig. 2). Animalele crescute în litiere mici au fost semnificativ mai grele decât cele din litiere normale, indiferent de dieta lor (Fig. 4A; Velkoska și colab. 2005). Cu toate acestea, de la vârsta de 11 săptămâni nu a existat un efect semnificativ al dimensiunii așternutului asupra greutății corporale (Fig. 4A). Leptina plasmatică a fost crescută la animalele de la scaunele mici, comparativ cu cele din scuturile normale la vârsta de 8 săptămâni, indiferent de dieta lor după înțărcare (Fig. 4B), sugerând că supraalimentarea precoce are efecte de lungă durată asupra grăsimii corporale. La vârsta de 16 săptămâni, greutatea organelor și masa de grăsime a animalelor din așternuturile mici au avut tendința de a fi ușor mai grele decât cele din așternuturile normale, dar aceste diferențe nu au atins importanță și colab. 2005). Din nou, a existat o creștere modestă a greutății corporale de 4-5% a așternutului în ambele grupuri de dietă.
Greutatea corporală și concentrațiile plasmatice de leptină după înțărcare A, greutatea corporală după înțărcarea șobolanilor din așternut normal hrănit (NC, n= 11; □), gunoi normal hrănit cu conținut ridicat de grăsimi (NF, n= 11; ▪), hrană mică pentru așternut (SC, n= 12; ○) și deșeuri mici alimentate cu conținut ridicat de grăsimi (SF n= 10; •). Datele au fost analizate de ANOVA cu două căi, cu măsuri repetate urmate de post hoc test de diferență cel mai puțin semnificativ. B, concentrațiile plasmatice de leptină până la vârsta de 16 săptămâni în NC (bar deschis), SC (bară ușor umbrită), NF (bară umbrită mai închisă) și SF (bară umplută). Datele au fost analizate cu ANOVA bidirecțională urmată de post hoc Testul Bonferroni. Rezultatele sunt exprimate ca mijloace ± s.e.m. †P Velkoska și colab. (2005); folosit cu permisiunea.
Așa cum am observat în cazul alimentării cu conținut ridicat de grăsimi cu debut la adulți, greutatea corporală a crescut în decurs de 2 săptămâni de la punerea în aplicare a dietei bogate în grăsimi după înțărcare (Fig. 4A), iar greutatea corporală a rămas mai mare la animalele hrănite cu o dietă bogată în grăsimi pe tot parcursul studiului (Fig. 4A). La vârsta de 16 săptămâni, șobolanii cu hrană bogată în grăsimi din ambele grupuri de așternut erau cu 20% mai grei decât omologii lor hrăniți cu chow și consumau de două ori mai multă energie (Velkoska și colab. 2005). Chiar și după standardizarea greutății corporale, șobolanii cu conținut ridicat de grăsimi aveau mai mult țesut adipos (Velkoska și colab. 2005). Similar cu obezitatea alimentară cu debut la adulți (Hansen și colab. 2004), ingerarea unei diete bogate în grăsimi după înțărcare a dus la o dublare a leptinei plasmatice de la vârsta de 8 săptămâni; dieta de 4-5 săptămâni; Fig. 4B).
Creșterile legate de dietă ale tensiunii arteriale sistolice par a fi întârziate față de creșterea greutății corporale și a leptinei plasmatice. În timp ce tensiunea arterială a fost similară în toate grupurile de tratament la vârsta de 7 săptămâni, creșterea tensiunii arteriale de 11-20 mmHg a fost evidentă în ambele grupuri cu conținut ridicat de grăsimi în raport cu martorii hrăniți cu chow la 13 săptămâni (Velkoska și colab. 2005). Când s-au combinat șobolani cu conținut ridicat de grăsimi și șobolanii cu dietă chow, tensiunea arterială a fost corelată pozitiv cu leptina plasmatică și insulina plasmatică la vârsta de 13 săptămâni în fiecare grup de așternut (Velkoska și colab. 2005). Reduceri semnificative ale NPY hipotalamic (inclusiv PVN) au fost observate la 16 săptămâni ca răspuns la dieta bogată în grăsimi. În plus, o corelație negativă semnificativă a fost evidentă între leptină și NPY hipotalamic total în ambele grupuri de mărime a așternutului (Velkoska și colab. 2005).
Impactul supranutriției timpurii
Deși se sugerează că supranutriția în perioadele critice de dezvoltare conferă un risc crescut de obezitate ulterioară și tulburări metabolice, relația dintre momentul apariției supraalimentării și riscul obezității este neclară. În mâinile noastre, supranutriția postnatală indusă de dimensiunea redusă a așternutului a dus la modificări timpurii ale greutății corporale, cel mai probabil legate de creșterea consumului de lapte. Acest impact al dimensiunii mici a așternutului pentru a crește greutatea corporală a fost menținut pentru o perioadă până la vârsta adultă tânără (10 săptămâni), în conformitate cu studiile anterioare (Faust și colab. 1980; Plagemann și colab. 1999), care a arătat creșterea masei grase și a numărului de celule grase ca urmare a supranutriției timpurii. Munca noastră demonstrează dezvoltarea unei hiperleptinemii marcate la animale la puști mici, împreună cu creșterea mai mare în greutate corporală. De asemenea, este posibil ca efectele timpurii ale mediului legate de modificarea dimensiunii puilor, cum ar fi interacțiunea alterată mamă-pui, să aibă impact asupra comportamentului ulterior și asupra răspunsului la stres. Lucrările anterioare au arătat că manipularea puilor a dus la creșterea îngrijirii materne (lins și îngrijire) și că acest lucru a fost asociat cu o reacție hipotalmo-hipofizară-suprarenală amortizată la stres ca adulți (Liu și colab. 1997).
De asemenea, am examinat efectul prelungirii supraalimentării cu debut precoce prin supunerea animalelor la o dietă bogată în grăsimi după înțărcare. Indiferent de dimensiunea deșeurilor, dieta bogată în grăsimi a dus la o creștere semnificativă a greutății corporale comparativ cu dieta chow după doar 2 săptămâni. Am observat hiperleptinemia și hiperinsulinemia induse de dietă, precum și creșteri semnificative ale masei grase. Aceste descoperiri demonstrează că hrănirea pe termen lung a unei diete bogate în grăsimi poate înlătura efectele precoce ale induse de dimensiunea deșeurilor, indicând importanța supranutriției în viața ulterioară (Velkoska și colab. 2005). Cu toate acestea, animalele crescute în litiere mici au rămas moderat mai grele decât cele crescute în litiere normale de-a lungul maturității, deși acest lucru nu a reușit să atingă semnificație. Acest lucru sugerează că nutriția timpurie poate juca în continuare un rol mic, dar important.
Ce leagă obezitatea și tensiunea arterială?
Ajustarea dimensiunii așternutului la șobolani, influențând astfel tiparele de hrănire timpurie, poate influența tensiunea arterială a adulților (Myers și colab. 1996; Plagemann și colab. 1999), la fel și tipul de dietă. Am privit această întrebare în două moduri. În primul rând, punerea în aplicare a unei diete bogate în grăsimi (fie ca adult, fie la înțărcare) a dus la creșteri precoce și marcate ale greutății corporale și ale concentrațiilor de leptină; acestea au fost asociate cu creșteri modeste ale tensiunii arteriale sistolice care s-au manifestat după câteva luni. În al doilea rând, supraalimentarea șobolanilor pentru o perioadă limitată de la o vârstă foarte fragedă (ziua 1-24) a dus, de asemenea, la creșteri prelungite ale greutății corporale, iar concentrațiile de leptină au rămas crescute mult timp după ce o dietă normală a fost pusă în aplicare după înțărcare. Efectul supranutriției pe termen scurt, indus de reducerea dimensiunii deșeurilor, asupra tensiunii arteriale necesită investigații suplimentare în studii adecvate.
O altă considerație importantă este distribuția țesutului adipos la subiecții obezi. S-a dovedit că obezitatea centrală este asociată cu o activare simpatică mai mare în raport cu obezitatea periferică, cu afectarea echivalentă a controlului baroreflex (Grassi și colab. 2004). Un alt raport nu a constatat nicio creștere a activității nervoase simpatice musculare la bărbații cu obezitate subcutanată (Alvarez și colab. 2004) în ciuda concentrațiilor crescute de leptină. Este intrigant mecanismul prin care depunerea regională de grăsime conferă riscuri cardiovasculare diferite. Într-un studiu anterior am observat creșterea nivelurilor de mARN de 11β - HSD1 în țesutul adipos alb retroperitoneal la șobolani adulți care au fost supra-hrăniți ca pui tineri (Velkoska și colab. 2005). S-a speculat că producția crescută de glucocorticoizi ca urmare a creșterii ARNm 11β - HSD1 în țesutul adipos la oamenii obezi poate influența acumularea de grăsime (Rask și colab. 2002).
Copiii care au o masă corporală mai mare sunt mai predispuși să devină adulți obezi și prezintă un risc mai mare de a dezvolta tulburări cardiovasculare (Gunnell și colab. 1998; Jeffreys și colab. 2003). Șobolanii supraalimentați de la vârste fragede au dezvoltat o creștere a greutății corporale, împreună cu modificări ale mediatorilor implicați atât în reglarea hrănirii, cât și a tensiunii arteriale. Sunt necesare cercetări suplimentare pentru a ne spori înțelegerea mecanismelor care stau la baza dezvoltării tensiunii arteriale crescute în obezitate.
- Obezitatea centrală este asociată cu infecția cu helicobacter pylori, cu o secțiune transversală la scară largă
- Efectele antiinflamatorii ale melatoninei în obezitate și hipertensiune SpringerLink
- Obezitatea abdominală definită ca o circumferință a taliei mai mare decât era de așteptat este asociată cu rasetetica
- Dincolo de adipozitatea centrală Grăsimea hepatică și zona de grăsime viscerală sunt asociate cu sindromul metabolic în
- Există tulburări sau afecțiuni asociate cu obezitatea; supraponderal NICHD - Eunice Kennedy