1 Departamentul de Neurologie, Spitalul General Kuala Lumpur, Jalan Pahang, 50586 Kuala Lumpur, Malaezia
2 Unitate de diagnostic molecular și proteine, Institutul de Cercetări Medicale (IMR), Jalan Pahang, 50586 Kuala Lumpur, Malaezia
3 Departamentul de genetică, Spitalul general Kuala Lumpur, Jalan Pahang, 50586 Kuala Lumpur, Malaezia
4 Departamentul de patologie, Universitatea din Malaya, Lembah Pantai, 50603 Kuala Lumpur, Malaezia
Abstract
Boala Pompe (deficit de acid maltazic, boală de depozitare a glicogenului tip II) este o tulburare autozomală recesivă cauzată de un deficit de acid lizozomal
1. Introducere
Boala de depozitare a glicogenului de tip II (boala Pompe) este o boală de depozitare lizozomală autozomală recesivă cauzată de un deficit de acid α-1,4-glucozidază (GAA; maltază acidă, EC; 3.2.1.20/3), care este o enzimă cheie în hidroliza glicogenului lizozomal în glucoză. Persoanele afectate vor avea o acumulare excesivă de glicogen în lizozomi și citoplasmă a tuturor țesuturilor, mai ales în mușchii scheletici. Boala Pompe are un spectru larg de prezentări clinice. Cele 3 forme clinice majore sunt debutul infantil, juvenil și adult. Forma infantilă se caracterizează prin miopatie proximală rapidă și cardiomiopatie. Insuficiențele respiratorii și cardiace sunt principalele cauze ale decesului în primii 2 ani de viață. În schimb, boala Pompe cu debut la adulți este o boală lent progresivă a miopatiei proximale cu creatin kinază crescută și implicarea ulterioară a mușchilor respiratori, rezultând insuficiență respiratorie. Implicarea cardiacă și complicațiile sale sunt rare [1, 2].
Deficitul de α-1,4-glucozidaza rezultă din mutații ale genei care codifică acidul α-1,4-glucozidază (gena GAA). Gena GAA este localizată pe cromozomul 17q25.2-q25.3, cu o lungime de aproximativ 20 kbp și constă din 20 de exoni [3]. Până în prezent, peste 300 de mutații ale genei GAA au fost descrise în baza de date a mutației bolii Pompe și în baza de date a mutației genelor umane (HGMD). Cu toate acestea, datele privind mutația genetică a bolii Pompe cu debut la adulți din Asia de Sud-Est, în special pacienții din Malaezia de origine chineză, sunt limitate. În această lucrare, prezentăm un caz de mutație nouă a bolii Pompe cu debut la adulți la un pacient chinez din Malaezia.
2. Raport de caz
O doamnă chineză în vârstă de 28 de ani a fost internată la serviciul de neurologie al spitalului Kuala Lumpur în decembrie 2005, cu slăbiciune musculară proximală progresivă pe o durată de 5 ani. Cu două săptămâni înainte de internare, avea o slăbiciune bilaterală a membrelor superioare și inferioare, cu toleranță redusă la efort și dificultăți de respirație, făcând-o incapabilă să meargă. Într-o zi, respirația ei s-a înrăutățit, necesitând o ventilație asistată. În acest moment, a fost tratată pentru o polineuropatie postinfecțioasă. Istoria familiei nu a dezvăluit vreo consanguinitate, iar istoria nașterii a fost de neînțeles. Este cea mai mică dintre cei trei frați.
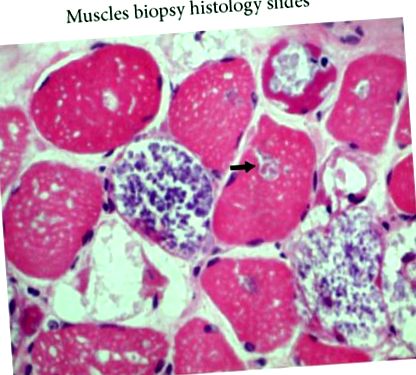
Colorarea hematoxilinei și a eozinei (H&E) prezintă miopatie vacuolară.
Analiza moleculară a ADN-ului a relevat două mutații heterozigoice compuse la c.444C> G (p.Tyr14
) în exonul 2 și c.2238G> C (p.Trp746Cys) în exonul 16. Prima mutație la c.444C> G a arătat o schimbare de nucleotide la codonul 148 introducând un codon stop prematur. Această mutație perturbă îmbinarea normală și se prevede că va produce un acid trunchiat α-glucozidaza. Această mutație descrisă este o mutație nouă și nu a fost raportată anterior atât în HGMD, cât și în bazele de date despre mutația bolii Pompe. Analiza omologică a mutației noi a arătat că localizarea mutației la codonul 148 se află într-o regiune foarte conservată (Figura 3). A doua mutație la c.2238G> C determină o schimbare de la triptofan aromatic nepolar la cisteină alifatică polară la codonul 746 și se știe că afectează funcția enzimatică a acidului α-glucozidază [4] (vezi Figura 4).
Electroferograme de secvență ADN ale celor doi compuși heterozigoti detectați la acest pacient. C.444C> G (p.Tyr14
Ea a început în regim alimentar bogat în proteine (1,2-1,5 g de proteine / kg/zi) cu fizioterapie continuă și sprijin de reabilitare. Din cauza slăbiciunii mușchilor respiratori și a parezei diafragmatice, a fost ventilată pe o durată totală de 9 luni. Acest lucru a fost complicat cu colapsuri pulmonare recurente. După 6 luni de regim alimentar bogat în proteine, a fost înțărcată cu succes din ventilator cu o traheostomie permanentă, suplimentată cu oxigen acasă folosind un concentrator. Puterea musculară a membrelor superioare s-a îmbunătățit la 5/5 pe scara MRC. Puterea musculară a gâtului și a membrelor inferioare proximale s-a îmbunătățit la 3-4/5 pe scara MRC. La descărcare de gestiune, a reușit să ambuleze fără ajutor pe distanțe scurte de 140 de metri în 6 minute și independent de activitățile zilnice de viață. Nivelul ei de creatin kinază a rămas ridicat la 691 U/L.
3. Discuție
Boala Pompe este o tulburare autozomală recesivă moștenită cauzată de o deficiență a enzimei lizozomale acid alfa-glucozidază (GAA). Expresia fenotipică apare atunci când ambele alele ale genei GAA adăpostesc o mutație patogenă și, în acest caz, așa cum se arată în analiza genetică, așa cum a fost descris mai devreme. Datele privind mutațiile genetice pentru debutul tardiv al bolii Pompe (copilărie, juvenil și adult) cu populația chineză sunt limitate, cu doar o mână de rapoarte din China [5] și Taiwan [4]. Majoritatea studiilor au analizat pacienții cu boală Pompe cu debut infantil. În acest caz, am identificat două mutații heterozigoice compuse într-un caz de boală Pompe severă cu debut tardiv, care a necesitat sprijin prelungit al ventilatorului la scurt timp după prezentare, care s-a îmbunătățit cu dieta bogată în proteine și terapia de substituție enzimatică (ERT).
Managementul actual al bolii Pompe cu debut la adulți este reducerea depunerii de glicogen în mușchiul scheletic prin modificarea dietei sau terapia de substituție enzimatică. Datele sunt disponibile pentru a susține utilizarea unei diete bogate în proteine în boala Pompe cu debut la adulți [11, 12]. Deficiența energetică subiacentă în boala Pompe produce o stare catabolică cronică cu potențialul de a afecta semnificativ funcția și conservarea mușchilor scheletici [13]. Acest aport scăzut de carbohidrați și proteine are ca scop reducerea catabolismului muscular, prevenind risipa de mușchi striat care compromite performanța fizică și duce la insuficiență respiratorie. Înainte de introducerea terapiei de substituție enzimatică, rezultatele terapiei cu conținut ridicat de proteine în boala Pompe cu debut la adulți au fost încurajatoare. Această dietă, în combinație cu exercițiile fizice programate, inversează acumularea de glicogen muscular și s-a dovedit că întârzie rata deteriorării clinice. S-a raportat că acest lucru este benefic și la pacienții cu insuficiență respiratorie [12]. Cu toate acestea, doar 25% din toți subiecții raportați au prezentat o îmbunătățire a funcției musculare sau respiratorii după o dietă bogată în proteine [14]. Acest lucru se datorează în principal respectării slabe a cantității mari de diete proteice necesare și consecințelor creșterii în greutate.
Până în prezent, terapia de substituție enzimatică (ERT) cu alglucozidază alfa este singurul tratament disponibil pentru boala Pompe cu debut tardiv la adulți. Datele rezultatelor clinice au sugerat că ERT a stabilizat deficitele neuromusculare peste un an [15] și a dus la o creștere a capacității vitale forțate prevăzute [16]. Studiul de tratament cu debut tardiv (LOTS) arată că beneficiile ERT în grupul de tratament (săptămână alternativă, doză de 20 mg/kg) observate în primele 26 de săptămâni de terapie și menținute pe parcursul celor 78 de săptămâni ale studiului [16] . Studiul LOTS arată un beneficiu modest, dar semnificativ statistic, în testul de mers pe jos de 6 minute. Cu toate acestea, acest beneficiu nu se traduce prin îmbunătățiri semnificative din punct de vedere funcțional. Acest lucru a ridicat posibilitatea ca doza de alglucozidază din săptămâna alternativă, 20 mg/kg să fie insuficientă la pacientul adult cu debut tardiv al lui Pompe. Doza prescrisă în prezent de alglucozidază s-a bazat pe beneficiile clinice ale bolii Pompe cu debut infantil [17].
În concluzie, raportăm o doamnă chinezească din Malaezia cu debut tardiv al bolii de depozitare a glicogenului de tip II din cauza a două mutații heterozigoice compuse. Analiza genetică a relevat o mutație nouă la c.444C> G (p.Tyr14) la exonul 2. Acest pacient are manifestare clinică tipică a bolii Pompe cu debut tardiv, cu slăbiciune musculară proximală și progresie rapidă către insuficiență respiratorie fără complicații cardiace. Identificarea timpurie a bolii și tratamentul cu dietă bogată în proteine și terapie de substituție enzimatică la pacienții cu această mutație nouă îmbunătățesc funcția musculară și au un impact benefic asupra supraviețuirii.
Abrevieri
| ERT: | Terapia de substituție enzimatică |
| GAA: | Acid α-1,4-glucozidaza |
| HGMD: | Baza de date a mutației genelor umane |
| MULTE: | Studiu de tratament cu debut tardiv |
| MRC: | Consiliul Cercetării Medicale |
| MUAP-uri: | Potențialele de acțiune ale unității motorii |
| rhGAA: | Acid uman recombinant α-glucozidaza. |
Aprobare etică
Acesta a fost obținut de la Registrul Național de Cercetări Medicale din Malaezia, NMRR-13-1144-18458. Toate procedurile urmate au fost în conformitate cu standardele etice ale comisiei responsabile pentru experimentarea umană (instituțională și națională) și cu Declarația de la Helsinki din 1975, revizuită în 2000 (5).
Consimţământ
Consimțământul informat a fost obținut de la pacientul inclus în acest raport de caz.
Conflict de interese
Dr. Hiew Fu Liong, Siti Aishah Abdul Wahab, Yusnita Yakob, Dr. Ngu Lock Hock, profesorul Dr. Wong Kum Thong și Dr. Shanthi Viswanathan declară că nu au niciun conflict de interese.
Contribuția autorilor
Dr. Hiew Fu Liong și Dr. Shanthi Viswanathan a fost responsabilă pentru conceptul și designul studiului. Dr. Hiew Fu Liong a contribuit la achiziționarea, analiza și interpretarea datelor. Dr. Hiew Fu Liong a fost, de asemenea, responsabil pentru redactarea lucrării. Dr. Hiew Fu Liong, Dr. Shanthi Viswanathan și Dr. Ngu Lock Hock a fost responsabil pentru revizuirea citării lucrării pentru conținut intelectual important. Diapozitivele și interpretarea histologică a biopsiei musculare au fost pregătite de profesorul Dr. Wong Kum Thong. Analiza moleculară a genei GAA și cromatograma a fost pregătită de Siti Aishah Abdul Wahab și Yusnita Yakob.
Confirmare
Autorii ar dori să mulțumească directorului general al sănătății din Malaezia pentru că le-a permis să publice acest studiu de caz.
Referințe
- N. Leslie și B. T. Tinkle, „Boala de depozitare a glicogenului de tip II (boala pompei)” GeneReviews, 2007. Vizualizare la: Google Scholar
- R. Hirschhorn și A. J. J. Reuser, „Boala de depozitare a glicogenului de tip II: deficit (acid maltazic)”, în Bazele metabolice și moleculare online ale bolilor moștenite (OMMBID), C. R. Scriver, A. L. Beaudet, W. S. Sly, D. Valle și B. Vogelstein, Eds., Capitolul 135, McGraw-Hill, New York, NY, SUA, 2013. Vezi la: Google Scholar
- L. H. Hoefsloot, M. Hoogeveen-Westerveld, A. J. J. Reuser și B. A. Oostra, „Caracterizarea lizozomului uman α-gena glucozidazei " Jurnal Biochimic, vol. 272, nr. 2, pp. 493–497, 1990. Vezi la: Google Scholar
- C. C. Yang, Y. H. Chien, N. C. Lee și colab., „Cursul rapid progresiv al bolii Pompe cu debut ulterior la pacienții chinezi” Genetică moleculară și metabolizare, vol. 104, nr. 3, pp. 284–288, 2011. Vizualizare la: Site-ul editorului | Google Scholar
- Qiu J. J., M. Wei, W. M. Zhang, J. J. Qiu, Y. Meng și Z. Q. Qiu, „Studiu genetic și molecular pe doi pacienți cu forma juvenilă a bolii Pompe în China”. Zhonghua er ke za zhi, vol. 45, nr. 10, pp. 760–764, 2007. Vezi la: Google Scholar
- L. Wan, C.-C. Lee, C.-M. Hsu și colab., „Identificarea a opt mutații noi ale acidului α-gena glucozidazei care cauzează forma infantilă sau juvenilă a bolii de depozitare a glicogenului de tip II, ” Jurnalul de Neurologie, vol. 255, nr. 6, pp. 831–838, 2008. Vizualizați la: Site-ul editorului | Google Scholar
- M. Hagemans, L. Winkel, P. van Doorn și colab., "Manifestarea clinică și cursul natural al bolii Pompe cu debut tardiv la 54 de pacienți olandezi" Creier, vol. 128, nr. 3, pp. 671–677, 2005. Vizualizare la: Site-ul editorului | Google Scholar
- W. Müller-Felber, R. Horvath, K. Gempel și colab., „Boala Pompe cu debut tardiv: spectru clinic și neurofiziologic de 38 de pacienți, inclusiv urmărire pe termen lung la 18 pacienți”. Tulburări neuromusculare, vol. 17, nr. 9-10, pp. 698–706, 2007. Vizualizare la: Site-ul editorului | Google Scholar
- C. F. Boerkoel, R. Exelbert, C. Nicastri și colab., „Mutația cu splicing scurgeri în gena acidă a maltezei este asociată cu debutul întârziat al glicogenozei de tip II”. American Journal of Human Genetics, vol. 56, nr. 4, pp. 887–897, 1995. Vizualizare la: Google Scholar
- A. Herzog, R. Hartung, A. J. J. Reuser și colab., „Un studiu transversal cu un singur centru asupra spectrului bolii Pompe, pacienții germani: analiza moleculară a genei GAA, manifestarea și corelațiile genotip-fenotip”. Jurnalul Orphanet al bolilor rare, vol. 7, nr. 1, articolul 35, 2012. Vizualizați la: Site-ul editorului | Google Scholar
- A. E. Slonim, R. A. Coleman, M. A. McElligot și colab., „Îmbunătățirea funcției musculare în deficiența acidă a maltazei prin terapie cu conținut ridicat de proteine”. Neurologie, vol. 33, nr. 1, pp. 34–38, 1983. Vizualizare la: Site-ul editorului | Google Scholar
- M. L. Margolis și A. R. Hill, „Deficitul de maltază acidă la un adult. Dovezi pentru îmbunătățirea funcției respiratorii cu terapia dietetică bogată în proteine " Revista americană a bolilor respiratorii, vol. 134, nr. 2, pp. 328–331, 1986. Vizualizare la: Google Scholar
- J. M. Pascual și C. R. Roe, „Anomalii metabolice sistemice în deficitul de maltază acidă cu debut la adulți dincolo de acumularea de glicogen muscular”. JAMA Neurologie, vol. 70, nr. 6, pp. 756–763, 2013. Vizualizare la: Site-ul editorului | Google Scholar
- O. A. F. Bodamer, J. V. Leonard și D. Halliday, „Tratamentul dietetic în deficitul de maltază acidă cu debut tardiv” Jurnalul European de Pediatrie, vol. 156, nr. 1, pp. S39 - S42, 1997. Vizualizare la: Site-ul editorului | Google Scholar
- S. Strothotte, N. Strigl-Pill, B. Grunert și colab., „Terapia de substituție enzimatică cu alglucozidază alfa la 44 de pacienți cu debut tardiv al bolii de depozitare a glicogenului tip 2: rezultate pe 12 luni ale unui studiu clinic observațional”. Jurnalul de Neurologie, vol. 257, nr. 1, pp. 91–97, 2010. Vizualizați la: Site-ul editorului | Google Scholar
- A. T. van der Ploeg, P. R. Clemens, D. Corzo și colab., "Un studiu randomizat al alglucozidazei alfa în boala Pompe cu debut tardiv" The New England Journal of Medicine, vol. 362, nr. 15, pp. 1396–1406, 2010. Vizualizați la: Site-ul editorului | Google Scholar
- P. S. Kishnani, D. Corzo, M. Nicolino și colab., „Acid uman recombinant α-glucozidaza: beneficii clinice majore în boala Pompe cu debut infantil ” Neurologie, vol. 68, nr. 2, pp. 99–109, 2007. Vizualizare la: Site-ul editorului | Google Scholar
- A. Toscano și B. Schoser, „Terapia de substituție enzimatică în boala Pompe cu debut tardiv: o revizuire sistematică a literaturii” Jurnalul de neurologie, vol. 260, nr. 4, pp. 951–959, 2013. Vizualizare la: Site-ul editorului | Google Scholar
- D. Güngör, M. E. Kruijshaar, I. Plug și colab., „Impactul terapiei de substituție enzimatică asupra supraviețuirii la adulții cu boala Pompe: rezultatele unui studiu observațional internațional prospectiv”. Jurnalul Orphanet al bolilor rare, vol. 8, nr. 49, nr. 1, 2013. Vizualizare la: Site-ul editorului | Google Scholar
- Sindromul Liddle datorat unei mutații noi în subunitatea γ a canalului epitelial de sodiu (ENaC) în
- HCG Drops Instrucțiuni de stocare pentru eficacitate maximă - Do-It-Yourself HCG
- Huntington WV Gastroenterolog Medici - Boala Crohn Semne timpurii, simptome, dietă, cauze,
- Vindecarea naturală a cistitei interstițiale - Mama mea; Povestea bolii cronice
- Vindecarea tipului 1 Diabet Kefir probiotic