medicamente casnice lista a-z efecte secundare centru medicamentos soluție lactuloză (soluție lactuloză) medicament
Ce este Lactuloza și cum se utilizează?
Soluția de lactuloză este o dizaharidă sintetică, un tip de zahăr care este descompus în intestinul gros în acizi ușori care atrag apă în colon, care ajută la înmuierea scaunelor. Soluția de lactuloză este utilizată pentru a trata constipația cronică. Soluția de lactuloză este, de asemenea, utilizată pentru a trata sau preveni complicațiile bolilor hepatice (encefalopatie hepatică). Soluția de lactuloză este disponibilă sub formă generică.
Care sunt efectele secundare ale lactulozei?
Efectele secundare ale soluției de lactuloză includ:
- diaree,
- greaţă,
- vărsături,
- balonare,
- gaz,
- eructații și
- dureri de stomac sau disconfort.
PENTRU ADMINISTRAREA ORALĂ ȘI RECTALĂ PENTRU PREVENIREA ȘI TRATAMENTUL ENCEFALOPATIEI PORTAL-SISTEMICE
DESCRIERE
Lactuloza este o dizaharidă sintetică sub formă de soluție pentru administrare orală sau rectală. Fiecare 15 ml de soluție de lactuloză USP conține 10 g de lactuloză (și mai puțin de 1,6 g de galactoză, mai puțin de 1,2 g de lactoză și 0,1 g sau mai puțin de fructoză). De asemenea, conține D&C Yellow No. 10, FD & C Yellow Nr. 6 și apă purificată.
Lactuloza este un acidifiant colonic pentru tratamentul și prevenirea encefalopatiei portal-sistemice.
Denumirea chimică pentru lactuloză este 4-O-β-D-galactopiranozil-D-fructofuranoză. Are următoarea formulă structurală:
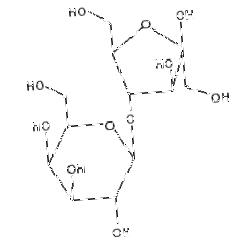 |
Greutatea moleculară este 342,30. Este liber solubil în apă.
INDICAȚII
Pentru prevenirea și tratamentul encefalopatiei portal-sistemice, inclusiv etapele pre-comă și comă hepatică.
Studiile controlate au arătat că terapia cu soluție de lactuloză reduce nivelul de amoniac din sânge cu 25 până la 50%; acest lucru este în general paralel cu o îmbunătățire a stării mentale a pacienților și cu o îmbunătățire a tiparelor EEG. Răspunsul clinic a fost observat la aproximativ 75% dintre pacienți, ceea ce este cel puțin la fel de satisfăcător ca cel rezultat din terapia cu neomicină. O creștere a toleranței la proteine a pacienților este, de asemenea, frecvent observată cu terapia cu lactuloză. În tratamentul encefalopatiei portal-sistemice cronice, lactuloza a fost administrată de peste 2 ani în studii controlate.
SLIDESHOW
DOZAJ SI ADMINISTRARE
Adult: Doza orală obișnuită pentru adulți este de 2 până la 3 linguri (30 până la 45 ml, conținând 20 g până la 30 g lactuloză) de trei sau patru ori pe zi. Dozajul poate fi ajustat în fiecare zi sau două pentru a produce 2 sau 3 scaune moi zilnic.
Se pot utiliza doze orare de 30 până la 45 ml soluție de lactuloză pentru a induce laxarea rapidă indicată în faza inițială a terapiei cu encefalopatie sistemică portal. Când s-a atins efectul laxativ, doza de lactuloză poate fi redusă la doza zilnică recomandată. Îmbunătățirea stării pacientului poate apărea în decurs de 24 de ore, dar nu poate începe înainte de 48 de ore sau chiar mai târziu.
Terapia continuă pe termen lung este indicată pentru a diminua severitatea și a preveni recurența encefalopatiei portal-sistemice. Doza de lactuloză în acest scop este aceeași cu doza zilnică recomandată.
Copii: S-au înregistrat foarte puține informații despre utilizarea lactulozei la copii mici și adolescenți. Ca și în cazul adulților, obiectivul subiectiv al unui tratament adecvat este de a produce 2 sau 3 scaune moi zilnic. Pe baza informațiilor disponibile, doza orală inițială zilnică recomandată la sugari este de 2,5 până la 10 ml în doze divizate. Pentru copiii mai mari și adolescenții, doza zilnică totală este de 40 până la 90 ml. Dacă doza inițială provoacă diaree, doza trebuie redusă imediat. Dacă diareea persistă, lactoza trebuie întreruptă.
Rectal
Când pacientul adult se află în stadiul de comă sau comă iminentă a encefalopatiei portal-sistemice și există pericolul aspirației sau când procedurile endoscopice sau de intubație necesare interferează fizic cu administrarea dozelor orale recomandate, soluția de lactuloză poate fi administrată ca clisma de retenție printr-un cateter cu balon rectal. Nu trebuie folosite clisme de curățare care conțin spumă de săpun sau alți agenți alcalini.
Trei sute de ml de soluție de lactuloză trebuie amestecate cu 700 ml de apă sau ser fiziologic și păstrate timp de 30 până la 60 de minute. Clisma lactuloza poate fi repetată la fiecare 4 până la 6 ore. Dacă această clismă lactuloză este evacuată din greșeală prea rapid, aceasta poate fi repetată imediat.
Scopul tratamentului este inversarea stadiului de comă pentru ca pacientul să poată lua medicamente orale. Inversarea comei poate avea loc în decurs de 2 ore de la prima clismă la unii pacienți. Lactuloza administrată pe cale orală în dozele recomandate trebuie începută înainte ca lactuloza prin clismă să fie întreruptă în totalitate.
CUM FURNIZAT
Soluție de lactuloză USP (Soluție orală sau rectală), 10 g/15 ml, este o soluție limpede, de la galben la galben-auriu, livrată într-o sticlă de o halbă (473 ml) și două litri (1,89 L). Soluția de lactuloză conține: 667 mg lactuloză/ml (10 g/15 ml).
A se păstra la 25 ° C (77 ° F); excursii permise la 15-30 ° C (59-86 ° F) (vezi temperatura camerei controlată de USP). Nu înghețați. A se ține bine închis.
În condițiile de depozitare recomandate, poate apărea o întunecare normală a culorii. O astfel de întunecare este caracteristică soluțiilor de zahăr și nu afectează acțiunea terapeutică.
Expunerea prelungită la temperaturi de peste 30 ° C (86 ° F) sau la lumină directă poate provoca întunecări extreme și turbiditate care pot fi inacceptabile farmaceutic. Dacă această afecțiune se dezvoltă, nu utilizați. Expunerea prelungită la temperaturi de îngheț poate provoca schimbarea într-un semisolid, prea vâscos pentru a fi turnat. Vâscozitatea va reveni la normal după încălzirea la temperatura camerei.
Distribuiți într-un recipient etanș, rezistent la lumină, așa cum este definit în USP, cu o închidere rezistentă la copii.
Fabricat de: Novex Pharma, Richmond Hill, Ontario Canada L4C 5H2. Fabricat pentru: Apotex Corp. Weston, FL 33326. Iulie 2003. Data revizuirii FDA: 28.07.2003
- Utilizări, efecte secundare, dozare, interacțiuni și beneficii pentru sănătate
- Utilizări cu indiu, efecte secundare, interacțiuni, dozare și avertisment
- Efecte secundare ale lactulozei, dozare, utilizări și multe altele
- Utilizări orale ale lactulozei, efecte secundare, interacțiuni, imagini, avertismente; Dozare - WebMD
- Citrat de magneziu (Citrat de magnezie) - Efecte secundare, interacțiuni, utilizări, dozare, avertismente
